Материал: Спектры люминесценции Ln3+ в кристаллах твердых растворов со структурой шеелита
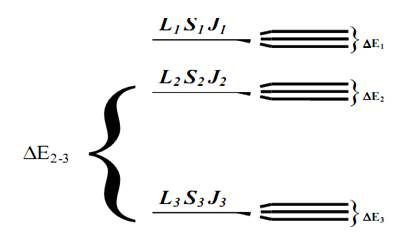
Рисунок 5 - Схема энергетических уровней
= 0, 1, 2, 3, 4, 5, 6,P,D,F,G,H,I,
Набор этих чисел записываются в следующем виде - 2S+1LJ. Например, для основного состояния иона неодима 4I9/2, что означает S=3/2, L=6, J=9/2. Из квантовых чисел можно так же определить количество подуровней на которые данный энергетический уровень расщепился. Количество подуровней будет равно S+1/2. Например, для уровня 4I15/2 количество подуровней будет равно 8. Неоднородное и однородное уширение. Спектры поглощения и люминесценции кристаллов, активированных ионами редкоземельных элементов, состоят из отдельных групп узких линий. Каждая группа представляет собой штарковскую структуру, возникающую из-за расщепления атомных уровней основного и возбуждённого состояний, характеризуемых моментами J и J'. Таким образом, группе приписывают оптический переход в свободном атоме S,L,J → S',L',J', с которым она связана генетически. Если сравнить спектры одного и того же РЗ иона в разных кристаллах, то окажется, что число линий в S,L,J → S',L',J' группе, характер их расположения и относительные интенсивности различны. Эти характеристики связаны с особенностями ближайшего окружения РЗ иона (строением РЗ центра). Анализ штарковской структуры спектра позволяет получить информацию о строении оптического РЗ центра, в частности, определить его симметрию. В спектрах стёкол в тех же диапазонах частот, где в случае кристаллов имеются группы узких линий, наблюдаются размытые полосы с более или менее выраженными максимумами. Они выглядят так, как если бы линии спектра кристалла увеличили ширину, оставаясь на прежнем месте, и частично наложились друг на друга. Типичные значения ширины линий для перехода между парой отдельных штарковских уровней в случае кристаллов ≈10 см-1, в случае стёкол ≈100 см-1.
С чем связано такое различие спектров стёкол и кристаллов? Сравним структуру стёкол и кристаллов. Основным свойством кристалла является упорядоченность его структуры, которая характеризуется как точечной, так и пространственной симметрией. Поэтому атомы в кристалле занимают совершенно определённые места (положения). Число различного типа мест для атомов в кристалле невелико. Все "места" одного типа сбольшой точностью можно считать идентичными. Когда ионы активаторы занимают место определённого типа, то все они оказываются в одинаковом положении. Окружение действует на них одинаковым образом, штарковские расщепления уровней и спектральных линий для них одинаковы.
Иная ситуация в стекле, где в расположении атомов приблизительно сохраняется ближний порядок, а дальний порядок отсутствует. Поэтому, строго говоря, положения всех атомов в стекле различны, положения некоторых приблизительно схожи. С химической точки зрения лазерные стёкла представляют собой сплавы окислов. Число различных окислов в промышленном стекле может достигать десятка. Среди этих окислов выделяют "главный", благодаря наличию которого сплав при охлаждении переходит в стеклообразное состояние, а не кристаллизуется. Этот окисел называют "стеклообразователем", в процентном отношении его количество составляет примерно половину или больше от всего состава. Другие окислы называются "модификаторами". Самым распространённым стеклообразователем, на основе которого получают почти все оптические стёкла, является SiO2. Соответствующие стёкла называются "силикатными". В квантовой электронике используются также "фосфатные" стёкла, в которых стеклообразователем является P2O5. Согласно исследованиям структуры стёкол с помощью рассеяния рентгеновских лучей и нейтронов только вокруг атомов стеклообразователей имеет место ближний порядок. А именно, подавляющее число атомов кремния в силикатных стёклах и атомов фосфора в фосфатных стёклах находится в центре тетраэдров из атомов кислорода. Катионы модификаторы, в том числе редкоземельные ионы, не имеют определённого координационного числа. Кроме того, даже в случае фиксированного координационного числа конфигурации лигандов могут меняться в очень широких пределах.
Таким образом, в стекле каждый из РЗ ионов находится в своём специфическом поле, которое отлично от полей, действующих на другие ионы. Строго говоря, все оптические центры различны, а значит, у них различаются штарковские расщепления уровней и штарковская структура спектров. Спектр, наблюдаемый в условиях обычного эксперимента, есть результат наложения спектров отдельных центров (рисунок6). Понятно, что такое наложение проявляется в виде уширения спектральных линий.
Уширение спектральных полос, обусловленное тем,
что энергия оптических переходов различна у разных центров внутри одного
образца, называется неоднородным.
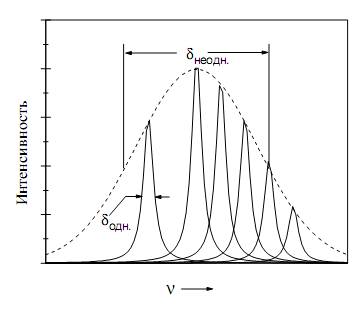
Рисунок 6 - Спектр люминесценции
Ширина спектральных линий отдельных центров
называется однородной. В настоящей лабораторной работе исследуется
люминесценция очень важного класса оптических материалов - кристаллов и стёкол,
активированных ионами неодима. Такие материалы являются самым массово
производимым лазерным материалом. Их используют как в огромных установках для
термоядерного лазерного синтеза, так и в миниатюрных лазерах, размеры которых
не превышают нескольких миллиметров. Такое широкое распространение связано с
тем, что на ионах неодима возможно получить высокие мощности излучения,
различные режимы генерации (импульсный, непрерывный), а также низкие пороговые
уровни генерации за счет четырехуровневой схемы. Генерация лазерного излучения
происходит на трех переходах (рисунок. 7). Большинство лазеров работает на
переходе 4F3/2→4I11/2с длиной волны 1,06 мкм. Ионы неодима обладают
интенсивными полосами поглощения в широком спектральном диапазоне, поэтому для
накачки неодимовых лазеров и усилителей света широко используются импульсные
лампы. В последнее время получило распространение использование для накачки
лазерных диодов, которые излучают в ИК диапазоне, что сильно увеличивает КПД
таких лазеров.
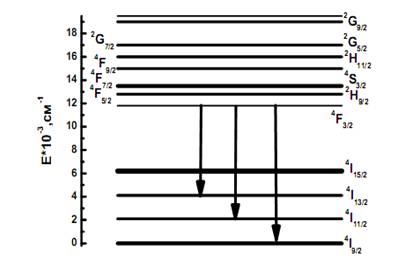
Рисунок 7 - Схема энергетических уровней и
лазерных переходов иона неодима
1.5 Твердые растворы. Типы диаграмм
состояния. Твердые растворы шеелитов
Твердые растворы - это фазы, содержание компонентов в которых может изменяться без нарушения типа кристаллической решетки основного компонента. В зависимости от способа размещения атомов в кристаллической решетке различают следующие типы твердых растворов - замещения, внедрения и вычитания.
Способность образовывать твёрдые растворы свойственна всем кристаллическим твёрдым телам <#"800869.files/image028.jpg">
Рисунок 8 - Кристаллическая решетка
твердых растворов
Типы диаграмм состояния. На
диаграмме состояния
<#"800869.files/image029.gif"> соотв.) и
область сосуществования обеих фаз (Ж + ![]() ). Тип б встречается крайне редко,
главным образом в случае оптич. изомеров орг. веществ. В системах с
непрерывными твердыми растворами, согласно принципу соответствия, должна быть
только одна кривая ликвидуса и одна кривая солидуса. Поэтому в точке минимума
или максимума происходит плавный переход одной части кривой в другую.
). Тип б встречается крайне редко,
главным образом в случае оптич. изомеров орг. веществ. В системах с
непрерывными твердыми растворами, согласно принципу соответствия, должна быть
только одна кривая ликвидуса и одна кривая солидуса. Поэтому в точке минимума
или максимума происходит плавный переход одной части кривой в другую.
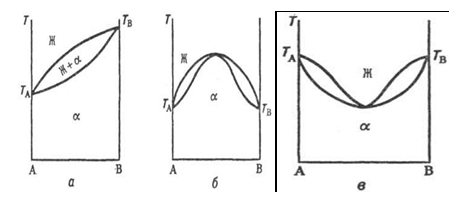
Рисунок 9 - Диаграммы состояний
<#"800869.files/image029.gif">-pаствоp,
образуются лишь до определенной концентрации
<#"800869.files/image031.gif">-pаствоpa, концентрация
<#"800869.files/image029.gif"> и ![]() , составы
которых по мере снижения температуры изменяются в соответствии с ходом линий GM
и FN (рисунок 10, а). Образование подобных твердых растворах наблюдается,
например, в системах Сu-Ag, Pb-Sn. Во втором случае твердые растворы образуют
перитектику-нонвариантную точку также трехфазного равновесия, но расположенную
по одну сторону от точек состава твердый раствор. (точка Р, рисунок 10,б).
Примером системы перитектич. типа может служить Cd-Hg.
, составы
которых по мере снижения температуры изменяются в соответствии с ходом линий GM
и FN (рисунок 10, а). Образование подобных твердых растворах наблюдается,
например, в системах Сu-Ag, Pb-Sn. Во втором случае твердые растворы образуют
перитектику-нонвариантную точку также трехфазного равновесия, но расположенную
по одну сторону от точек состава твердый раствор. (точка Р, рисунок 10,б).
Примером системы перитектич. типа может служить Cd-Hg.
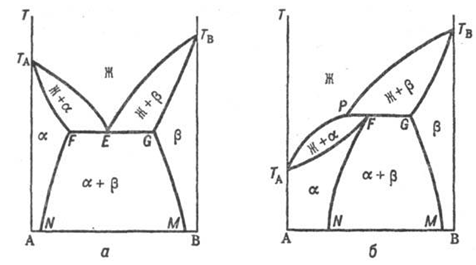
Рисунок 10 - Диаграммы состояния
<#"800869.files/image029.gif"> и ![]() : а-система с эвтектичной точкой Е;
б-система с перитектич. точкой Р. Остальные обозначения те же, что и на рисунке
9
: а-система с эвтектичной точкой Е;
б-система с перитектич. точкой Р. Остальные обозначения те же, что и на рисунке
9
На линиях ликвидуса ограниченных твердых растворов иногда встречаются экстремальные точки-минимум или (чаще) максимум. Последнее характерно для солевых и оксидных систем только в случае гетеровалентных твердых растворов (см. ниже) с переменным числом ионов <#"800869.files/image033.gif">
Рисунок 11 - Распад непрерывного
твердого раствора с образованием двухфазной системы. Жирная линия - бинодаль,
отделяющая область существования твердого раствора от области существования
двухфазной системы
При охлаждении однородного раствора
ниже критич. температуры растворимости (смешения) (точка К) образуется
двухфазная система, состоящая из несмешивающихся Твердыеpастворы a1 и a2
(рисунок 11), составы которых изменяются с температурой по линиям KL и KN
соответственно. Дркугой тип распада твердых растворов a наблюдается, если
компоненты А и В могут образовать хим. соед. АmВn (рисунок 12),
характеризующееся упорядоченным расположением частиц (атомов или ионов) в
кристаллической решетке, в отличие от статистического беспорядка в расположении
частиц, характерного для твердых растворов. На основе АmВn образуется твердый
раствор ![]() с
компонентами А и В. Превращение в упорядоченную фазу (сегрегация) может
происходить как фазовый переход <#"800869.files/image034.gif">
с
компонентами А и В. Превращение в упорядоченную фазу (сегрегация) может
происходить как фазовый переход <#"800869.files/image034.gif">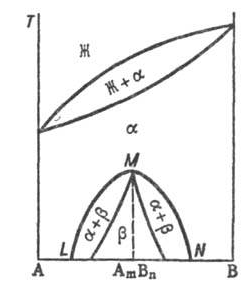
Рисунок 12 - Распад непрерывного
твердого раствора с образованием хим. соед. АmВn. Жирная линия-т-ра начала кристаллизации
<#"800869.files/image031.gif"> на основе
АmВn.
Полиморфизм. С полиморфным
превращением вещества, на основе которого образуется твердый раствор, всегда
связано и превращение твердых растворов. На рисунке 13 приведены диаграммы
состояния <#"800869.files/image029.gif"> и ![]() ,
образующихся на основе двух модификаций компонента А, с твердым раствором g на
основе компонента В расположена ниже температуры Тн полиморфного превращения, а
область гомогенности Твердые растворы на основе низкотемпературной модификации
(b) уже, чем на основе высокотемпературной (a); при перитектоидном (рисунок 13,
б) - наоборот.
,
образующихся на основе двух модификаций компонента А, с твердым раствором g на
основе компонента В расположена ниже температуры Тн полиморфного превращения, а
область гомогенности Твердые растворы на основе низкотемпературной модификации
(b) уже, чем на основе высокотемпературной (a); при перитектоидном (рисунок 13,
б) - наоборот.
![]()
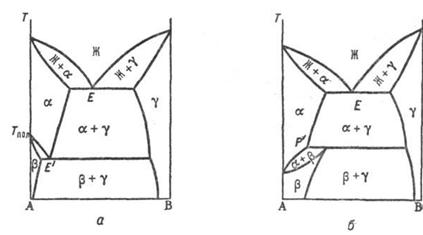
Рисунок 13 - Диаграммы состояния <#"800869.files/image037.gif">
Рисунок 14 - Диаграмма состояния сплавов с
неограниченной растворимостью компонентов в твердом состоянии и кривые
охлаждения типичных сплавов а) - диаграмма состояния сплавов с неограниченной
растворимостью компонентов в твердом состоянии; б) - кривые охлаждения типичных
сплавов
Проведем анализ полученной диаграммы.
. Количество компонентов: К = 2 (компоненты А и В).
. Число фаз: f = 2 (жидкая фаза L, кристаллы твердого раствора α).
. Основные линии диаграммы:- линия ликвидус, выше этой линии сплавы находятся в жидком состоянии;- линия солидус, ниже этой линии сплавы находятся в твердом состоянии.
. Характерные сплавы системы:
Чистые компоненты А и В кристаллизуются при постоянной температуре, кривая охлаждения компонента В представлена на рисунке 14, позиция б. Остальные сплавы кристаллизуются аналогично сплаву I, кривая охлаждения которого также представлена на рисунке 14, позиция б.
Процесс кристаллизации сплава I до точки 1
охлаждается сплав в жидком состоянии. При температуре, соответствующей точке 1,
начинают образовываться центры кристаллизации твердого раствора α.
На
кривой охлаждения отмечается перегиб (критическая точка), связанный с
уменьшением скорости охлаждения вследствие выделения скрытой теплоты
кристаллизации. На участке 1-2 идет процесс кристаллизации, протекающий при
понижающейся температуре, так как согласно правилу фаз в двухкомпонентной
системе при наличии двух фаз (жидкой и кристаллов твердого раствора α)
число
степеней свободы будет равно единице С = 2 - 2 + 1 = 1. При достижении
температуры соответствующей точке 2, сплав затвердевает, при дальнейшем
понижении температуры охлаждается сплав в твердом состоянии, состоящий из
однородных кристаллов твердого раствора α.
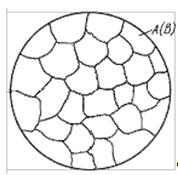
Рисунок 15 - Схема микроструктуры сплава -
однородного твердого раствора
. Количественный структурно-фазовый анализ сплава.
Пользуясь диаграммой состояния можно для любого сплава при любой температуре определить не только число фаз, но и их состав и количественное соотношение. Для этого используется правило отрезков. Для проведения количественного структурно-фазового анализа через заданную точку проводят горизонталь (коноду) до пересечения с ближайшими линиями диаграммы (ликвидус, солидус или оси компонентов).
Определение состава фаз в точке m:
Для его определения через точку m проводят горизонталь до пересечения с ближайшими линиями диаграммы: ликвидус и солидус.
Состав жидкой фазы определяется проекцией точки пересечения горизонтали с линией ликвидус p на ось концентрации. Состав твердой фазы определяется проекцией точки пересечения горизонтали с линией солидус q (или осью компонента) на ось концентрации.
Состав жидкой фазы изменяется по линии ликвидуса, а состав твердой фазы - по линии солидуса.
С понижением температуры состав фаз изменяется в сторону уменьшения содержания компонента В.
Определение количественного соотношения жидкой и твердой фазы при заданной температуре (в точке m):
Количественная масса фаз обратно пропорциональна отрезкам проведенной коноды. Рассмотрим проведенную через точку m коноду и ее отрезки.
Количество всего сплава (Qсп) определяется отрезком pq.
Отрезок, прилегающий к линии ликвидус pm,
определяет количество твердой фазы:
![]()
Отрезок, прилегающий к линии солидус (или к оси
компонента) mq, определяет количество жидкой фазы:
![]()
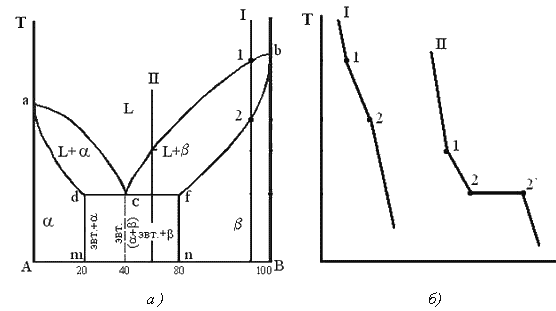
Рисунок 16 - Диаграмма состояния сплавов с
ограниченной растворимостью компонентов в твердом состоянии и кривые охлаждения
типичных сплавов а) - диаграмма состояния сплавов с ограниченной растворимостью
компонентов в твердом состоянии; б) - кривые охлаждения типичных сплавов
Проведем анализ диаграммы состояния <#"800869.files/image042.jpg">
Рисунок 17 - Зависимости частот КР
колебательных мод от составов твердых растворов шеелитов [7]
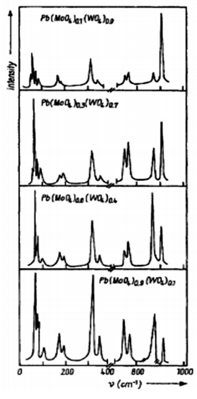
Рисунок 18 - Cпектры КРтвердых растворов
Pb(MoO4)x(WO4)1-x [5]
Кристаллы вольфрамата бария, а также вольфраматов и молибдатов стронция и бария являются универсальными ВКР-средами, обеспечивающими высокую эффективность ВКР-преобразования как в нано- так и в пикосекундном диапазонах накачки, в сравнении с большинством известных кристаллических материалов.
Анализ литературных данных показывает отсутствие
возможности выращивания монокристаллов вольфраматов и молибдатов бария и
стронция крупного размера и высокого оптического качества традиционным
высокоградиентным методом Чохральского. Для создания методики получения
кристаллов, удовлетворяющих требованиям устройств для
ВКР-преобразования,необходимо комплексное исследование особенностей
кристаллизации данных материалов и поиск возможностей обеспечения оптимальных
условий выращивания на базе стандартного ростового оборудования при минимуме
временных и материальных затрат.
1.6 Явление комбинационного
рассеяния света. Вынужденное комбинационное рассеяние света (ВКР) в кристаллах
вольфраматов и молибдатов щелочноземельных металлов
Явление комбинационного рассеяния света состоит
в том, что в снектре излучения, прошедшего через газы, жидкости или кристаллы,
помимо песмещенной линии содержатся новые линии, частоты которых представляют
собой комбинацию частоты щ и частот колебательных или вращательных переходов: ![]() .
Спектр рассеяния содержитиндивидуальный для данного вещества набор
комбинационных линий (сателлитов), расположенных симметрично относительно
возбуждающей линии. Интенсивности линий, смещенных в инфракрасную сторону
спектра
.
Спектр рассеяния содержитиндивидуальный для данного вещества набор
комбинационных линий (сателлитов), расположенных симметрично относительно
возбуждающей линии. Интенсивности линий, смещенных в инфракрасную сторону
спектра ![]() больше,
чем у соответствующих линий, смещенных в ультрафиолетовую область (
больше,
чем у соответствующих линий, смещенных в ультрафиолетовую область (![]() )[23].
Основными параметрами, характеризующими линии спектров комбинационного
рассеяния, являются:
)[23].
Основными параметрами, характеризующими линии спектров комбинационного
рассеяния, являются: