Материал: спектр и фотометр

Для испытания подлинности таблеток «ко-тримоксазола» могут быть использованы УФ-спектры поглощения. Хлороформное извлечение имеет максимум поглощения в области 246 нм и плечо 262-276 нм.
Подлинность подтверждают также методом ТСХ на пластинках Кизельгель при хроматографирование подвижной фазе состава хлоро- форм-ментол-раствор аммиака концентрированный (80:20:3). После проявления реактивом Драгендорфа должны обнаруживаться два основных пятна на уровне стандартных образцов веществ-свидетелей триметоприма и сульфаметоксазола.
Этим же методом обнаруживают в таблетках наличие посторонних примесей (не более 1%), сульфаниламида (стрептоцида) и кислоты сульфаниловой (не более 0,5% и 0,3% соответственно).
Количественное определение (по ФС) выполняют раздельно химическим методом на каждый из компонентов. Сульфаметоксазол определяют нитритометрическим методом. Точку эквивалентности определяют методом неводного титрования в смеси ледяной уксусной кислоты и уксусного ангидрида (30:10). Титруют 0,1М раствором хлорной кислоты (индикатор кристаллический фиолетовый).
Хранят «Ко-тримоксазол», как и другие сульфаниламиды в одном лекарственном препарате обеспечивает его высокую бактериостатическую активность, в том числе в отношении бактерий, устойчивых к другим сульфаниламидам.
Назначают «Ко-тримоксазол» при инфекциях дыхательных, мочевыводящих путей, ЖКТ, кожи и др.
Выпускают в таблетках по 0,12 и 0,48 г в виде суспензии (сиропа). Аналогичным по фармакологическому действию является отечествен-
ный препарат сульфатон. Выпускают его в виде таблеток, содержащих
0,25 г сульфамонометоксина и 0,1 триметоприма.
Замещенные сульфонилмочевины
Для идентификации алкилуреидов сульфокислот (гликлазида, глипизида, глибенкламида и др.) используют ИК-спектроскопию, подтвержденную данными ПМР-спектров. ИК-спектры лекарственных веществ, растёртых в вазелиновом масле, регистрируют в области 4000-650 см-1. Они должны соответствовать спектрам стандартных образцов.
Подлинность производных сульфонилмочевины также можно установить методом спектрофотометрии в УФ-области по расположению максимумов поглощения и по удельному показателю поглощения. Раствор карбутамида в этаноле имеет максимум при 269 нм, в 0,1 М растворе хлороводородной кислоты – при 266 и 272 нм, а в 0,1 М растворе гидроксида натрия – при 255 нм.
101
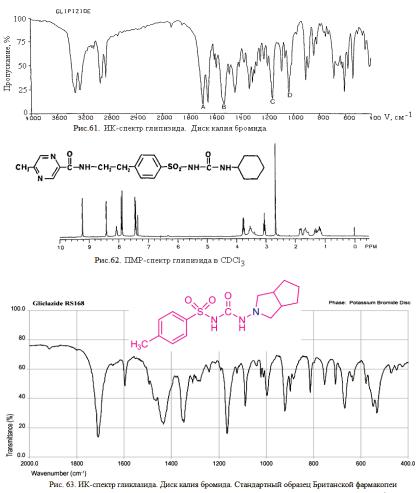
УФ-спектрраствора гликлазида имеет максимум поглощения при 228 нм, раствора глибенкламида в метаноле – три максимума (227, 273 и 293 нм), наибольшее значение удельного показателя поглощения (597) при длине волны 227 нм. Для подтверждения подлинности глипизида и гликвидона устанавливают идентичность УФ-спектров поглощения спектрам стандартных образцов этих лекарственных веществ.
Подлинность глипизида устанавливают также методом ВЭЖХ по времени удерживания испытуемого вещества, которое должно быть сопоставимым со временем удерживания стандарта.
102
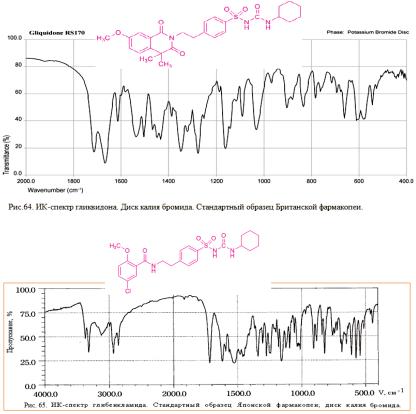
Для подтверждения подлинности гликвидона используют также метод ТСХ. Основное пятно на хроматограмме должно соответствовать по расположению и интенсивности флуорес-ценции основному пятну стандартного образца.
Методом ВЭЖХ в гликлазиде устанавливают допустимое содержание примесей (не более 0,2%) других производных сульфонилмочевины. Примесь остаточных растворителей (этилацетата) определяют методом
ГЖХ.
Количественное определение глибенкламида в таблетках выполняют методом спектрофотометрии. Для этого около 0,13 г (точная навеска) порошка растертых таблеток помещают в мерную колбу вместимостью 50 мл, прибавляют 20 мл спирта 95 %, перемешивают в течение 10 мин при нагревании на водяной бане до 50оС, охлаждают, доводят объем раствора тем же спиртом до метки, перемешивают и фильтруют через бумаж-
103

ный фильтр, отбрасывая первые 20 мл фильтрата. Измеряют оптическую плотность фильтрата на спектрофотометре в максимуме поглощения при длине волны 300 нм в кювете с толщиной слоя 10 мм.
Параллельно измеряют оптическую плотность раствора РСО гли-
бенкламида. В качестве раствора сравнения используют спирт 95 %. Содержание глибенкламида в одной таблетке в граммах (Х) вычисля-
ют по формуле:
где: А1 – оптическая плотность испытуемого раствора; Ао – оптическая плотность раствора РСО глибенкламида; а1 – навеска препарата, в г;
ао – навеска РСО глибенкламида (в пересчете на сухое вещество), в г; mср – средняя масса таблетки, в г.
Примечание. Приготовление раствора РСО глибенкламида. Около 0,05 г (точная навеска) глибенкламида помещают в мерную колбу вместимостью 50 мл, прибавляют 25 мл спирта 95%, перемешивают до растворения при нагревании на водяной бане до 50оС, охлаждают и доводят объем раствора тем же спиртом до метки (раствор А). 5 мл раствора (А) переносят в мерную колбу вместимостью 50 мл, доводят объем раствора спиртом 95 % до метки и перемешивают (раствор Б). 1 мл раствора Б содержит около 0,0001 г глибенкламида. Срок годности раствора Б – 1 сутки.
Содержание С23Н28СlN3О5S (глибенкламид) должно быть от 0,0045 до 0,0055 г, считая на среднюю массу одной таблетки.
Количественное определение глипизида осуществляют методом ВЭЖХ по стандартному образцу в следующих условиях:
колонка: 15 см х 3,9 мм; неподвижная фаза – октадецилсиликагель, 5 мкм;
подвижная фаза – буферный раствор (водные растворы мононатрийфосфата и натрия гидроксида до рН 6,0 ± 0.05) в смеси с метанолом
(55:45),
детектируют на спектрофотометре при длине волны 225 нм. Содержание глипизида в одной таблетке в граммах (Х) вычисляют по
формуле:
где: S и So – площади пиков на хроматограммах раствора испытуемого препарата и раствора СО глипизида, соответственно;
aо – навеска СО глипизида, г;
104
mср – средняя масса одной таблетки, г;
a – навеска порошка растертых таблеток, г.
Гликвидон и другие производные сульфонилмочевины в лекарственных формах количественно определяют методом УФ-спектрофотометрии в указанных выше максимумах поглощения.
Применение. Производные сульфонилмочевины стимулируют образование инсулина β-клетками поджелудочной железы, понижая при этом содержание сахара в крови. Назначают при различных формах сахарного диабета в виде таблеток; карбутамид по 0,5 г, глибенкламид по 0,005 г, гликлазид по 0,08 г, глипизид по 0,005 и 0,01 г, гликвидон по 0,03 г.
ПРОИЗВОДНЫЕ ГУАНИДИНА
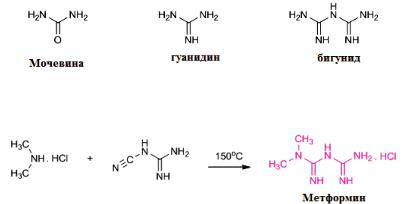
В 70-х гг. было установлено, что наряду с производными сульфонилмочевины противодиабетическим действием обладают также не содержащие сульфоксильного радикала вещества, в т. ч. производные бигуанида:
Производным бигуанида является метформин.
Синтезируют метформин из диметиламина гидрохлорида и дициандиамида (см. схемы 4):
Схема 4. Синтез метформина
Метформин легко растворим в воде (допускается опалесценция), мало и медленно растворим в этаноле, практически нерастворим в эфире.
Подлинность. ИК-спектр метформина, снятый после прессования в виде таблеток с бромидом калия, в области 2000-400 см-1 по положению и относительным интенсивностям полос должен полностью совпадать с приложенным к ФС рисунком спектра.
Для испытания подлинности и количественного определения метформина используют УФ-спектрофотометрию. Водный раствор должен иметь максимум поглощения в области 233 нм. В этом максимуме опре-
105