Материал: спектр и фотометр
тов благодаря наличию спина, и они ориентируются в магнитном поле аналогично тому, как стрелка компаса ориентируется в слабом магнитном поле Земли.
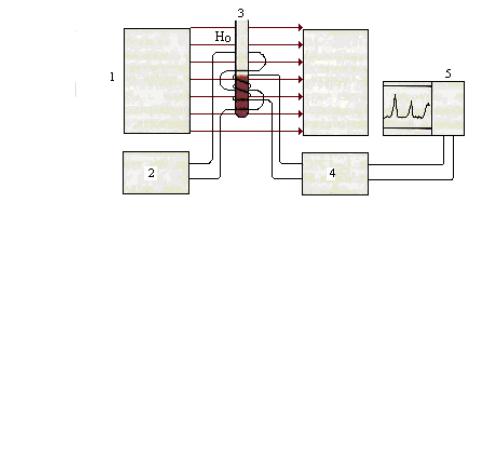
Такой метод становится возможным, если поместить образец в сильное магнитное поле, создаваемое большим постоянным магнитом или электромагнитом. Основные части прибора изображены на рисунке 25.
Частота поглощаемых радиоволн зависит от собственных магнитных свойств ядра и пропорциональна величине приложенного магнитного поля.
Ценность ЯМР для химической науки определяется прежде всего тем, что атомы водорода в различном химическом окружении (например, водород группы ОН и водороды группы C-СН3) поглощают при разных частотах радиоволн, потому что кроме приложенного магнитного поля Но имеется экранирующий эффект электронов, находящихся вблизи ядра. Разные ядра испытывают различную степень экранирования и, следовательно, поглощают различные частоты радиоволн.
Рис. 25. Спектрометр ЯМР записывает поглощение радиочастотного излучения образцом в магнитном поле. 1 – магнит с переменным магнитным полем Но; 2 – радиочастотный осциллятор; 3 – образец;
4 – радиочастотный приемник; 5 – записывающее устройство
Различия в частотах поглощения разных типов ядер водорода называются химическими сдвигами, и их можно использовать для идентификации типов водородов, присутствующих в неизвестном соединении
(см. рис. 26).
Представленные спектры иллюстрируют химические сдвиги протонов п-ксилола и трет-бутилацетата, а также подтверждают, что площади пиков пропорциональны числу атомов водорода, вызывающих их.
51
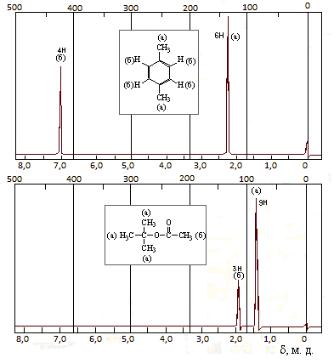
Рис. 26. ЯМР 1Н-спектр п-ксилола (а) и трет-бутилацетата (б)
Когда атомы водорода, имеющие различные химические сдвиги, находятся у одного и того же атома углерода или у соседних углеродов, спектр усложняется благодаря спин-спиновому взаимодействию, которое является результатом влияния магнитного поля одного ядра на ориентацию в магнитном поле всех близких магнитных ядер. Таким образом, каждый тип водорода может проявляться как мультиплет, как, например, в спектре 1,1,2-трихлорэтана, представленного на рисунке 27. Характер расщепления сигналов протонов можно предсказать, и он дает почти такую же ценную информацию, как химические сдвиги. Например, близко расположенные протоны, разделенные только двумя или тремя связями, обычно расщепляют сигналы друг друга на четкие мультиплеты. Суммарная площадь под пиками пропорциональна числу протонов, соответствующих каждому химическому сдвигу (см. рис. 27).
В настоящее время широко применяется ЯМР на ядрах 1Н, 19F, 13C, 31P, спиновое число которых равно1/2. Наиболее изучена спектроскопия ЯМР на протонах (ЯМР-1Н) и углеродах (ЯМР-13С) (см. табл. 5 и 6).
52
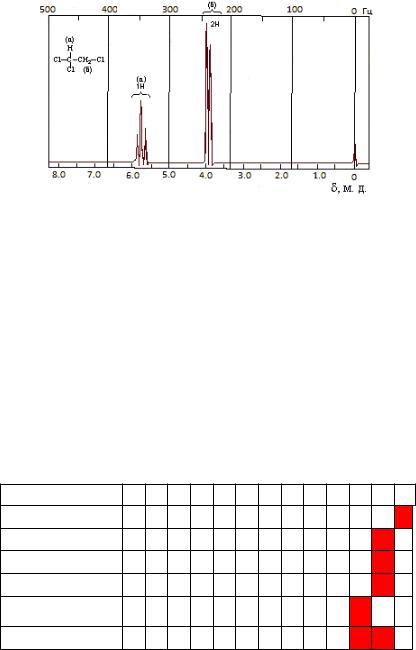
Рис. 27. ЯМР 1Н-спектр 1,1,2-трихлорэтана
Информативная ценность спектроскопии ЯМР базируется на том, что протон в зависимости от электронного окружения поглощает излучение различных частот, так как в разной степени экранируется магнитными полями электронов и ядер. Как выше уже указывалось, смещение резонансной частоты поглощения под влиянием электронного окружения называется химическим сдвигом. Его измеряют относительно выбранного стандарта – тетраметилсилана (СН3)4Si (ТМС), химический сдвиг протонов которого принят равным нулю.
Величина химических сдвигов протонов, как правило, зависит от электроотрицательности соседних атомов и групп. Электроноакцепторные заместители уменьшают электронную плотность вокруг данного протона (дезэкранируют его) и сдвигают сигнал в слабое поле по сравнению с протонами ТМС.
Таблица 5
Области химических сдвигов для ядер 1Н, δ, м.д.
Относительно ТМС |
12 11 10 9 |
8 |
7 |
6 |
5 |
4 |
3 |
2 |
1 |
0 |
H3C-алкил
H3C-C-галоген
H3C-C=C
H3C-C-C
H3C- арил, -гетероарил
H3C-CO
53
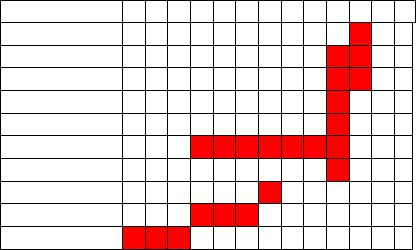
Относительно ТМС |
12 11 10 9 |
8 |
7 |
6 |
5 |
4 |
3 |
2 |
1 |
0 |
H3C-S-
H3C-SO2-
H3C-N
H3C-O-
-CH2-Cl
H-C=C-
Арил-СН2-N=
-NH-CO
Ph-H
-COOH
Электронодонорные заместители действуют противоположным образом. В первом приближении, чем более кислым является протон, тем больше его химический сдвиг. Однако протоны в некоторых соединениях, например бензоле, дают сигнал в более слабом поле, чем можно было бы ожидать, исходя из электроотрицательности sр2 гибридизованного атома углерода. Такое сильное дезэкранирование объясняется возникновением «кольцевого тока» за счет циркуляции электронов бензольного кольца под влиянием внешнего магнитного поля. Кольцевой ток индуцирует магнитное поле, которое совпадает с направлением внешнего магнитного поля в области нахождения протонов и дезэкранирует их. Величины химических сдвигов ароматических протонов используются в качестве экспериментального критерия ароматичности.
В ЯМР 1Н-спектре этанола (см. рис. 28) протоны метиленовой и гидроксильной групп вследствие различного окружения имеют отличающиеся резонансные сигналы, наблюдаемые при разных напряженностях поля. Сравнение интенсивности сигналов, определяемых по высоте ступенек интегральной кривой (пунктирная линия), позволяет определить соотношение числа эквивалентных протонов в отдельных группировках. Таким образом, по величине химических сдвигов и суммарной интенсивности резонансных сигналов можно сделать начальные выводы о структуре исследуемого соединения.
Как видно из рисунка 28, протоны одного типа – метильные или метиленовые – проявляются не в виде единичного резонансного сигнала, а расщепляются на ряд линии. Это явление, называемое спин-спиновым
54

взаимодействием, возникает в результате влияния соседних протонов друг на друга через две (Н-С-Н) или три ковалентные связи (Н-С-С-Н). Магнитное поле, наведённое одним протоном, изменяет магнитное поле вокруг второго протона, приводя к расщеплению его сигнала. Мерой спин-спинового взаимодействия служит константа спин-спинового взаимодействия J, которая характеризует расстояние между расщепленными линиями.
Таблица 6
13С химические сдвиги, δ, м.д.
Относительно ТМС |
220 |
200 |
180 |
160 |
140 |
120 |
100 |
80 |
60 |
40 |
20 |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
H3C-C-первичн |
|
|
|
|
|
|
|
|
|
|
|
|
H3C-S- |
|
|
|
|
|
|
|
|
|
|
|
|
H3C-N- |
|
|
|
|
|
|
|
|
|
|
|
|
H3C-O- |
|
|
|
|
|
|
|
|
|
|
|
|
-H2C-C-вторичн |
|
|
|
|
|
|
|
|
|
|
|
|
Циклопропаны |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
-H2C-S- |
|
|
|
|
|
|
|
|
|
|
|
|
-H2C-N- |
|
|
|
|
|
|
|
|
|
|
|
|
-H2C-O- |
|
|
|
|
|
|
|
|
|
|
|
|
-H2C-галогены |
|
|
|
|
|
|
|
F |
Cl |
Br |
I |
|
=СН-С-третичн |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=СН-S- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=СН-N- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
=СН-галоген |
|
|
|
|
|
|
F |
Cl |
Br |
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С-С четвертичн |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С-S- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С-N- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С-O- |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С-галоген- |
|
|
|
|
|
|
|
Cl |
Br |
I |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Алкины |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
С=С=С аллены |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
55