Материал: Синтез каталитически активных полимер-стабилизированных наночастиц палладия
Большинство исследований посвящено формированию наночастиц в мицеллах амфифильных блок-сополимеров с функциональным ядром в органической среде, тогда как выбор блок-сополимеров в водной среде очень ограничен, и формирование частиц металла обычно усложнено. Несколько примеров таких блок-сополимеров включают П2ВП-6-ПЭО и ПБ-б-ПЭО [57]. Кроме того, необходимо принимать во внимание рН-среды [58], например, при рН ниже 5 П2ВП-6-ПЭО становится молекулярно растворим в воде. В случае ПБ-б-ПЭО, мицеллы, образующиеся в воде, очень плотные, поэтому они успешно выполняют две роли: служат в качестве нанореакторов для формирования наночастиц Pd, Pt, Rh и как содержащие металлические частицы подложки для блочной полимеризации мезопористой окиси кремния [40].
Важным свойством амфифильных блок-сополимеров является их способность к микросегрегированию в связи с несовместимостью блоков [46].
Морфологическую стабильность наблюдали для высокоассиметричных диблочных мономеров, в которых более короткий блок (ПАК) образует сферические микродомены внутри матрицы основного компонента - ПС [59]. При этом было обнаружено, что ни введение ионов кадмия, ни формирование наночасиц CdS не изменяют морфологию блок- сополимера.
Для диблочного сополимера на основе изопрена и 2-винилпирролидона (2ВП) было показано [60], что при низком содержании наночасиц палладия'сохраняется ламелярная структура блок-сополимера, тогда как при увеличении- содержания палладия, упорядоченная (регулярная) структура нарушается. Таким образом, рост наночастиц влияет на структуру блок-сополимера.
Однако прослеживается и обратная связь: межфазные поверхности пленок влияют на образование наночастиц внутри микрофазы блок-сополимера. Рост наночастиц серебра [61], палладия [60, 62] и других металлов внутри микросегрегированных слоев ограничен толщинами этих слоев. Проникновения зародышей- металлов и растущих частиц в соседние неполярные слои практически не наблюдалось, то есть блок-сополимерный домен играет роль нанореактора при формировании наночастиц металлов. Наилучшая' упорядоченность в расположении наночастиц в многослойных блок-сополимерных пленках наблюдалось в том случае, если пленки были получены в неравновесных условиях, обеспечивающих формирование сильно »асимметричных наноразмерных частиц [63].
Интересным свойством ПЭ является их способность формировать тонкие пленки на различного рода инертных материалах. С недавнего времени многие статьи посвящаются объединению неорганических материалов и супрамолекулярных органических структур с целью создания новых гибридных материалов для последующего применения в различных областях, в том числе и в качестве стабилизаторов наночастиц металлов [64 - 66].
ПЭ способны формировать на поверхности различных носителей как моно-, так и полислоевые покрытия. Такие ультратонкие слои могут рассматриваться как наноразмерные реакторы, в которых рост наночастиц металлов ограничивается толщиной слоя. Однако, необходимо отметить, что в этом случае поверхность твердого носителя (например, Al2O3, SiO2) должна нести определенный заряд. Так при однократном нанесении катионного ПЭ (ПДАДМАХ или хитозана) необходимо наличие отрицательного заряда на поверхности окиси алюминия, для получения которого исходная окись алюминия обрабатывается водным раствором щелочи. Такая обработка приводит к перезарядке поверхности (перемене знака электрокинетического потенциала), что значительно улучшает электростатическое взаимодействие с катионным ПЭ. Ионы металла включаются в пленку ПЭ и затем восстанавливаются, формируя наночастицы (Рис. 9, верх). Но описанный метод однократного нанесения имеет ряд недостатков, главным из которых является недостаточно прочное закрепление ПЭ на поверхности носителя, в результате чего в процессе использования такого наноструктурированного материала, часть ПЭ слоя может смываться, а система - терять свои первоначальные свойства.
Адсорбция противоположно заряженного ПЭ (например,
сильного анионита при нанесении катионного ПЭ) в качестве первого слоя
позволяет создать благоприятные условия для последующего нанесения (Рис. 9,
низ). Это так называемое нанесение "слой за слоем", которое включает
последовательную адсорбцию поликатионов и полианионов. Данная техника позволяет
наносить пленку практически на любую поверхность, поэтому она даст возможность
формировать полимер-содержащие системы на субстратах с высокой площадью
поверхности, таких как оксид алюминия [66, 67].
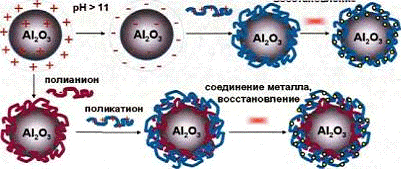
Рисунок 9.
Схема синтеза катализатора методом однократного нанесения поликатиона и
нанесения «слой за слоем»
Некоторые авторы использовали технику нанесения «слой за слоем» для создания тонких пленок коллоидного золота и показали, что имеет место сильное взаимодействие между наночастицами в смежных слоях. Нанесение изолирующих слоев ПЭ между слоями наночастиц золота позволяет регулировать взаимодействие между слоями. Такие изолирующие слои могут быть различными, начиная от тиола [68], полимеров [69, 70] и заканчивая большими макромолекулами, такими как ДНК [71].
В настоящее время наиболее, перспективными органическими носителями для синтеза наночастиц металлов контролируемого размера, их стабилизации и последующего применения в катализе являются сверхсшитые полимерные материалы. Такие материалы способны контролировать процессы нуклеации и роста частиц за счет наличия наноразмерных пустот высокой степени монодисперсности [38,40].
Жесткие сверхсшитые полимеры обладают весьма большой внутренней поверхностью, обычно около 1000 м2/г, а также способностью к набуханию в любой жидкой среде, в том числе и в осадителях для исходного полимера. Для получения сверхсшитой сетки необходимо выполнение двух основных условий: Во-первых, полимер должен быть получен в присутствии хорошего растворителя для предотвращения фазового расслоения и формирования открытой сетчатой» микроструктуры. Во-вторых, конечная полимерная сетка должна быть конформационно-жесткой, для предотвращения ее коллапса при удалении-растворителя.
Особое внимание исследователи уделяют сверхсшитому полистиролу (СПС). Это уникальная-полимерная сеть, в которой поры формируются спонтанно в ходе синтеза полимера. В связи с его высокой степенью сверхсшивки, которая может превышать 100%, СПС состоит из наноразмерных жестких пустот размером порядка 2-3 нм. Его получают путем химического включения метиленовых групп между соседними фенильными кольцами в растворенном гомополимере ПС или гелеобразном поли(стирол-и- дивинилбензол)-сополимере в присутствии дихлорэтилена (Рис. 10).
Для СПС вводится расчетная характеристика степени сшивки - Z. Это мольная доля (%) мостиков (структурных элементов сетки с двумя узлами) в общем количестве структурных элементов сетки (мостиков и фрагментов с незамещенными фенильными кольцами). Например, при введении 1 моля бифункционального сшивающего агента на 1 осново-моль ПС каждое звено формально оказывается.вовлеченным в образование двух мостиков, и расчетная величина сшивки Z=200 %. При этом, с увеличением Z, образуется полимерная структура с аномально низкой плотностью упаковки, то есть свободный объем составляет большую часть объема СПС (60 - 70 % для ПС, сшитого более чем на 100%) [88].
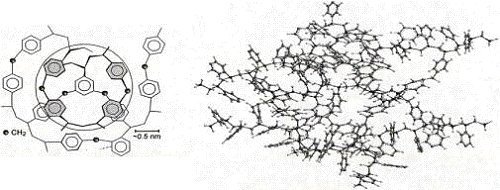
Рисунок 10.
Схематическое изображение внутренней структуры СПС (окружностью обозначена
отдельная пора сверхсшитой сетки) (а) и объемная модель участка СПС,
образованного при сшивании трех цепей ПС -СН2-мостиками (Z
= 100 %) (б)
Уникальным свойством СПС является его способность к набуханию в различных растворителях, даже в термодинамически неустойчивых (например, в воде) [40, 89]. Такая всесторонность способствует включению различных органометаллических соединений в наноструктурированную матрицу СПС [89].
Наличие нанопор или нанопустот стандартного размера и формы в полимерной матрице создает поверхности раздела между объемом пор и стенками полимера - наноструктуры, которые могут служить нанореакторами для роста частиц. В этом случае размер частиц может ограничиваться размером пор [40]. На рисунке 11 показана схема формирования наночастиц металлов в пустотах (порах) сверхсшитой полимерной матрицы СПС.
О первом использовании СПС в качестве среды для
формирования наночастиц металлов сообщалось в 1999 [82]. Авторы работы [80]
исследовали формирование наночастиц кобальта в порах СПС. Средний диаметр
частиц составлял 2,1 ± 1,0 и 2,6 ± 1,6 нм для образцов с содержанием кобальта
5,07 и 10,08 (масс.) % соответственно. В относительно широком интервале
концентраций кобальта (от 0,9 до 8,0 (масс.) %) именно наноразмерные пустоты в
СПС отвечали за контролируемое формирование наночастиц этого металла. При
содержании кобальта сверх некоторого предельного значения (>8 (масс.) %)
начинался рост крупных частиц. Наиболее вероятной причиной контролируемого
роста частиц в матрице СПС является неспецифическое взаимодействие фенильных
колец поверхностью металла, что должно приводить к стерической стабилизации
наночастиц кобальта [38].
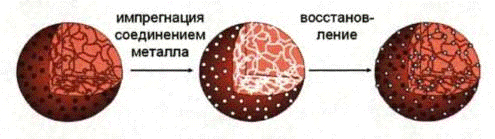
Рисунок 11.
Схема синтеза наночастиц в пустотах (норах) СПС
В работе [55] изучалось формирование наночастиц платины в порах СПС. Средний размер частиц составлял 1,3 ± 0.3 нм. Такое расхождение с размерами частиц кобальта, можно объяснить разными механизмами формирования наночастиц этих металлов. При 200°С кластеры кобальта способны легко мигрировать в поры СПС, формируя частицы, соответствующие размеру пор. В случае же платины восстановление водородом происходило при комнатной температуре, при которой миграция атомов или кластеров платины или молекул исходного соединения металла не происходит, поэтому размер частиц пропорционально количеству ионов соли металла, наполняющего поры.
Таким образом, при формировании наночастиц кобальта матрица СПС контролирует размеры металлических наночастиц непосредственно - путем физического ограничения их размера размером пор (2 нм), В случае же наночастиц платины поры ограничивают количество исходного соединения металла, заполняющего отдельную пору при восстановлении его объем уменьшается (увеличивается плотность частицы) до объема частицы [88].
В соответствии с мультиплетной теорией A.A. Баландина [56] максимум каталитической активности в реакции гидрирования С=С связи приходится на палладий и другие переходные металлы платиновой группы из-за оптимального межатомного расстояния для активации водорода и ацетиленовой связи.
Между металлами существуют различия по значениям селективности и скорости гидрирования тройной связи до двойной. Известно [80, 82], что более сильная, связь металл - водород ингибирует дальнейшее гидрирование алкена до алкана. По значениям энергии связи металл - адсорбированный атомарный водород переходные металлы располагаются в ряду W > Pd > Fe > Ni > Rh > Pt.
Кроме того, чем выше свободная энергия поверхности металла, тем больше величина энергии связи Ме-Н и Ме-органическое соединение и адсорбционная способность металла. Свободная энергия, поверхности связана с теплотой сублимации металла-катализатора. В каждом ряду периодической» системы теплота сублимации снижается с увеличением порядкового номера и в этом же ряду растет теплота адсорбции водорода, то есть от железа к никелю, от рутения к палладию и от осмия к платине. Низкая теплота сублимации палладия по сравнению с другими металлами платиновой группы определяет его способность поглощать большие объемы водорода, что приводит к изменению параметров решетки с 3,885 до 4,01 Ä в зависимости от количества растворенного водорода. При большой энергии связи атомов металла в кристаллической решетке растворение водорода потребовало бы затраты колоссальной энергии на ее расширение [77]. Высокая селективность гидрирования ацетиленовой связи до двойной на палладии связана с тем, что реакция вдет в основном за счет растворенного водорода, энергетически пригодного для гидрирования тройной связи [77]. Для палладия теплота растворения водорода в объеме составляет 42 ± 2 кДж/моль, то есть на палладии хемосорбируется наиболее однородный водород [75].
Основными активными формами адсорбированного водорода являются атомы в линейной и мостиковой связи с поверхностью. В образовании полу гидрированной формы участвует атомарно-адсорбированный водород, который на поверхности образует диполь, обращенный положительным концом в газовую фазу или раствор. Дипольный характер адсорбции приводит к образованию протона, который с молекулами воды образует ион гидроксония и при подходящих условиях может проникать внутрь решетки, образуя там гидридные фазы. Десорбция растворенного в палладии водорода происходит при низких температурах (20°С) [76].
При взаимодействии адсорбированного водорода с наиболее: энергетически ненасыщенными атомами металлов происходит наиболее прочная. многоцентровая адсорбция атома водорода, который при этом располагается между двумя атомами не над поверхностью металла, а под. ней (в приповерхностных слоях) с образованием отрицательно заряженной частицы. Это так называемая мостиковая структура адсорбированного атома водорода, роль которого проявляется при восстановлении соединений с высоким окислительно-восстановительным потенциалом [76].
Специфическая адсорбция ионов изменяет строение, емкость и состав-двойного электрического слоя, что оказывает весьма существенное: влияние на поведение системы Рd-Н. Специфическая адсорбция; катионов на поверхности палладия тормозит процесс диффузии растворенного водорода, и снижает количество адсорбированного.Такое изменение состояния системы Рd-Н в растворах катионов. повышает избирательность процесса гидрирования. В первую очередь гидрированию подвергается органическое соединение, обладающее максимальной адсорбционной способностью. Вещества с низкой адсорбционной способностью не способны преодолеть энергетический барьер, необходимый для протекания фазового β→α-перехода с достаточной скоростью. В этом случае процесс гидрирования или не идет, или протекает с очень маленькой скоростью. Скорость фазового перехода можно варьировать в широких пределах путем модифицирования поверхности палладия различными количествами катиона.
Несмотря на то, что в гетерогенном катализе все события происходят па поверхности каталитически активного центра, ключевую роль может играть прилегающий к поверхности участок. Атомы углерода могут растворяться в металлической частице и изменять электронную структуру поверхности [40, 45], причем Рd-С стабилен только в условиях реакции [42]. Было также обнаружено, что состояние палладия сильно зависит от температуры, когда концентрация водорода в газовой фазе близка к пределу фазового перехода Рd в β-гидрид Рd. Рd-С появляется в заметном количестве при температуре превышающей температуру разложения [β -гидрида [45].
Так как только атомы, а не молекулы, могут проникать в кристаллическую решетку металла, было сделано предположение, что молекулы многих алкинов распадаются в начале реакции [22]. Данное предположение согласуется с исследованиями, показывающими обратимое потребление углерода в начале любой селективной реакции гидрирования алкинов [105], а также с наличием в таких системах индукционного периода. Наличие углерода в приповерхностных слоях палладия наблюдали с использованием сканирующей туннельной микроскопии. Было показано, что углерод занимает октаэдральные приповерхностные участки [29],
В то же время от присутствия углерода сильно зависит тип водорода, участвующего в гидрировании. Включение углерода в приповерхностные слои палладия нарушает равновесие между адсорбированным и растворенным водородом и препятствует участию растворенного водорода в каталитическом процессе, повышая селективность последнего [54].
Катализаторы на основе наночастиц металлов, стабилизированных в ультратонких слоях ПЭ, нанесенных на инертную подложку, также достаточно распространены. Ионы и комплексы переходных металлов, иммобилизованные в ПЭ слоях, являются многообещающими катализаторами из-за благоприятного сочетания свойств гетерогенных и гомогенных систем. В работе [67] исследовалась импрегнация наночастиц палладия в полимерную матрицу, состоящую из чередующихся слоев ПАК и ПЭИ, нанесенных на окись алюминия. Эти катализаторы исследовались на примере реакции гидрирования алифатических спиртов. Важно отметить, что активность такого катализатора уменьшалась с возрастанием числа бислоев полимеров. Это связано, по всей видимости, с зависимостью доступности каталитически-активных центров для реагирующих молекул от числа слоев полимерной матрицы.