Материал: Синтез каталитически активных полимер-стабилизированных наночастиц палладия
- способности масштабировать синтез и сборку для дешевого, крупномасштабного производства нанострктурированных материалов, удерживая в то же время контроль над размером и качеством поверхностей раздела [5].
В нанометровом диапазоне взаимодействие частица-частица может быть обусловлено слабыми Ван-дер-Ваальсовыми силами, более сильными полярными и электростатическими или ковалентными взаимодействиями в зависимости от вязкости и полярности растворителя. Путем модификации поверхностного слоя частицы тенденция к коагуляции может быть усилена или ослаблена [2].
Существует три типа стабилизации синтезированных наночастиц [7]:
) электростатическая стабилизация. Анионы и катионы исходного вещества остаются в растворе и ассоциируют с наночастицами. Частицы окружает двойной электрический слой, что приводит к электростатическому отталкиванию и препятствует агрегации;
) стеричёская стабилизация. Агрегация предотвращается посредством адсорбции больших молекул (полимеров или поверхностно активных веществ (ПАВ));
) электростерическая, стабилизация.
На рисунке 2 схематично представлена зависимость
потенциальной энергии от расстояния между частицами для различных способов
стабилизации [30].
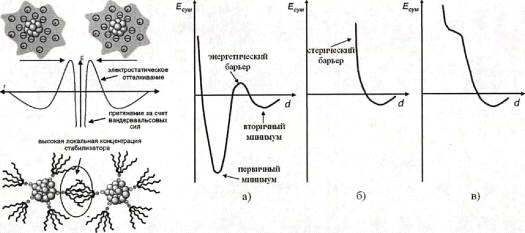
Рисунок 2. Зависимость потенциальной энергии от расстояния между частицами для различных способов стабилизации: электростатического (а), стерического (б) и электростерического (в)
В случае электростатической стабилизации (Рис. 2 (а)) реализуется теория взаимодействия двойных электрических слоев (ДЛФО), основанная на модели Гуи-Чепмена и числовом решении уравнения Пуассона-Вольцмана для сферических частиц [31]. Характерной чертой является наличие глубокого первичного минимума и плоского вторичного минимума, разделенных энергетическим барьером. Если барьер достаточно велик, то частицы находятся в первичном минимуме в метастабильном состоянии [30, 31].
Стерическая стабилизация (Рис. 2 (б)) возможна за счет наличия адсорбционного слоя полимера. Молекулы, адсорбированные на поверхности, ограничивают движение в пространстве между частицами, что приводит к уменьшению энтропии и увеличению свободной энергии частиц. Одновременно из-за локального увеличения концентрации адсорбированных молекул происходит их взаимопроникновение, приводящее к возникновению осмотического отталкивания; растворитель восстанавливает равновесие посредством разбавления полимерных молекул и разделения частиц. Положение плоского энергетического минимума обусловлено толщиной адсорбционного слоя, который в свою очередь связан с молекулярной массой полимера [30]. Необходимо отметить, что полимеры способны стабилизировать наночастицы не только за счет стерического эффекта, а также связываясь слабо с поверхностью частиц посредством гетероатомов, играющих роль лигандов [32],
Если же адсорбирующийся полимер является полиэлектролитом (ПЭ), реализуется электростерическая стабилизация (Рис. 2 (в)) [30].
В работах [33, 34] было показано, что адсорбция органических соединений на наночастицах сопровождается формированием органической оболочки на неорганическом ядре и приводит к резкому (более чем на порядок) снижению межфазного поверхностного натяжения, стабилизации образующихся наночастиц от их агрегации, торможению роста частиц, а также резкому повышению их устойчивости к воздействию окружающей среды. Отмечалось, что образующиеся наночастицы обладают узким распределением по размерам, а средний размер частиц существенно меньше (для благородных металлов это обычно 1-6 нм). Было также показано, что радиус критического зародыша новой фазы в растворе в зависимости от интенсивности адсорбции органических соединений на образующуюся наночастицу может приводить к резкому уменьшению этой величины вплоть до размеров, соизмеримых с размерами атомных кластеров. В интервале 0,5 < r < 10 нм, где проявляется влияние кривизны поверхности растущей частицы, ее равновесный радиус заметно уменьшается из-за возникновения межфазного поверхностного слоя [33]. Если радиус частицы мал (r < 0,5 нм), то превалирующими будут флуктуации поверхностного натяжения, то есть само понятие поверхностного натяжения становится принципиально неприемлемым [35]. Более того, было обнаружено, что процесс нуклеации из жидкой фазы не может быть описан в рамках одностадийного (однобарьерного) классического подхода (п. 1.1.1) и требует учета реальной структуры жидкой фазы, промежуточных метастабильных аморфных «до зародышей» и различных модификаций кристаллических зародышей [36, 37].
Существуют различные подходы к использованию полимеров в качестве носителей и стабилизаторов наночастиц металлов [38 - 40]. Однако наиболее часто используются два типа полимеров: ПЭ, комбинирующие стерический и электростатический эффекты стабилизации, и твердые наноструктурированные полимерные матрицы, способные контролировать размер образующихся наночастиц за счет наличия наноразмерных пустот (пор) и удобные в практическом применении. Эти два класса полимеров будут рассмотрены более подробно.
ПЭ называют органические высокомолекулярные соединения, макромолекулы которых содержат ионогенные группы способные к диссоциации и обмену подвижных ионов на ионы других соединении в растворе.
По характеру ионогенных групп с одной стороны ПЭ делятся на поликислоты (содержат -SО3Н, -СООН, -РО(ОН)2, -ОН, -SН и другие группы), полиоснования (содержат -NH2, -NHR, -NR1R2, -N+R1R2R3 и др.) и полиамфолиты, в состав которых входят одновременно кислотные и основные группы [41], а с другой - на слабые и сильные ПЭ.
В зависимости от происхождения ПЭ подразделяют
на природные (ДНК, РНК, аминополдисахариды) (Рис. 3), модифицированные
природные (производные целлюлозы и хитина) и синтетические (Рис. 4) [30].
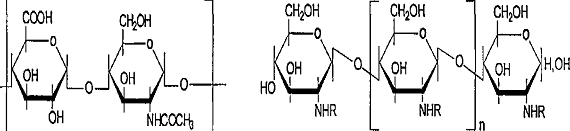
Рисунок 3. Примеры
природных ПЭ
Среди синтетических ПЭ можно выделить следующие:
- поликислоты: полистиролсульфокислота (ПСС) и поливинилсульфоновая кислота (ПВС). К слабым поликислотам относятся полиакриловая (ПАК) и полиметакриловая (ПМАК) кислоты (Рис. 4 (а));
- полиоснования: полиэтиленимин (ПЭИ), поли-2-винилпиридин (П2ВП), поли-4-винилпиридин (П4ВП), полидиаллилдиметилхлорид аммония (ПДАДМАХ), поли-2-метил-5-винилпиридин (П2М5ВП), поливинил-N-бутилпиридиний бромид (ПВБПБ), полиаминостирол (ПАС) (Рис. 4 (б)). Сильные полиоснования содержат группы четвертичных замещенных аммония -N+R1R2R3, слабые -NHR, -NR1R2, -NH2 - группы.
Растворы ПЭ - сложные системы, характеризующиеся
различными ионными и неионными взаимодействиями. Проблемы физикохимии растворов
ПЭ имеют, по крайней мере, два аспекта - полимерный (конформационный) и
электрохимический. В случае ПЭ появляется целый ряд дополнительных факторов
(диссоциация, специфическое и неспецифическое связывание ионов,
электростатические и гидрофобные взаимодействия).
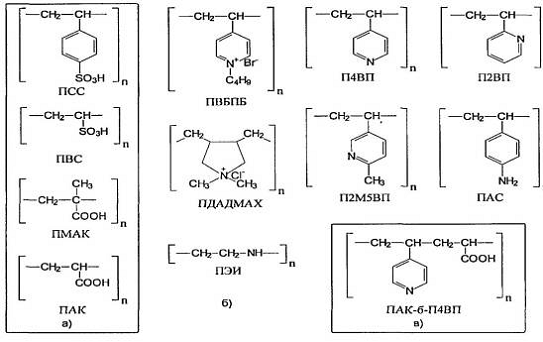
Рисунок 4.
Примеры синтетических ПЭ: полианионы (а), поликатионы (б),
полиамфолит
(в)
Благодаря наличию в макромолекуле ПЭ ионогенных групп при растворении его в ионизирующем растворителе происходит электролитическая диссоциация с образованием высокомолекулярного полииона и низкомолекулярного противоиона (Рис. 5) [30].
Одним из наиболее интересных свойств ПЭ с
высокой плотностью заряда является их склонность к образованию комплексов с
противоположно заряженными крупными молекулами (ПЭ, в частности).
Полиэлектролитные
комплексы (ПЭК), или симплексы, позволяют комбинировать физико-химические
свойства, по крайней мере, двух ПЭ. Движущей силой образования ПЭК являются
сильные электростатические взаимодействия между противоположно заряженными ПЭ,
приводящие к внутриполимерной ионной конденсации. В формирование ПЭК также
принимают участие внутренние макромолекулярные взаимодействия
такие, как водородные связи, Ван-дер-Ваальсовы силы, гидрофобные и
диполь-дипольные взаимодействия.
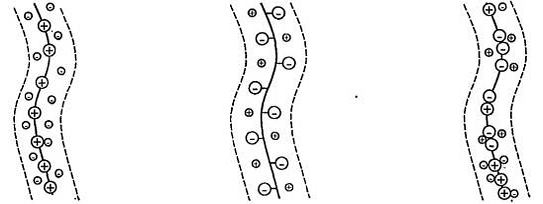
Рисунок 5.
Заряженные ПЭ в растворе
Процесс комплексообразования самопроизволен, так как приводит к возрастанию энтропии в результате освобождения противоионов. При длине полимера не превышающей шесть мономеров константа комплексообразования, возрастает экспоненциально. Выше этой критической длины цепи полимера какого-либо заметного влияния молярной массы на константу комплексообразования обнаружено не было.
Комплексы, синтетических ПЭ (поли(4-винилбензилтриметилхлорида аммония) с ПСС) были впервые исследованы в 1961 г. Михаэлисом [42]. Здесь необходимо различать ПЭ интегрального и «подвесного» типа (Рис. 5). Для ПЭ «подвесного» типа, у которых заряды несут боковые группы, было обнаружено, что если хотя бы одна ионная связь сформировалась, соседние реакционные группы взаимодействуют с близко расположенными комплементарными участками, и образуется равновесная солевая структура.
Исходя из общих свойств ПЭ возможно образование ПЭК двух основных типов: стехиометрического и нестехиометрического. Если ПЭ со слабыми ионогенными группами и большой разницей в молярных массах смешиваются в нестехиометрическом соотношении (относительно катионных и анионных групп), то могут образовываться водорастворимые ПЭК. Такие структуры состоят из длинноцепочечных молекул-хозяев, связанных с более короткими «гостевыми» молекулами (Рис. 6 (в)) [43]. Особенностью таких ПЭК является то, что молекула-гость может перемещаться вдоль молекулы-хозяина. При этом растворимость в воде зависит от соотношения между обоими типами ПЭ.
Если смешиваются ПЭ с сильными ионогенными
группами и сопоставимыми молярными массами, то имеет место стехиометрическое
соотношение 1:1, и образующиеся агрегаты могут быть описаны двумя моделями:
лестничная структура с фиксированной ионной сшивкой (Рис. 6
(а)); более хаотичная структура «клубок» со статистической компенсацией зарядов
(Рис. 6 (б)).
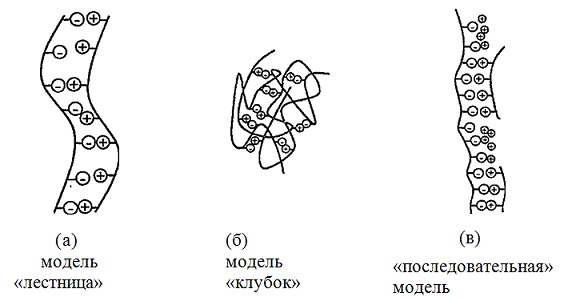
Рисунок 6.
Модели ПЭК для более (а) или менее (б) упорядоченных стехиометрических
комплексов (согласно Михаэлису) в сравнении с нестехиометрическими комплексами
(в) (согласно Кабанову)
Образование более упорядоченных структур главным образом зависит от степени соответствия пространственного расположения заряженных центров обоих компонентов равно, как и от условия формирования ПЭК.
Поведение ПЭ в растворах определяется взаимодействием заряженных участков полиионов друг с другом и окружающими их противоионами. Одной из особенностей ПЭ является «полиэлектролитное набухание», заключающееся в разворачивании клубков макромолекул и увеличения их линейных размеров в результате электростатического отталкивания одноименно заряженных звеньев макромолекулы. В случае достаточно большой концентрации электрических зарядов на полимерной цепи жесткость последней может оказаться настолько большой, что станут невозможными свернутые конформации, и макромолекула будет принимать стержнеобразную форму [44].
Полиэлектролитное набухание подавляется
добавлением в раствор сильного низкомолекулярного электролита или поддержанием
постоянной ионной силы раствора (изоионное разбавление). При этом происходит
экранирование зарядов полииона, уменьшение занимаемого им объема, в результате
ПЭ в растворе ведет себя как незаряженный полимер (Рис. 7)
[30].
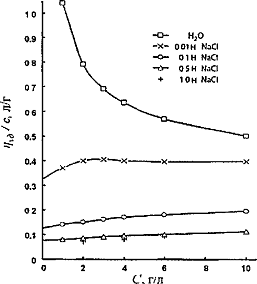
Рисунок 7.
Зависимость раствора ПЭ (сополимера малеиновой кислоты и ПДАДМАХ) от
концентрации полимера и добавленного NaCl
[30]
Аналогичная картина наблюдается в растворителях
с низкой диэлектрической проницаемостью, в которых диссоциация ПЭ подавлена;
Данные по вязкости водных растворов ПЭ могут быть описаны эмпирическим
уравнением Фуосса (1):
ηуд/с
=
А/(1 + В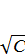
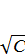 ) (1)
) (1)
где А определяет предельную длину, которой может достичь полимерный клубок в результате электростатического отталкивания;
В характеризует электростатическое взаимодействие с растворителем [44]:
Важной особенностью амфифильных ПЭ (Рис. 4 (в)), построенных из нескольких (чаще двух) блоков с различным химическим строением, является то, что такие блок-сополимеры способны к микросегрегации на фазы в твердом состоянии и образуют мицеллы в разбавленных растворах в селективных растворителях (хороший растворитель только для одного блока); При этом размер и форма мицелл зависит от химической структуры блока; молекулярного веса каждого блока и типа растворителя (гидрофильного или гидрофобного) [40, 46, 47].
ПЭ, используемый для стабилизации наночастиц металлов, должен удовлетворять следующим требованиям:
- растворяться в различных растворителях;
- быть термически стабильным в ходе приготовления каталитической системы и ее применения;
- хорошо взаимодействовать с поверхностью металла;
- хорошо
взаимодействовать с исходным соединением металла [30];
1.4 Стабилизация наночастиц в мицеллах
амфифильных блок-сополимеров
В случае использования в качестве, стабилизатора амфифильных блок-сополимеров в процессе синтеза наночастиц необходимо, чтобы один из блоков ди- или триблочного сополимера содержал функциональные группы, способные: взаимодействовать, с соединениями металлов. Если в ядро мицеллы-входит блок, который содержит группы, способные реагировать с соединениями металлов с образованием комплекса или соли, то это ядро может быть наполнено соответствующим металлом, входящим в состав комплекса или соли, и в дальнейшем использоваться как нанореактор для формирования наночастиц металлов.
Наиболее часто в качестве таких блоков используются, поли (2- или 4)винилпиридины (П4(2)ВП), так как ПВП не токсичен и растворяется во многих полярных растворителях [48 - 53]. Также можно использовать ПМАК или ПАК, полибутадиен (ПБ), ПЭИ и некоторые другие соединения [40].
Корона мицеллы должна быть образована блоком, не содержащим функциональных групп, но обеспечивающим растворимость и стабильность мицелл в соответствующем растворителе. Такие блоки могут состоять из полистирола (ПС), полиэтиленоксида (ПЭО), полиизобутилена (ПИБ) и других полимеров.
На рисунке 8 показана типичная схема формирования
наночастиц металлов в ядрах мицелл амфифильных блок-сополимеров.
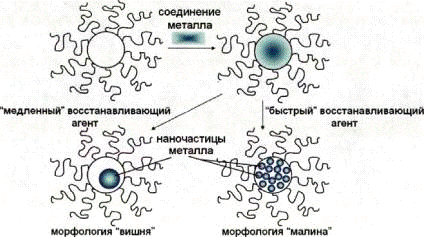
Рисунок 8. Схема формирования наночастиц металлов в мицеллах амфифильных блок-сополимеров
Восстановление солей металлов в присутствии стабилизатора путем введения восстанавливающего агента является классической методикой получения коллоидов металлов. Для этого могут быть использованы различные восстановители в зависимости от типа металла [54]. Формирование частиц Аu, Рd, Рt и других в блок-сополимерных мицеллах, полученных от блок-сополимеров ПС-6-П4ВП, показало, что морфология наночастиц сильно зависит от типа восстанавливающего агента. При использовании медленного восстанавливающего агента (например, гидразина), может быть сформирована одна наночастица на мицеллу (морфологи "вишня"), если нет обмена между мицеллами [55]. Быстрое восстановление (например, NaBH4) приводит к образованию множества маленьких частиц в мицелле (морфология "малина"), что предпочтительно для каталитического использования (Рис. 8) [40].
Использование ядер блок-сополимерных мицелл в качестве нанореакторов позволяет синтезировать моно и биметаллические наночастицы; при этом морфология биметаллических частиц зависит от конкретной пары металлов [53].
Наночастицы могут формироваться не во всем ядре, а только во внешнем слое, если использовать триблок-сополимер, в котором только центральный блок обладает способностью координироваться*с соединениями металлов, и кроме того, центральный и один из концевых блоков не должны растворяться в реакционной среде. Такие системы могут представлять особый интерес для использования в катализе, так как наночастицы, находящиеся во внешней сфере ядра, более доступны для субстрата [38]. Типичным примером синтеза наночастиц металла в блок-сополимерах, содержащих комплексы или наночастицы в отдельно выбранном блоке, является введение групп Fe(CO)3 в ПБ-блок триблок-сополимера ПС-б-ПБ-б-ПС посредством комплексообразования [56].