Материал: Синтез каталитически активных полимер-стабилизированных наночастиц палладия
Синтез каталитически активных полимер-стабилизированных наночастиц палладия
СОКРАЩЕНИЯ И ОБОЗНАЧЕНИЯ
ПАВ - поверхностно-активное вещество
ПЭ - полиэлектролит
ПСС - полистиросульфокислота
ЛВС - поливинилсульфоновая кислота
ПАК - полиакриловая кислота
ПМАК- полиметакриловая кислота
ПЭИ - полиэитленимин
П2ВП - поли-2-винилпиридин
П4ВП - поли-4-винилпиридин
ПДАДМАХ - полидиаллилдиметилхлорид аммония
П2М5ВП - поли-2-метил-5-винилпиридин
ПВБПБ - поливинил-N-бутилпиридиний бромид
ПАС - полиаминостирол
ПЭК - полиэлектролитные комплексы
ПБ - полибутадиен
ПС - полистирол
ПЭО - полиэтиленоксид
ПИБ - полиизобутилен
ВП - 2-винилпирролидон
СПС - сверхсшитый полистирол
ПОДС - полиоктадецилсилоксан
ДГЛ - дегидролиналоол
ЛН - линалоол
ИФ - изофитол
ДиГЛ - дигилролиналоол
ДМЭК - диметилэтинилкарбинол
ДГИФ - дегидроизофитол
ГЛ - D-глюкоза
ГЛК - D-глюконовая кислота
АХ - Аl2Оз и хитозан
ПЕХ - ПСС и хитозан
ПИД - пламенно-ионизационный детектор
РФА - рентгенфлуоресцентный анализ
РФЭС - рентгенофотоэлектронная спектроскопия
СЭМ - сканирующая электронная микроскопия
СЗС- санитарно-защитная зона
БАС- биологически активное соединение
СОДЕРЖАНИЕ
палладий наночастица катализатор
ВВЕДЕНИЕ
ЛИТЕРАТУРНЫЙ ОБЗОР
.1 Способы синтеза наночастиц металлов
.2 Основные закономерности формирования нанофазы в растворе
1.3 Стабилизация наночастиц металлов
1.4 Стабилизация наночастиц в мицеллах амфифильных блок-сополимеров
2 Экспериментальная часть
2.1 Методика приготовления катализаторов. Методика приготовления наночастиц Палладия, стабилизированных в ультратонких слоях хитозана, нанесенных на окись алюминия
.2 Оборудование и методики проведения экспериментов
2.3 Методика гидрирования
.4 Физико-химические методы исследования катализаторов
2.5 Хемосорбция СО
2.6 Определение содержаний металлов методом рентгенфлуоресцентного анализа
2.7 Использованные реактивы
3 РЕЗУЛЬТАТЫ И ИХ ОБСУЖДЕНИЕ
3.1 Физико-химические свойства нанокомпозитов на основе наночастиц палладия, стабилизированных в ультратонких слоях хитозана, нанесенных на инертную подложку
3.2 Рентгенфлуоресцентное исследование образцов
3.3 Каталитические свойства ианочастиц палладия, стабилизированных в ультратонких слоях хитозана
4 ОХРАНА ОКРУЖАЮЩЕЙ СРЕДЫ
.1 Воздействие вредных источников на атмосферу
4.2 Характеристика объекта как загрязнения атмосферы
4.3 Энергетическое воздействие объекта на окружающую среду
4.4 Воздействие вредных веществ на окружающую среду
4.5 Мероприятия по уменьшению негативного воздействия на атмосферный воздух
4.6 Установление границ санитарно-защитной зоны предприятия
ВЫВОДЫ
СПИСОК ИСПОЛЬЗОВАННЫХ ИСТОЧНИКОВ
ВВЕДЕНИЕ
Актуальность проблемы и общая характеристика работы. Ключевая роль катализатора - ускорение реакции с достижением высокой селективности и выхода целевого продукта. Наноразмерные частицы металлов характеризуются значительным количеством атомов с низким координационным числом на краевых и угловых участках, которые могут обеспечить наличие большого числа каталитически активных центров. Одной из проблем при создании и использовании таких материалов является стабилизация формы и размера наночастиц. Применение стабилизирующих агентов, наиболее перспективными среди которых в настоящее время: являются полимеры, позволяет успешно решать, данную проблему. Возрастающие потребности в продукции химико-фармацевтической и пищевой промышленности требуют создания новых путей получения» биологически активных соединений (БАС). В основе ряда существующих в настоящее время-синтезов лежат реакции селективного каталитического гидрирования; и окисления. Так, селективное каталитическое гидрирование ацетиленовых спиртов используется в производстве душистых веществ, БАС, лекарственных препаратов и витаминов А, Е и К. Реакции окисления моносахаридов, в частности, D-глюкозы (ГЛ), лежат в основе методов получения витамина В2, B15 и глюконата кальция: Применяемые традиционные катализаторы, хотя и обеспечивают необходимую селективность, но содержание активных металлов в них достаточно высоко. Кроме того, такие катализаторы зачастую требуют использования гомогенных модификаторов, что ухудшает качество целевого продукта. Вышеперечисленные обстоятельства определяют актуальность исследований, направленных на создание каталитических систем; на основе полимер - стабилизированных наночастиц металлов, исследование их физико-химических и каталитических свойств в реакциях селективного гидрирования и окисления, что ведет к совершенствованию технологии продуктов тонкого органического синтеза.
Целью работы является создание теоретических и экспериментальных основ синтеза каталитически активных полимер-стабилизированных наночастиц Pd использование, которых позволит достичь высокой эффективности проведения реакций селективного гидрирования тройной связи ацетиленового спирта - 3,7-диметилоктаен-6- ин-1-ола-З (ДГЛ), а также окисления карбонильной группы ГЛ.
Для достижения поставленной цели решались следующие задачи: теоретический анализ способов стабилизации наночастиц металлов; и обоснование выбора исходных компонентов катализаторов; синтез полимер-стабилизированных наночастиц Pd; физико- химическое исследование нанокомпозитов; изучение кинетических закономерностей гидрирования ДГЛ и окисления ГЛ на оптимальных катализаторах; выбор математических моделей и расчет кинетических параметров.
1.
ИТЕРАТУРНЫЙ ОБЗОР
1.1 Способы синтеза наночастиц металлов
Наночастицы обладают свойствами отличными от
свойств объемных материалов, так как число атомов или молекул на их поверхности
сравнимо с их числом внутри частиц. Например, нано
частица
диаметром 5 нм имеет около половины атомов на поверхности (таблица 1) [1].
Таблица 1
Соотношение между общим числом атомов в кластере и долей поверхностных атомов
|
Кластеры |
|
|
|
|
|
|
|
Общее число атомов |
13 |
55 |
147 |
309 |
561 |
1415 |
|
Поверхностные атомы, % |
92 |
76 |
63 |
52 |
45 |
35 |
Поэтому наночастицы можно использовать для создания материалов с уникальными свойствами. Отклонение поверхностных и межфазных свойств от свойств в объеме для большинства таких материалов может приводить к неожиданным поверхностным эффектам, включающим каталитическую активность [2 - 4].
Причина состоит в том, что материалы могут проявлять фундаментально новое поведение, когда их размер уменьшается ниже некоторого критического значения, ассоциирующегося с каким-либо заданным свойством. Таким образом, любое свойство материала может быть в значительной степени изменено и прогнозируемо посредством контролируемого селективного синтеза и сборки наноразмерных «строительных блоков». В качестве строительных блоков для создания наноструктур могут использоваться атомы, молекулы, кластеры и наночастицы. Такие характеристики «строительных блоков», как размер и распределение по размеру, состав, изменение состава и морфология, должны хорошо контролироваться. Также, огромное значение имеет граница раздела между «строительными блоками» и их окружением [5].
Высокая площадь поверхности наноматериалов может быть достигнута либо за счет создания маленьких частиц или кластеров, либо за счет синтеза материалов, у которых площадь поверхности пустот (пор) высока по сравнению с количеством твердой фазы. Под первую категорию подпадают такие материалы, как высокодисперсные катализаторы на основе металлов, закрепленных на подложке, и газофазные кластеры. Микропористые (нанопористые) материалы, такие, как цеолиты, неорганические оксиды с высокой площадью поверхности, пористый углерод принадлежат ко второй категории [5].
Обычно синтез наноструктур с высокой площадью поверхности идет по одному из двух фундаментальных направлений:
1) Так называемый "снизу вверх" подход (или конденсация), при котором наноструктуры строятся из индивидуальных атомов или молекул. Это основа большей части «науки о кластерах» равно, как и синтеза кристаллических материалов, обычно химическим путем. Используя этот подход, получают как частицы с высокой площадью поверхности, так и микро- и мезопористые кристаллические материалы с высоким объемом пустот (пор).
) Подход "сверху вниз" (или диспергирование), в котором наноструктуры получают путем разрушения исходных материалов. Это основа для таких методов, как механическое дробление, литография, которые обычно используются для получения наноразмерных материалов, которые, в свою очередь, могут использоваться непосредственно или как «строительные блоки» для макроскопических структур [5, 6].
Оба подхода обладают своими определенными преимуществами. Метод "сверху вниз" является идеальным с точки зрения возможности соединения и интеграции, как в электронной схеме. "Снизу вверх" сборка очень эффективна при создании идентичных структур с атомарной точностью, таких как супрамолекулярные функциональные единицы в живых организмах [2].
В рамках двух упомянутых направлений существует широкий спектр способов синтеза и сборки, начиная от биологических методов для молекул способных к самосборке и заканчивая усложненными химическими методами осаждения и разнообразными химическими и физическими аэрозольными техниками для создания кластеров или наночастиц с последующим их диспергированием или связыванием в консолидированные формы [5, 7 - 11]. Отнесение к тому или иному направлению приготовления проводится в зависимости от ключевой стадии, входящей в данный метод и в значительной степени определяющей основные показатели получаемого наноматериала [6].
Так, например, к направлению "снизу вверх" будут относиться следующие методы: осаждение из газовой фазы (конденсация инертного газа [11], химическая паровая конденсация [11, 12], плазменное напыление [13], сжигание в пламени [14], термический пиролиз [15], электрораспыление: [16]); осаждение из растворов ; (золь-гель метод [6], использование носителей [17, 18], электроосаждение [19], радиолиз [20] (восстановление; солей металлов под действием сольватированных электронов и свободных радикалов) и фотолиз фотолабильных комплексов металлов [21]).
К направлению "сверху вниз" относятся: механическое: диспергирование [22], травление [6], термолиз [23], лазерная абляция [24]; акустическая кавитация [25]; (ультразвуковая обработка) и гидродинамическая кавитация [26] (золь-гель раствор перемешивается при быстром сжатии и сильном • нагреве в суперкритических условиях, высвобождающиеся - гидродинамические пузырьки отвечают за нуклеацию, рост и охлаждение наночастиц).
1.2 Основные закономерности формирования
нанофазы в растворе
Необходимо отметить, что «влажный химический» синтез (осаждение из растворов с использованием восстанавливающего агента) у открытый 150 лет назад М. Фарадеем [27], получил наибольшее распространение при создании каталитически активных наночастиц металлов [7] Первый воспроизводимый синтез такого рода был осуществлен J. Turkevich с сотр., которые получили частицы Au размером 20 нм путем восстановления [AuCl4]- цитратом [28]. Ими также был предложен механизм: ступенчатого формирования: наночастиц путем нуклеации, роста и агломерации.
Получение наночастиц в рамкахподхода «снизу
вверх» в жидкой ¡фазе
происходит посредством контролируемых химических, реакций и самосборки
[29].
В
обобщенном
виде схему формирования наночастиц металла в растворе можно представить
следующим образом [7]:
xMn+ + nxe-
→M0n
(кластер)
Термодинамически движущая сила для формирования новой фазы должна уравниваться свободной поверхностной энергией маленькой частички. В процессе образования новой фазы, свободная поверхностная энергия управляет ростом коллоидной частицы, при этом каждая частица находится в локальном состоянии равновесия с растворителем [30].
В дисперсиях, содержащих как большие, так и маленькие частицы, концентрация растворенного вещества выше рядом с маленькими частицами, а диффузионный поток растворенного вещества направлен от маленьких частиц к большим. В результате маленькие частицы уменьшаются в размерах и растворяются, а большие увеличиваются в размерах, то есть имеет место так называемое «созревание Оствальда» [30].
Модель, предложенная для объяснения осаждения из
раствора, основывается на диаграмме Ла Мера (Рис. 1), которая иллюстрирует
зависимость концентрации от времени в ходе осаждения при условии, что
концентрация нуклеация является лимитирующей стадией процесса.
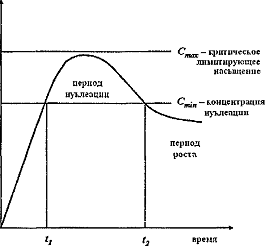
Рисунок 1. Диаграмма
Ла Мера. Концентрация растворенного вещества до и после нуклеации как функция
времени
Вначале концентрация растворенного вещества
возрастает, и как только она достигает критического значения насыщения,
происходит нуклеация. Это приводит к снижению концентрации растворенного
вещества, и Стах снижается до Сmin,
при которой процесс нуклеации уступает место процессу роста. Дальнейшее
снижение концентрации связано с ростом частиц, который продолжается до тех пор,
пока концентрация не достигнет равновесного значения. Однако, необходимо
отметить, что модель Ла Мера не учитывает стабилизацию образующихся частиц
[30].
.3 Стабилизация наночастиц металлов
Несмотря на широкий спектр методов синтеза наночастиц, описанный в разделе 1.1, в процессе создания наноструктурированных материалов важно учитывать, что «строительные блоки» для этих материалов сохраняют свои уникальные свойства до тех пор, пока они не консолидированы. Таким образом, существует два критических момента:
) контроль размера и состава компонентов нанокластеров, являются ли они аэрозольными частицами, порошками, полупроводниковыми точками или другими нанокомпонентами. Например, в наноразмерных каталитических материалах химическая селективность ассоциируется с локальным окружением так называемых активных центров. Под этим подразумевается, что размер; тип и геометрия атомов, составляющих активный центр, играют критическую роль в определении условий, при которых эти активные центры будут способны выполнять определенные функции;
) контроль границ раздела и распределения нанокомпонентов внутри полностью сформированных материалов.
Эти два аспекта формирования наноструктур неразрывно связаны; тем не менее, важно понять, как осуществить раздельный контроль над нуклеацией наноструктурированных «строительных блоков» и ростом (например, минимизация, коагуляции или агломерации) этих компонентов в ходе процесса синтеза и сборки. Обеспечение такого контроля касается важности следующего:
- химической, термической и временной стабильности сформированных наноструктур. Обычно считается, что чем меньше наноструктура (в случае катализа металлами, активный центр), тем более вероятно, что она может перемещаться, агрегировать, быть отравлена, разложиться шли изменить форму, состав или морфологию при температурном и/или химическом воздействии. Для практического применения важно определить. рамки стабильной работы такого материала, когда особая структура будет отвечать за желаемое его поведение.