Материал: Шмид Р. Наглядная биотехнология и генетическая инженерия
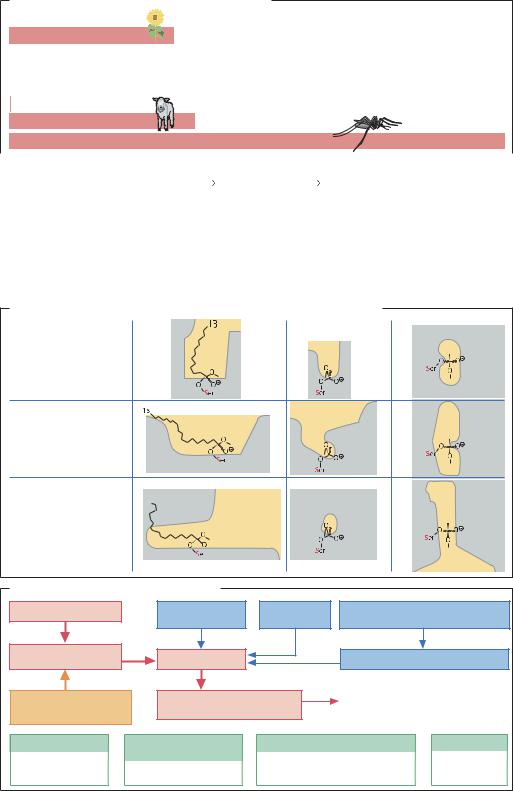
Разнообразие живых организмов (число видов)
 Простейшие 30 800
Простейшие 30 800
Высшие растения 248 400
 Водоросли 26 900
Водоросли 26 900  Грибы 69 000
Грибы 69 000
 Прокариоты (бактерии и археи) 4 800 Вирусы 1 000
Прокариоты (бактерии и археи) 4 800 Вирусы 1 000 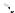

Животные 281 000
|
|
|
|
|
|
Насекомые 751 000 |
|
|
|
|
|
|
|
||
|
Свойства различных ДНК-полимераз |
|
|
|
|
||
|
|
|
|
|
|||
|
|
|
|
|
|
||
|
Источник |
Время |
3' 5'-экзонуклеаз- |
5' 3'-экзонуклеаз- |
Свойства концевых |
|
|
|
|
полужизни |
ная активность |
ная активность |
участков продукта |
|
|
|
|
фермента |
|
|
|
|
|
|
|
при 95° С, мин |
|
|
|
|
|
|
Thermus aquaticus |
40 |
Отсутствует |
Присутствует |
3'А |
|
|
|
Thermotoga maritima |
20 |
Отсутствует |
Присутствует |
3'А |
|
|
|
Pyrococcus furiosus |
> 120 |
Присутствует |
Отсутствует |
? |
|
|
|
Thermococcus litoralis |
1380 |
Присутствует |
Отсутствует |
> 95% тупых концов |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Pазнообразие липаз (структура и консенсусная последовательность)
Candida antarctica B (S = серин
в активном центре)
– TWSQG – |
0,5 нм |
|
|
|
|
Rhizomucor miehei
– GHSLG –
Candida rugosa
– GESAG – |
|
|
|
|
|
Способы получения новых ферментов |
|
|
|
|
|
Скрининг ферментов |
Белковая |
Направленная |
Выделение ДНК из проб, отобранных |
|
|
|
инженерия |
эволюция |
в необычных средаx обитания |
|
|
Клонирование |
Метод получения |
|
Экспрессия в организмах-хозяевах |
|
|
(не всегда) |
|
|
|||
|
|
|
|
|
|
Скрининг in silico (базы |
Применение |
|
Традиционный путь |
|
|
данных о структуре ДНК) |
в промышленных технологиях |
|
|
|
|
ДНК |
Расщепление |
Экспрессия в клетках-хозяевах |
Отбор |
|
|
Из донных |
рестриктазами |
E. coli, стрептомицеты и др. |
Выбор |
|
|
Получение фрагментов |
|
||||
отложений, |
|
|
«подходящего» |
|
|
из почвы |
ДНК необходимой длины |
|
|
фермента |
105 |
|
|
|
|
|
|
Ферменты |
Белковая инженерия |
ковая инженерия принято понимать замену амино- |
|
|
ВВЕДЕНИЕ. Под термином белковый дизайн или бел- |
|
кислоты (аминокислот) в белке методами генетиче- |
|
ской инженерии. Такие изменения проводят с целью: |
1)изучения механизма ферментативной реакции;
2)изменения субстратной или антигенной специфичности белка; 3) создания белка с новыми свойствами (температурная и рН-стабильность, устойчивость к действию протеиназ, растворимость, аллергенные свойства). Для этого в белке с известной аминокислотной последовательностью осуществляют направленную замену определенной аминокислоты. Такой подход называется рациональным дизайном. Отбор среди множества белков, полученных в результате случайного мутагенеза, тех, которые обладают определенными свойствами, называется направленной эволюцией.
ОБЩИЕ ПРИНЦИПЫ. Оба метода – рациональный дизайн и направленная эволюция – предполагают внесение мутаций в ген исследуемого белка и последующую экспрессию мутантных форм. Информацию о том, какую аминокислоту следует изменить, в случае белковой инженерии получают из структуры белка (например, рентгеноструктурного анализа кристалла белка или ЯМР-исследования) или структурных моделей, полученных методами биоинформатики из сравнения с гомологичными белками с известной пространственной структурой.
МУТАГЕНЕЗ. В современных исследованиях с целью делеции определенной аминокислоты или ее замены используется метод ПЦР. Разработаны многочисленные методики, позволяющие достаточно быстро и воспроизводимо осуществлять модификации белка. Для проведения случайного мутагенеза ген в составе вектора вносят в клетки штамма E. coli, в котором нарушена система репарации ДНК, и затем культивируют клетки в условиях, вызывающих мутации. Другой способ введения случайных мутаций заключается в изменении условий реакции ПЦР (например, добавление ионов Mn2+), приводящих к увеличению вероятности ошибок при амплификации ДНК до 1–3%. Метод gene shuffling основан на том, что гомологичный ген (>80% идентичных оснований) ферментативным путем расщепляют на небольшие фрагменты, а затем мутации вносятся в ходе ПЦР как результат случайной (статистической) рекомбинации.
РАЦИОНАЛЬНЫЙ ДИЗАЙН. Информацию о пространственной структуре белка получают из данных рентгеноструктурного или ЯМР-анализа. К середине 2005 г. данные о пространственной структуре почти 30 000 белков были размещены в базе данных (Protein DataBase, PDB). Когда таких данных нет, то ис-
106 пользуют компьютерные банки данных: если имеется
белок с известной структурой, более чем на 30% гомологичный исследуемому, можно предсказать структуру исследуемого белка (молекулярное моделирование). Еще недавно подобное моделирование было доступно лишь в виде приближенных расчетов для условий вакуума. С использованием современных суперкомпьютеров и расчетных систем становится возможным предсказание структуры белка, особенностей его взаимодействия с субстратом или антигенами в водном растворе. Расчеты молекулярных механизмов зачастую требуют обработки данных о десятках тысяч атомов одновременно. Данные, полученные с применением такой «in silico»-методики, всегда должны контролироваться в ходе многократных циклов моделирования и в генноинженерных экспериментах («цикл белковой инженерии»).
НАПРАВЛЕННАЯ ЭВОЛЮЦИЯ. В отличие от рационального белкового дизайна для осуществления направленной эволюции не нужно знать структуру белка. В ген исследуемого белка (фермента) случайным образом вносят мутации, а затем с помощью быстрого функционального теста из образовавшихся форм белка выбирают те, которые обладают улучшенными свойствами, например повышенной активностью. Метод phage display позволяет быстро анализировать способность большого количества мутантных белков (1010) связываться с другими веществами, прежде всего с антителами. В обоих случаях решающую роль играет качество чипов. В последнее время методы направленной эволюции позволили достичь значительных успехов в оптимизации ферментов, используемых в промышленности. Стало возможным менять субстратную специфичность белков, их термостабильность и устойчивость в спиртовых растворах. Для скрининга большого количества мутантов разработаны автоматические многоканальные системы.
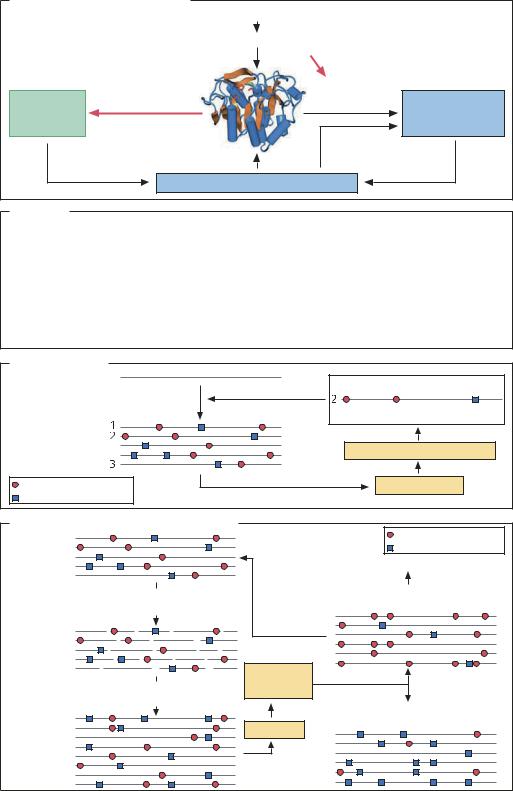
Принципы белковой инженерии |
|
|
|
|
|
Клонирован структурный ген |
|
||
|
Имеется ли информация о структуре? |
|
||
|
Компьютерное моделирование, |
Да |
Нет |
|
|
выявление аминокислотных |
|
|
|
|
остатков, играющих важную |
|
|
|
|
роль в поддержании |
|
Направленная |
|
|
структуры белка и его |
|
|
|
Сайт- |
|
эволюция |
Случайный мутагенез |
|
функционировании |
|
|||
направленный |
|
|
|
(«неточная» ПЦР, |
мутагенез |
|
|
|
gene shuffling) |
|
Многократное |
|
Многократное |
|
|
повторение цикла |
|
повторение цикла |
|
|
Экспериментальная проверка модели |
|
||
Примеры |
|
|
|
|
Фермент |
Метод |
Мутация |
Эффект |
|
Протеаза, используемая |
Рациональный дизайн |
222Мet → Аla |
Устойчивость к окислению |
|
в стиральном порошке |
|
|
|
|
Инсулин человека |
Рациональный дизайн |
22Lys → Pro |
Замедленная деградация |
|
Тканевой активатор |
Рациональный дизайн |
4 |
положения + замена |
Замедленная деградация |
плазминогена |
|
углеводного остатка |
|
|
Пенициллинацилаза |
Направленная эволюция |
5 |
положения |
Повышенная устойчивость |
Р450-гидроксилаза |
Направленная эволюция |
4 |
положения |
Изменена субстратная |
жирных кислот |
|
|
|
специфичность |
«Неточная» ПЦР |
|
|
Исходный ген |
Результат: |
|
|
||
Случайный мутагенез |
Новый цикл |
|
(«неточная» ПЦР) |
новые позитивные свойства |
|
|
||
Набор ДНК |
|
|
с различными |
Функциональный анализ белков |
|
изменениями |
||
|
||
«Позитивные» мутации |
Экспрессия |
|
«Негативные» мутации |
|
|
«Перемешивание генов» (gene shuffling) |
«Позитивные» мутации |
|
Набор |
||
«Негативные» мутации |
||
измененных |
||
Оптимизированный ген |
||
ДНК |
||
Расщепление ДНКазой I, |
Отбор «позитивных» мутантов |
|
фрагментация |
Многократное |
|
|
повторение |
|
Набор |
цикла |
|
|
||
случайных |
|
|
фрагментов |
Функциональ- |
|
|
||
Случайная рекомбинация |
ный анализ |
|
белков |
||
фрагментов (ПЦР) |
||
|
«Негативные» мутанты удаляются
Экспрессия
Рекомбинированные ДНК
107

Пекарские и кормовые дрожжи
Пекарские и кормовые дрожжи
ВВЕДЕНИЕ. Технология приготовления теста из муки известна с древних времен. На древнеегипетских глиняных табличках изображен процесс выпечки «пивного» хлеба из ячменных зерен при дрожжевом брожении. До XIX в. в Европе для хлебопечения также использовали пивные дрожжи, которые получали по «голландскому» способу (1750 г.) фильтрацией солодового отстоя или по «венской» технологии (1800 г.) – соскабливанием со стенок бродильного чана. В 1870 г. Луи Пастер показал, что рост биомассы пекарских дрожжей Saccharomyces cerevisiae происходит в аэробных условиях. С этого времени культивирование пекарских дрожжей осуществляется в открытых резервуарах с интенсивным перемешиванием и аэрацией. Основным источником углерода служит меласса. Мелкими хозяйствами в некоторых странах в 30-е гг. ХХ в. были предприняты первые попытки получения кормовых дрожжей. В послевоенные годы их применение оказалось наиболее актуальным в развивающихся странах, где имелся недостаток белковых продуктов.
СЫРЬЕ ДЛЯ ФЕРМЕНТАЦИИ. Чаще всего сырьем для ферментации служит меласса (отходы производства сахара из сахарной свеклы или сахарного тростника). Это объясняется низкой стоимостью мелассы, а также высоким содержанием в ней лекго расщепляемых азотсодержащих соединений, витаминов и микроэлементов. Мелассу эстрагируют горячей водой из измельченной массы сахарной свеклы или тростника. Меласса содержит 40–50% сахарозы, которая под действием инвертазы из Saccharomyces cerevisiae
превращается в глюкозу и фруктозу.
ТЕХНОЛОГИЧЕСКИЙ ПРОЦЕСС. Для того чтобы коэффициент превращения мелассы в биомассу дрожжей Ys был максимален, необходимо насколько возможно снизить скорость образования этанола; для этого культивирование проводят при интенсивной аэрации
итщательно регулируют содержание глюкозы в питательной среде. При содержании глюкозы >100 мг/л происходит ингибирование катаболитами,
иначинается анаэробное брожение, сопровождающееся образованием этанола. Современные установки для культивирования дрожжей обладают системой контроля за поступлением мелассы и устройствами для перемешивания. Эффективность процесса превращения меллассы в биомассу дрожжей описывают
параметром Н27 – это относительная величина, равная 27% массы сухих дрожжей в мелассе. Меласса содержит 50% сахара, а максимальный выход дрожжей составляет 54 г на 100 г израсходованного сахара, таким образом, из 1 кг мелассы можно получить 1 единицу Н27 (т. е. 270 г дрожжей из 1 кг мелас-
сы). В результате высушивания прессованных дрожжей в мягких условиях получают сухие дрожжи, которые могут храниться несколько месяцев, а при добавлении воды и сахара начинают работать уже через несколько минут.
КОРМОВЫЕ ДРОЖЖИ. По рыночной цене и пищевой ценности для сельскохозяйственных животных кормовые дрожжи составляют конкуренцию таким источникам белка, как рыбная или соевая мука. Решающим фактором, влиящим на цену кормовых дрожжей, является доступность источника углерода, необходимого для осуществления ферментации. В настоящее время изучаются возможности выращивания дрожжей на отходах нефтяной и газовой промышленности, этаноле, метаноле, целлюлозе, крахмале, молочной сыворотке и других доступных источниках углерода. Шведский метод Симба, основанный на использовании картофельного крахмала (с участием дрожжей
Endomycopsis fibuliger и Candida utilis; при этом первый вид расщепляет крахмал, а второй синтезирует клеточный белок); финский метод Пекило, в котором гриб Paecilomyces variotii синтезирует клеточный белок из углеводных остатков от производства целлюлозы, а также канадский метод Ватерлоо, в основе которого выращивание гриба Chaetomium cellulolyticum на побочных продуктах сельского хозяйства, лесозаготовок и лесопереработки (солома, багасса*, стойловой навоз, древесные опилки) – все эти технологии нашли широкое применение из-за высоких цен на соевую муку, но впоследствии в связи с удешевлением растительного белка они потеряли свою конкурентоспособность. Сейчас применяется только метод МакДугалла, разработанный фирмой Rank-Hovis, в котором средой для роста гриба Fusarium graminearum служит очищенная глюкоза. QuornTM, клеточная масса этого гриба, ценится как фирменное вегетарианское блюдо с хорошим вкусом и необычной текстурой, поэтому данный метод успешно реализуется во многих странах.
108 * Багасса – жом сахарного тростника. – Прим. пер.
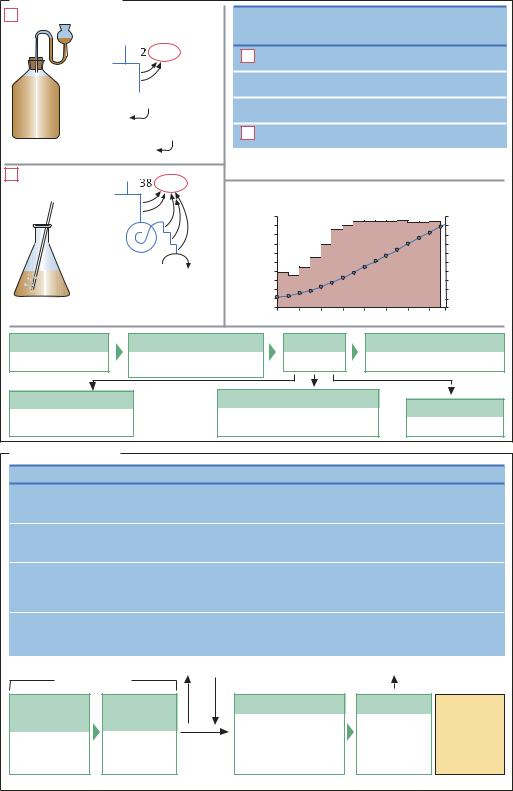
Пекарские дрожжи
A Брожение |
Метод |
Количество |
Этанол, л |
Глюкоза |
|
полученной |
|
|
биомассы Н27*, кг |
|
|
|
a |
АТФ |
|
|
A |
«Голландский» |
|
3–6 |
25–30 |
||
|
|
|
|
|
|
|
(до 1850 г.) |
|
|
|
|
|
|
|
|
|
|
|
|
«Венский» |
|
|
14 |
|
25 |
|
|
|
Пируват |
|
|
|
(до 1915 г.) |
|
|
|
|
|
|
|
|
|
|
|
«Копенгагенский» |
|
20 |
|
20 |
||
|
|
|
|
|
|
|
|
|
||||
|
2 CO2 |
|
|
|
(с 1877 г.) |
|
|
|
|
|
||
|
|
Ацетальдегид |
|
|
Б |
Современные |
|
до 85 |
|
< 1 |
||
Анаэробный |
|
|
Этанол |
|
|
|
технологии |
|
|
|
|
|
процесс |
|
|
|
|
* Современные технологии позволяют получать до 27 кг |
|
||||||
|
|
|
|
|
|
|||||||
Б Дыхание |
|
Глюкоза |
|
|
сухого веса дрожжей (Н27) из 100 кг мелассы |
|
|
|||||
Воздух |
|
|
АТФ |
|
Культивирование дрожжей в системе |
|
|
|||||
|
|
|
|
|
|
|
||||||
|
|
|
a |
|
|
с автоматизированной подачей мелассы |
|
|
||||
Интенсивная |
б |
|
|
|
дрожжей,Биомасса Н |
0 |
|
|
|
0 |
Поступлениемелассы, л/ч |
|
Цикл лимонной кислоты |
|
|
|
|||||||||
|
|
|
|
в |
|
|
20 |
|
|
|
2000 |
|
|
|
|
|
|
|
|
16 |
|
|
|
1600 |
|
|
|
б |
|
|
27 |
12 |
|
|
|
1200 |
|
|
|
|
|
O2 |
Н2O |
|
|
8 |
|
|
|
800 |
|
|
|
|
|
|
4 |
|
|
|
|
|
||
|
a |
Гликолиз |
|
|
|
|
|
|
400 |
|
||
аэрация |
в |
Дыхательная цепь |
|
|
0 |
4 |
8 |
12 |
Время, ч |
|
||
Предферментация |
|
Биореактор |
|
Выделение |
|
Побочные продукты |
||||||
Инокулят штамма |
|
|
Рабочий объем более 100 м3, |
Сепаратор |
|
Этанол, сточные воды, барда |
||||||
|
|
|
меласса, источники азота |
|
|
|
|
|
|
|||
Товарные дрожжи Н27 |
|
|
|
Сухие пекарские дрожжи |
|
Кормовые дрожжи |
||||||
|
|
|
|
|
|
|
|
|
|
|||
Вакуумный вращающийся |
|
Экструзия, высушивание в псевдо- |
|
|
||||||||
барабанный фильтр |
|
|
|
ожиженном слое, охлаждение |
|
Пастеризация |
|
|||||
Кормовые дрожжи |
|
|
|
|
|
|
|
|
|
|
||
Сырье |
|
|
Дрожжи и грибы |
|
Примечания |
|
|
|
|
|
||
Картофельный крахмал |
Endomycopsis fibuliger |
Метод Симба (Швеция), Е. fibuliger гидролизует крахмал, |
||||||||||
|
|
|
Candida utilis |
|
Candida utilis растет быстрее и при росте на глюкозе |
|
||||||
|
|
|
|
|
|
формирует биомассу |
|
|
|
|
||
Молочная сыворотка |
|
Kluyveromyces fragilis |
При очистке сточных вод в молочной промышленности. |
|||||||||
|
|
|
|
|
|
Продукт содержит дрожжи и остаточные количества |
|
|||||
|
|
|
|
|
|
молочной сыворотки |
|
|
|
|
||
Отработанный |
|
|
Saccharomyces cerevisiae, Остатки гексоз перерабатываются S. cerevisiae, пентоз – |
|||||||||
сульфитный щелок |
|
|
Candida utilis, |
|
C.utilis, метод Пекило (Финляндия); ферментация |
|
||||||
|
|
|
Paecilomyces variotii |
в непрерывном режиме для получения кормовых дрожжей |
||||||||
|
|
|
|
|
|
из отработанного сульфитного щелока |
|
|
||||
Очищенная глюкоза |
|
Fusarium graminearum |
Метод Rank-Hovis McDougall (Великобритания); |
|
||||||||
|
|
|
|
|
|
использование волокнистой структуры мицелия в качестве |
||||||
|
|
|
|
|
|
«функционального белка» |
|
|
|
|||
Метод Пекило |
SO2 |
Воздух, NH3 |
|
Сжигание отходов |
|
|||||||
|
|
|
|
|
|
|
|
|
||||
Отработанный |
|
SO2-стриппер |
|
|
|
Биореактор |
|
|
Обработка |
|
|
|
сульфитный |
|
(отпарная |
|
|
|
|
|
|
|
|
|
|
щелок |
|
колонна) |
|
|
Paecilomyces variotii, |
Фильтр, |
52–57% |
|
||||
|
|
|
3 |
|
|
360 м3, NH , |
|
пресс, сушка |
|
|||
Водяной пар |
|
|
|
|
|
3 |
|
|
|
чистого белка |
||
|
100 м /ч |
Охлаждение ионы калия и фосфаты, |
|
|
||||||||
|
|
|
|
|
|
30 °С, рН 4 |
|
|
|
|
|
|
Уровень переработки биодеградируемых веществ в молоке достигает 85% |
|
|
|
|
109 |
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|