Материал: Прищепа И.Н., Ефременко И.И. Нейрофизиология
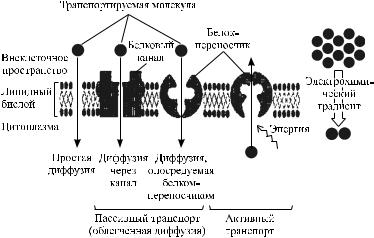
Рис. 22. Схематическое изображение пассивного транспорта молекул
ответствующего иона. Это тоже переносчики, но их способность транспортировать ионы регулируется с помощью специальных механизмов, зависимых от уровня мембранного потенциала или состояния специфических клеточных рецепторов, управляемых этими каналами. Кроме того, изменение ионной проницаемости, особенно у потенциалзависимых ионных каналов, может происходить с огромной скоростью – ка-
нал способен открываться только на 1–3 мс.
Натриевые каналы имеют устья, селективный фильтр, воротный механизм (рис. 23). Ворота у них двух типов – активационные и инактивационные. В условиях покоя (при мембранном потенциале, равном –80 мВ) активационные ворота закрыты, но они «готовы» в любой момент открыться, а инактивационные ворота открыты. При снижении мембранного потенциала (например, с +80 до +60 мВ) активационные ворота открываются, в результате чего интенсивность натриевого потока, входящего в клетку, возрастает. Однако спустя определенное время (1–2 мс) инактивационные ворота закрываются, т.е. происходит инактивация натриевых каналов. Следствием этого процесса является снижение почти до нуля входящего в клетку потока ионов Na+. Некоторое время спустя закрываются активационные ворота, открываются инактивационные ворота, и канал готов к новому циклу.
151
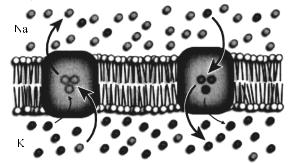
Рис. 23. Принцип действия натриевого насоса клеточной мембраны
Промежуток времени, в течение которого натриевые кана-
лы не способны пропускать через себя поток ионов Na+, получил название рефрактерного периода или периода невозбуди-
мости. У нейронов и скелетно-мышечных волокон он очень короткий (в пределах 1–3 мс), в клетках сердца длится 250– 300 мс. Скорость восстановления проницаемости натриевых каналов определяет лабильность возбудимых клеток, т.е. их способность к ритмической активности. Чем выше скорость, тем выше лабильность.
Натриевые каналы играют исключительно важную роль в деятельности нейронов, нервных и скелетно-мышечных волокон, миокардиоцитов и других возбудимых клеток, так как обеспечивают начальный компонент потенциала действия, т.е. его фазу деполяризации.
Натриевые каналы блокируются тетрадотоксином, а также новокаином и другими местными анестетиками, что служит основой для широкого применения местных анестетиков в ме-
дицинской практике, в частности с целью обезболивания. Калиевые каналы также характеризуются высокой избира-
тельностью по отношению к ионам К+. Каналы играют очень важную роль: с их участием формируется мембранный потенциал всех возбудимых клеток, а в период генерации потенциала действия они обеспечивают процесс реполяризации, т.е. восстановления исходного уровня мембранного потенциала. Кроме того, степень проницаемости калиевых каналов определяет способность возбудимых клеток к самовозбуждению,
или автоматии.
Кальциевые каналы обеспечивают поступление ионов Са2+ из внеклеточной среды во внутриклеточную, что имеет важ-
152
ное значение для процессов возбуждения нейронов, миокардиоцитов, гладкомышечных клеток, а также для функционирования синаптической передачи.
Характеристика активного транспорта веществ
Различают первично-активный и вторично-активный
транспорт.
Первично-активный транспорт – это такой транспорт, когда энергия расходуется непосредственно на перенос частиц. Он включает: перенос отдельных ионов вопреки концентрационному и электрическому градиентам с помощью специальных ионных насосов; эндоцитоз, экзоцитоз и транс-
цитоз.
Транспорт вещества с помощью ионных насосов. Насосы представляют собой белковые молекулы, обладающие свойствами переносчика и АТФ-азной активностью. Непосредственным источником энергии являются АТФ. Специфичность насосов заключается в том, что они обычно переносят какой-то определенный ион или два иона. Хорошо изучены Na+/Ka+-, Ca2+- и H–-насосы.
Постоянная работа насосов необходима для поддержания концентрационных градиентов ионов, электрического заряда клетки и движения воды и незаряженных частиц в клетку и из клетки вторично-активно согласно законам диффузии и осмоса.
Эндоцитоз, экзоцитоз и трансцитоз – это варианты активного транспорта, при которых меняется архитектура мембран.
Они осуществляются с затратой энергии.
Эндоцитоз – это процесс активного введения крупномолекулярных частиц из среды в клетку. Такой вид транспорта, к примеру, имеет место у новорожденных детей, которые
смолоком матери получают антитела (иммуноглобулины). Эти крупные белковые частицы, не разрушаясь, с помощью энтероцитов всасываются в кишечнике и попадают в кровь
ребенка, будучи совершенно ненарушенными и способными к выполнению своих функций (рис. 24, а).
При эндоцитозе клеточная мембрана образует впячивания, или выросты, внутрь клетки, которые, отшнуровываясь, превращаются в пузырьки. Последние затем обычно сливаются
спервичными лизосомами, образуя вторичные лизосомы,
153
в которых содержимое подвергается гидролизу – внутриклеточному перевариванию. Продукты гидролиза используются
клеткой.
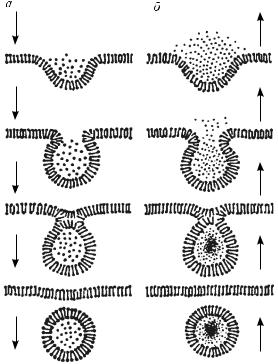
Экзоцитоз – это процесс выделения крупных молекул из клетки (рис. 24, б). Пример – выделение квантов медиатора из везикулы в синапсе. По сути, экзоцитоз представляет собой процесс, обратный эндоцитозу. При экзоцитозе вначале происходит упаковка транспортируемого вещества в мембранные экзоцитозные пузырьки. После того как такие структуры сформировались, они приближаются к плазмолемме и сливаются с ней. При этом мембрана пузырька встраивается в плазмолемму, а его содержимое выделяется во внеклеточное про-
странство.
Трансцитоз наблюдается в тех клетках, где на поверхности формируется эндоцитозный пузырек, который переносится
Рис. 24. Сравнение эндоцитоза (а) и экзоцитоза (б)
154
к противоположной поверхности клетки и выделяет свое содержимое во внеклеточное пространство. Трансцитоз характерен для эндотелиальных клеток кровеносных сосудов. В этих клетках пузырьки могут объединяться, образовывая временные трансцеллюлярные каналы, через которые транс-
портируются водорастворимые молекулы.
Вторично-активный транспорт представлен в эпителиальных клетках кишечника и в эпителии почек. В данном случае одним механизмом транспортируются одновременно две молекулы. В случае Na+/K+-насоса имеет место антипорт (поток ионов K+ направлен внутрь клетки, поток ионов Na+ направлен из клетки в среду). В случае же вторично-активного транспорта имеет место симпорт (потоки ионов направлены внутрь клетки).
Классификация биопотенциалов
Биопотенциалы – это общее название всех видов электри-
ческих процессов в живых системах.
Потенциал повреждения представляет собой исторически первое понятие, введенное для обозначения электрической активности живых организмов. Оно означает разность потенциалов между неповрежденной и поврежденной поверхностями живых возбудимых тканей (мышцы, нервы). При этом поврежденная поверхность является электронегативной по отношению к неповрежденной поверхности. Изучение природы потенциала повреждения послужило толчком к соз-
данию мембранной теории возникновения биопотенциалов.
Мембранный потенциал, или потенциал покоя (МП,
ПП), – это разность потенциалов между наружной и внутренней поверхностями мембраны клетки (мышечного волокна) в условиях покоя. Обычно МП различных возбудимых клеток
составляет 50–90 мВ со знаком минус внутри клетки. Потенциал действия (ПД) представляет собой относи-
тельно быстрое изменение мембранного потенциала возбуди-
мых клеток во время их возбуждения.
Возбуждающий постсинаптический потенциал (ВПСП) и тормозной постсинаптический потенциал (ТПСП) – это
изменение мембранного потенциала постсинаптической мембраны при передаче возбуждающего или тормозного воздей-
155