Материал: ПАТ. ФИЗИОЛОГИЯ ОТВЕТЫ ЗАЧЕТ
Терминальный период голодания наступает при расходовании 1/3-1/2 части всех белков (в норме 15 кг) и характеризуется усиленным распадом тканей. Развивается глубокое угнетение центральной нервной системы, нарастают слабость, апатия, переходящие в глубокую кому. Температура тела постепенно падает, опускаясь к моменту смерти до 30-28 °С. Выделение азотсодержащих продуктов с мочой (мочевина, креатинин, мочевая кислота, аминокислоты, пептиды), содержание калия, фосфора в моче, явления ацидоза и ацетонемии возрастают. Смерть наступает от интоксикации и истощения запасных веществ организма, в крови прогрессирующе нарастает содержание биогенных аминов, ряда гормонов (катехоламины) и других биологически активных веществ. Откармливание при голодании возможно даже в терминальном периоде. Сначала применяется искусственное стимулирование сокоотделения в желудке и введение жидкой пищи в ограниченном количестве, затем постепенно переходят к более энергичному питанию после восстановления возбудимости пищевого центра. Перегрузка пищей в первые дни откармливания может вызвать тяжелые расстройства желудочно-кишечного тракта (рвота, поносы) и интоксикацию.
Лечение голоданием Никаких отрицательных последствий после перенесенного кратковременного голодания не отмечается. При часто повторяющихся голоданиях (4-5 раз) масса тела восстанавливается с каждым разом труднее, развивается жировая дистрофия печени. Голодание с лечебной целью применялось в древней Индии, Греции, Египте, в начале 80-х гг. XIX в. стало использоваться и в Европе для лечения сахарного диабета, ревматизма, подагры, при заболеваниях почек, гипертонии, бронхиальной астме, некоторых кожных, нервно-психических болезнях и др. По окончании лечебного голодания применяется ахлоридная диета (фруктовые соки, кефир, позже растительное масло) с максимальным содержанием витаминов и минеральных солей. При постоянном увеличении объема пищи и ее энергетической ценности осторожность связана с тем, что желудочнокишечный тракт в период лечебного голодания находится в состоянии гипофункции и атрофии. Период откармливания продолжается около 2 недель. Курс повторного лечебного голодания переносится значительно легче, но обязательным требованием является полное восстановление после предыдущего голодания.
23. Метаболические нарушения при тяжелы ранения и травма
Ведущими звеньями патогенеза травматической болезни вначале становятся острая массивная кровопотеря, специфические расстройства функций поврежденных органов, гипоксемия, токсемия, болевой синдром, нарушение регуляторных процессов, а в дальнейшем - при неблагоприятном течении - моно- или полиорганная недостаточность. Расстройства дыхания после травмы или ранения могут возникать в любом звене газообмена - в системе внешнего дыхания, крови, кровообращения, а также на уровне тканей. Помимо нарушений внешнего дыхания тяжелые механические повреждения сопровождаются изменениями транспорта кислорода к тканям, возникающим за счет как кровопотери и гемодинамических нарушений, так и за счет расстройств микроциркуляции. Расстройства легочного газообмена проявляются постепенным развитием артериальной гипоксемии, причинами которой являются: альвеолярная гиповентиляция, нарушение вентиляционно-перфузионных отношений, внутрилегочное шунтирование венозной крови, диффузионные нарушения в легких. Нарушается синтез и функции легочного сурфактанта, легочные капилляры тромбируются агрегатами тромбоцитов и микросгустками, резко возрастает сопротивление сосудов малого круга кровообращения для тока крови, изменяется капиллярная проницаемость. Возникает состояние, называемое "респираторным дистресссиндромом", которое имеет и довольно выраженные морфологические эквиваленты в виде интерстициальных отеков, микро- и макроателектазов, экстравазации клеток крови ("легочное опеченение"). Доставка кислорода к тканям у пострадавших ограничивается сниженной кислородной емкостью крови за счет анемии, депонирования и агрегации части эритроцитов. Развивается порочный круг с постепенным нарастанием гипоксемии, приводящей в конечном итоге к изменениям клеточного метаболизма и возникновению ацидоза. Тяжелые нарушения в системе дыхания вплоть до развития респираторного дистресс-синдрома взрослых практически всегда сопровождают и перитониты при заболеваниях органов брюшной полости.
Стереотипной начальной реакцией эндокринной системы на травму является активизация практически всех ее комплексов и звеньев. Конечным результатом ее активации является действие на разнообразные клеточные и межклеточные структуры, мобилизация глюкозы, аминокислот, задержка натрия и воды. Уже с первых минут после травмы в сыворотке крови обнаруживается увеличение концентрации АКТГ и кортизола, регулирующих ключевые процессы жизнедеятельности организма, которое достигает максимума через 1 час после травмы, с последующим снижением АКТГ от 3-4 до 14-21 суток после травмы, а кортизола - к 21-35 суткам. Уровень этих гормонов нарастает прямо пропорционально тяжести травмы. Усиливается секреция ренина, вазопрессина и альдостерона, которые регулируют осмоляльность, объем внеклеточной жидкости, обеспечивают задержку натрия в организме и выведение калия. В 3-7 раз повышается содержание в сыворотке крови соматотропного гормона, регулирующего обмен аминокислот и подавляющего катаболизм [403]. Значительно повышен после травмы уровень глюкагона, а уровень инсулина, хотя и повышается, но незначительно. Концентрация инсулина не соотносится с тяжестью травмы, а высокие уровни глюкозы в посттравматическом периоде объясняются не только ее мобилизацией но и снижением чувствительности инсулиновых рецепторов клетоК. Тяжелое повреждение практически всегда сопровождается подавлением функции половых желез, что проявляется снижением продукции тестостерона, который усиливает анаболические процессы. С тяжестью травмы коррелирует и ответ щитовидной железы, что проявляется снижением, как уровня, так и активности трийодтиронина и тетрайодтиронина.
В остром периоде травматической болезни формируются метаболические проявления срочной адаптации, связанные в основном с катаболическими процессами, затем постепенно наступает нормализация гомеостаза с активацией анаболических процессов. В случае возникновения гнойно-септических осложнений после 7 суток с момента ранения вновь начинают преобладать катаболические процессы, а затем в период выздоровления нормализация метаболизма может растягиваться на несколько месяцев. Активация гликогенолиза в печени и мышцах приводит к гипергликемии и глюкозурии, а усиление анаэробного гликолиза - к накоплению лактата. Содержание глюкозы, лактата и пирувата в сыворотке крови тесно коррелирует с тяжестью травмы. Время нормализации уровня лактата является важным прогностическим фактором. При нормализации его уровня в течение 24 часов выжили все пострадавшие, в течение 24-48 часов - 75%, а свыше 48 - только 14%.
При травматической болезни происходит усиление катаболических процессов, что проявляется гипопротеинемией, которая коррелирует с объемом кровопотери, тяжестью травмы и шока. Наряду со снижением уровня общего белка развивается диспротеинемия, характеризуемая большим снижением содержания альбумина и "белков острой фазы" - трансферрина, церулоплазмина и других. Усиленный распад белков и нарушение их синтеза приводит к повышению в плазме концентрации аминокислот, креатинина и мочевины, увеличивается содержание мочевины, креатинина и в моче. Повышение энергетических затрат приводит к увеличению липолиза, на что указывает повышение концентрации свободных жирных кислот и триглицеридов уже в первые сутки после травмы [520]. Биохимические изменения, возникающие при тяжелой механической травме, создают предпосылки для инициации липидной пероксидации. Накопление конечных продуктов перекисного окисления липидов (ПОЛ) - окисленных жирных кислот, шиффовых оснований, диеновых коньюгат, малонового диальдегида, - приводит к необратимой инактивации ферментов за счет структурной перестройки мембран клеток, изменению их проницаемости, вплоть до гибели клеток. Активность супероксиддисмутазы, являющейся важнейшим фактором антиоксидантной защиты, в начальный период травматической болезни несколько повышается, а затем при осложненном тече нии - снижается. В связи с повреждением клеточных мембран в сыворотке крови повышается активность ферментов: креатинфосфокиназы, лактатдегидрогеназы, аланинаминотрансферазы, аспартатаминотрансферазы. При травматической болезни наблюдается значительное повышение активности калликреинкининовой системы крови. В остром периоде болезни это проявляется высокой активностью калликреина, низким содержанием неактивных предшественников, повышенными БАЭЭ-эстеразной, антитриптической и нормальной кининазной активностями сыворотки крови. Состояние калликреин-кининовой системы находится в соответствии с величиной кровопотери и тяжестью шока и определяется характером клинического течения травматической болезни, особенно в остром ее периоде. Однако изменение таких показателей системы, как калликреин и кининаза, отличается в группах с различной локализацией травмы.
Содержание в сыворотке крови ионов натрия и калия в начальном периоде травматической болезни подвержено большим колебаниям, однако в дальнейшем отмечается гипокалиемия и незначительная гипернатриемия, степень которых определяется тяжестью травмы и клиническим течением послеоперационного периода.
Одним из интегральных показателей активности катаболических процессов в организме считается уровень осмоляльности плазмы крови. При тяжелых сочетанных травмах с массивной кровопотерей и при неблагоприятном течении травматической болезни в жидких средах организма происходит накопление осмотически активных веществ (мочевины, натрия, глюкозы и др.). Пролонгированная гиперосмоляльность плазмы крови является плохим прогностическим признаком.
При травме возникают условия для раз- 45 вития метаболического ацидоза - накопление лактата, пирувата, кетоновых тел, нелетучих минеральных кислот. Вредными последствиями ацидоза являются угнетение микроциркуляции с усилением дефицита доставляемого периферическим тканям кислорода, и, таким образом, усилением самой причины ацидоза. Однако в некоторых случаях тяжелой механической травмы развивается и метаболический алкалоз.
Тяжелая механическая травма, сопровождаясь повреждением жизненно важных органов, гипоксией, вызывая нарушение метаболизма, приводит к избыточному накоплению в сыворотке крови промежуточных и конечных продуктов обмена (лактат, пируват, мочевина, креатинин, билирубин), продуктов извращенного обмена (альдегиды, кетоны), иммунологически чужеродных продуктов расщепления пластического материала (продукты гидролиза гликопротеидов), компонентов регуляторных систем (факторы свертывающей и фибринолитической систем, кинин-калликреиновой системы, перекисного окисления липидов, биогенных аминов), органо- и цитолокализованных веществ (трипсин, амилаза, трансаминазы, миоглобин, лизосомальные ферменты), продуктов жизнедеятельности нормальной, условно-патогенной и патогенной микрофлоры (эндо- и экзотоксины). Важную роль в развитии эндотоксикоза играют средне-молекулярные полипептиды, которые вызывают вторичную иммунодепрессию, ингибируют фагоцитарную активность лейкоцитов, подавляют ферменты клеточных мембран, нарушают глюконеогенез. Глубокие нарушения процессов обмена веществ развиваются и у больных с перитонитом, выраженность которых пропорциональна тяжести перитонита. Происходит нарушение гормональной регуляции. Изменяются углеводный, липидный, белковый, водно-солевой обмены, нарушается кислотно-основное состояние, повышается ферментативная активность, выявляется избыточное накопление продуктов перекисного окисления липидов и снижение антирадикальной активности.
22. Нарушения кос организма (кислотно-основного состояния организма), принципы лечения
Показатели КЩР подразделяют на основные и дополнительные Основные показатели. Оценку КЩР и его сдвигов в клинической практике проводят с учётом нормальных диапазонов его основных показателей: pH, pCO2, стандартного бикарбоната плазмы крови, буферных оснований и избытка оснований капиллярной крови.• Дополнительные показатели. С целью выяснения причины и механизма развития негазовых форм нарушений КЩР определяют ряд дополнительных показателей крови (КТ, МК) и мочи (титруемая кислотность - ТК и аммиак).

Механизмы регуляции кислотно-щелочного равновесияВ норме в организме образуется почти в 20 раз больше кислых продуктов, чем щелочных. В связи с этим доминируют системы, обеспечивающие нейтрализацию, экскрецию и секрецию избытка соединений с кислыми свойствами. К этим системам относятся химические буферные системы и физиологические механизмы регуляции КЩР.
Химические буферные системы представлены, в основном, бикарбонатным, фосфатным, белковым и гемоглобиновым буферами. Буферные системы начинают действовать сразу же при увеличении или снижении [H+] и способны устранить умеренные сдвиги КЩР в течение 10-40 с. Ёмкость и эффективность буферных систем крови весьма высока
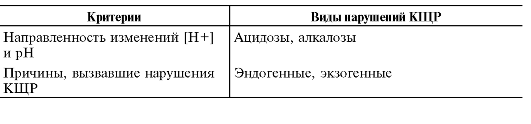

Ацидоз - типовая форма нарушения КЩР, характеризующаяся относительным или абсолютным избытком в организме кислот.В крови при ацидозе происходит абсолютное или относительное повышение [H+] и уменьшение pH ниже нормы (условно - ниже нейтральной величины pH, принимаемой за 7,39).
|
|
Алкалоз - типовая форма нарушения КЩР, характеризующаяся относительным или абсолютным избытком в организме оснований.В крови при алкалозе отмечается абсолютное или относительное снижение [H+] и увеличение pH (условно - выше нейтральной величины pH, принимаемой за 7,39).
Компенсированные и некомпенсированные нарушения КЩР
Определяющим параметром степени компенсированности нарушений КЩР является величина pH.
• Компенсированными сдвигами КЩР считают такие, при которых pH крови не отклоняется за пределы диапазона нормы: 7,35-7,45. За «нейтральную» величину условно принимают 7,39. При компенсированных формах нарушений КЩР изменяется абсолютная концентрация компонентов гидрокарбонатной буферной системы. Однако, соотношение [H2CO3]/[NaHCO3] сохраняется 20/1.
♦ При pH 7,38-7,35 - компенсированный ацидоз.
♦ При pH 7,40-7,45 - компенсированный алкалоз.
• Некомпенсированными нарушениями КЩР называют такие, при которых pH крови выходит за диапазон нормы. Некомпенсированные ацидозы и алкалозы характеризуются значительными отклонениями как абсолютной концентрации H2CO3 и NaHCO3, так и их соотношения.
♦ При pH 7,34 и ниже - некомпенсированный ацидоз.
♦ При pH 7,46 и выше - некомпенсированный алкалоз.
Газовые расстройства кислотно-щелочного равновесия
Газовые (респираторные) расстройства КЩР характеризуются первичным изменением содержания в организме CO2 и, как следствие, - концентрации угольной кислоты в соотношении: [HCO3-]/[H2CO3]. Угольная кислота диссоциирует с образованием H+. При газовом ацидозе концентрация угольной кислоты увеличивается, при газовом алкалозе - уменьшается.Респираторный ацидоз характеризуется снижением pH крови и гиперкапнией (повышением рСО2 крови более 40 мм рт.ст.). Причина: гиповентиляция лёгких (например, при спазме бронхиол или обтурации дыхательных путей).
У большинства раненых развивается анемия, пропорциональная объему кровопотери. Несмотря на возмещение кровопотери, она нарастает, достигая максимальной выраженности на 3-5-е сутки. Содержание эритроцитов, концентрация гемоглобина и величина гематокрита зависят не только от объема кровопотери, но и от патологического депонирования крови, перехода жидкости во внеклеточное пространство, характера и темпов инфузионно-трансфузионной терапии, объема и скорости диуреза. Даже при благоприятном течении анемия сохраняется до 3-х недель и более после ранения.
Уже в первые часы после травмы увеличивается число лейкоцитов и содержание их молодых форм. К 3-м суткам количество лейкоцитов несколько снижается, а к 5-7 суткам возрастает вновь, особенно при осложненном течении травматической болезни. Выявлены значительные изменения в иммунной системе, которые являются проявлением общего адаптационного синдрома при травме. Установлена подавляющая роль повышенной активности гормональной системы, а также промежуточных продуктов метаболизма на иммунный ответ.
Практически у всех пострадавших в ранний период травматической болезни наблюдается снижение в крови как относительного, так и абсолютного количества лимфоцитов, СD 33 и СD 19-лимфоцитов, с тенденцией к увеличению относительного количества СD 22 R- лимфоцитов. Выраженные изменения обнаружены среди показателей гуморального иммунитета. Степень иммунологической депрессии зависела от тяжести травмы и величины кровопотери.