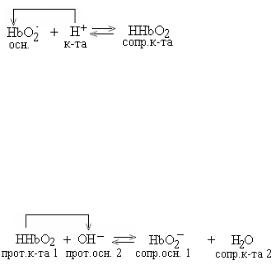
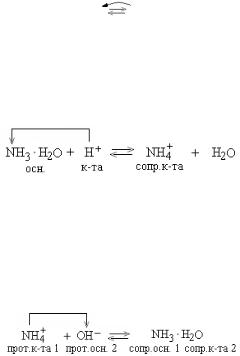
35. Аммиачная буферная система относится к буферным системам II типа. Запишем механизм буферного действия:
NH3 H2O NH4Cl
добавим постороннюю сильную кислоту НС1. Ее нейтрализует соль буфера:
NH |
H |
O HCl NH |
Cl H |
O |
3 |
2 |
4 |
2 |
|
Чем больше в буфере основания, тем больше посторонней сильной кислоты можно нейтрализовать, тем больше буферная
емкость по кислоте: |
Вк . |
|
|
|
ν |
о |
добавим постороннее сильное основание NaOH. Его нейтрализует кислота буфера:
NH |
Cl NaOH NH |
H |
O NaCl |
4 |
3 |
2 |
|
Чем больше в буфере соли, тем больше постороннего сильного основания можно нейтрализовать, тем больше буферная
. В данной буферной системе
буферная емкость по кислоте больше:
какой компонент буферной системы
характеризует и поставим знак > :
буферную емкость
, значит, в буфере
основания было больше, т.е. буферное отношение с / o 1.