Материал: Общая физика_под ред. Белокопытова_2016 -506с

количество теплоты на самом деле передается от рабочего тела). Если переписать последнее соотношение в виде
Q1 / T1 + Q2 / T2 = 0, |
(11.12) |
то его можно сформулировать следующим образом: в равновесном обратимом цикле Карно суммарная приведенная теплота всех процессов равна 0.
Рассмотрим произвольный обратимый цикл А-В-А (рис. 11.5). Разобьем этот цикл изотермами и адиабатами так, чтобы исходный цикл превратился в последовательность элементарных циклов Карно 1-2-3-4. Естественно, что чем ближе адиабаты 2-3 и 4-1 будут находиться одна к другой, тем точнее получится приближение последовательности циклов Карно к исходному циклу. Тогда можно сказать, что для осуществления исходного цикла потребуется множество нагревателей и холодильников. Для каждого из элементарных циклов Карно будет справедливо соотношение (11.12) в виде
δQ1i / T1i + δQ2i / T2 i = 0.
Если же просуммировать все эти выражения по исходному циклу, то получим
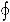 δQ / T = 0.
δQ / T = 0.
Математически это означает, что выражение δQ / T есть полный дифференциал некоторой функции S:
dS = δQ / T. |
(11.13) |
Такую функцию ввел и дал ей название энтропия (по-гречески «превращение») Р. Клаузиус в 1865 г.: это такая функция состояния термодинамической системы, дифференциал которой связан с элементарным тепловым эффектом в обратимом процессе соотношением (11.13).
p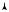
1 |
B |
|
|
|
2 |
A
43
0 |
V |
Рис. 11. 5
146
Выведем расчетную формулу для измерения энтропии в обратимом процессе идеального газа. Подставим выражение (11.13) в (10.3) и учтем (10.6):
T dS = dU + δA = dU + p dV .
Тогда, в соответствии с (8.9) и (10.5), получим:
dS = |
dU |
p |
i |
m |
dT |
m |
dV |
, |
------- |
+ ---- dV = |
---- |
---- R ------ |
+ --- |
R ------ |
|||
|
T |
T |
2 |
μ |
T |
μ |
V |
|
или после интегрирования для некоторого процесса 1-2
|
i |
m |
|
T2 |
|
m |
|
V2 |
|
S = |
---- |
---- |
R ln |
----- |
+ |
--- |
R ln |
----- |
|
2 |
μ |
T1 |
μ |
V1 . |
(11.14) |
Ясно, что если процесс круговой (цикл), то состояния 1 и 2 совпадают, т.е. T1 = T2 и V1 = V2 , а тогда
Sц = 0. |
(11.15) |
11.5.Основные свойства энтропии
1.Обратимый процесс. Рассмотрим цикл Карно как пример обратимого процесса, в котором участвуют три тела: нагреватель, рабочее тело и холодильник. Поскольку рабочее тело совершает замкнутый цикл, то для него справедливо (11.15), т.е. энтропия рабочего тела не изменяется. Следовательно, если Q1 / T1 — это измене-
ние энтропии в процессе теплообмена с нагревателем, то, согласно закону сохранения энергии, изменение энтропии нагревателя в этом процессе определится как – Q1 / T1. Аналогичный вывод можно сде-
лать и для второго слагаемого в (11.12). Тогда выражение (11.12) можно рассматривать и таким образом:
Sнагр + Sхол = 0.
Обобщая все выводы для рабочего тела, нагревателя и холодильника, получаем
Sсист = 0. |
(11.16) |
Таким образом, алгебраическая сумма изменений энтропии всех тел, участвующих в обратимом процессе, равна 0.
2. Необратимый процесс. Рассмотрим в качестве примера необратимого процесса передачу теплоты от одного (более горячего) тела, температура которого T1, к другому (более холодному) телу, темпера-
тура которого T2. Второе начало термодинамики утверждает, что про-
147
цесс возможен только в одном направлении: одно тело отдает количество теплоты Q1 , а другое получает количество теплоты Q2 .
Направление процесса передачи теплоты учитывается в знаке этих величин: Q1 < 0, а Q2 > 0. Согласно закону сохранения энергии
выполняется равенство Q1 = – Q2. Рассмотрим промежуточный этап
передачи столь малого количества теплоты, что температуры тел не изменяются. Изменения энтропии каждого из тел рассчитаем следующим образом: S1 = Q1 / T1, S2 = Q2 / T2 . Тогда общее изменение
энтропии системы из двух тел можно найти по формуле
Sсист = S1 + S2 |
= Q1 / T1 + Q2 / T2 . |
|
Учитывая, что T1 > T2, Q1 < 0, а Q2 |
> 0, получаем: |
|
Sсист > 0. |
(11.17) |
|
Таким образом, алгебраическая сумма изменений энтропии всех тел, участвующих в необратимом процессе, больше 0.
Объединяя выводы (11.16) и (11.17), получаем, что для всех тел изолированной системы, участвующих в произвольном процессе,
суммарное изменение энтропии неотрицательно: |
|
Sсист ≥ 0. |
(11.18) |
Этот вывод можно сформулировать несколько иначе: процессы в природе всегда идут в таком направлении, чтобы для всех тел, участвующих в процессе, алгебраическая сумма изменений энтропии была неотрицательна. Это правило, указывающее направление протекания любых процессов, также является формулировкой второго начала термодинамики.
Реальные процессы, происходящие в природе, всегда необратимы. Значит, энтропия системы в этих процессах должна возрастать. Рост энтропии продолжается до тех пор, пока в системе не наступит состояние равновесия, после чего все процессы в системе прекращаются. Другой вид приведенной формулировки может звучать и таким образом: не может самопроизвольно происходить процесс с уменьшением энтропии системы.
Распространение второго начала термодинамики, установленного для замкнутых систем, на всю Вселенную неправомерно. Такая экстраполяция может привести к выводу о неизбежности выравнивания температуры всех тел, к идее «тепловой смерти Вселенной» (ее выдвинул Р. Клаузиус). Согласно гипотезе Л. Больцмана, Вселенная все время пребывает в равновесном изотермическом состоянии,
148
но в ее различных частях происходят отклонения от этого состояния. Оказалось, что вследствие тяготения однородное изотермическое распределение вещества во Вселенной не соответствует максимуму энтропии, потому что не является наиболее вероятным. Поскольку Вселенная нестационарна, она расширяется и первоначально однородное вещество распадается под действием сил тяготения на галактики, звезды, планеты и т.д. Именно эти процессы и происходят с ростом энтропии, что полностью соответствует второму началу термодинамики. Эти процессы и позволят избежать «тепловой смерти Вселенной».
11.6. Статистический смысл второго начала термодинамики
До сих пор мы использовали термодинамический метод исследования и не интересовались внутренним строением изучаемых систем. Однако существует связь второго начала термодинамики с моле- кулярно-кинетической теорией строения вещества. Рассмотрим это на примере состояния системы молекул газа.
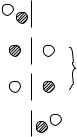
Каждому состоянию газа соответствует некоторое распределение его молекул по объему и определенное распределение молекул по скоростям. Предположим, что в сосуде находятся только две молекулы газа (рис. 11.6). «Цвет» молекул пусть будет соответствовать их скорости. Различные состояния газа различаются только распределением молекул по половинкам сосуда. Можно получить четыре различных распределения молекул. Вероятность каждого из них равна 0,25. Однако эта вероятность будет отличаться от вероятности термодинамического состояния системы. Дело в том, что в однородном газе все молекулы тождественны одна другой, т.е. они неразличимы. Поэтому два из четырех распределений будут тождественны одно
|
|
другому и определят одно из трех возможных |
|
|
|
состояний. Следовательно, вероятность состояния |
|
|
I |
II равна 0,5. |
|
|
|
В целом же вероятность какого-либо состояния |
|
|
|
||
|
|
системы W больше вероятности w отдельного рас- |
|
|
II |
пределения в P раз: |
|
|
|
||
|
|
|
|
|
|
W = wP, |
(11.19) |
|
|
где Р — термодинамическая вероятность |
|
|
|
||
|
III |
состояния системы. Она равна числу всевоз- |
|
|
|
можных микрораспределений частиц по коорди- |
|
|
|
||
Рис. 11. 6 |
натам и скоростям, соответствующих |
данному |
|
149
термодинамическому состоянию (макросостоянию). Необходимо учесть, что W ≤ 1, w ≤ 1, но P ≥ 1. В нашем примере PI = 1, PII = 2,
PIII = 1.
Л. Больцман доказал, что между энтропией системы и термодина-
мической вероятностью ее состояния существует связь: |
|
S = k ln P, |
(11.20) |
где k — постоянная Больцмана. Эта формула позволяет дать статистическое толкование второго закона термодинамики, утверждающего, что энтропия изолированной системы не убывает: термодинамическая вероятность состояния изолированной системы во всех происходящих в ней процессах не может убывать.
Таким образом, второй закон термодинамики является статистическим законом. Он выражает необходимые закономерности хаотического движения большого числа частиц, входящих в состав изолированной системы.
150