Материал: Общая физика_под ред. Белокопытова_2016 -506с

Г л а в а 12
ЯВЛЕНИЯ ПЕРЕНОСА В ГАЗАХ
В § 8.2 было введено понятие равновесного состояния термодинамической системы. Одно из условий такого состояния — отсутствие в системе потоков вещества и энергии. Однако беспорядочное тепловое движение молекул газа и столкновения между ними приводят к постоянному перемешиванию частиц и изменению их скоростей и энергий. Например, если в системе существует неоднородное распределение плотности или температуры, то происходит самопроизвольное выравнивание этих неоднородностей. Следовательно, при нарушении равновесного состояния системы она возвращается в это состояние. Поведение системы при этом можно описать, рассмотрев потоки массы, импульса, энергии и т.п. Подобные явления, происходящие при нарушении равновесного состояния систем, называются явлениями переноса. Рассмотрим некоторые из них.
12.1. Столкновения молекул
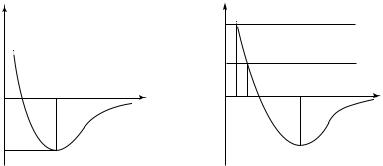
Наличие сил взаимодействия (отталкивания и притяжения) между молекулами приводит к появлению потенциальной энергии их взаимодействия. График зависимости потенциальной энергии от расстояния между молекулами приведен на рис. 12.1. Существование вещества в том или ином агрегатном состоянии при определенной температуре Т можно объяснить, сравнив глубину «потенциальной ямы» |U0 | и среднюю энергию хаотичного движения молекул, кото-
рая пропорциональна kT.
При выполнении неравенства |U0 | >> kT, т.е. при низких темпера-
турах вещества, молекулы располагаются близко одна от другой в строгом порядке. В этом случае тепловое движение молекул — это просто малые колебания молекул относительно положения равновесия. Вещество находится в твердом агрегатном состоянии. При |U0 | ≈ kT молекулы вещества непрерывно перемещаются по всему
его объему, однако расстояния между ними не превышают r0. Вещество находится в жидком агрегатном состоянии. При |U0 | << kT
в веществе наблюдается интенсивное хаотичное тепловое движение молекул. Молекулы удалены на значительные расстояния. Вещество находится в газообразном состоянии, а его молекулы непрерывно
151
U |
п |
Uп |
|
|
|
|
U2 |
|
|
|
|
|
|
|
|
|
|
|
|
U1 |
|
|
|
|
r0 |
0 |
|
|
r0 |
0 |
r2 |
r1 |
r |
||
|
r |
|
|||
U0 |
|
|
|
|
|
|
Рис. 12. 1 |
|
|
|
Рис. 12. 2 |
хаотично движутся и постоянно сталкиваются. Однако следует иметь в виду, что непосредственного «контакта» молекул при столкновениях не происходит. Объясняется это существенным увеличением сил отталкивания молекул при их сближении. Поэтому столкновением молекул будем называть такое их взаимодействие, при котором изменяются направления их движения. Процесс столкновения молекул тоже можно рассмотреть с помощью потенциальной кривой.
На график Uп ( r ) (рис. 12.2) нанесены значения полной энергии
системы двух молекул U. Поскольку силы взаимодействия молекул потенциальны, то, согласно закону сохранения механической энергии, U = const. Рассмотрим сближение молекулы 2 из положения r = = × с молекулой 1, неподвижно находящейся в положении r = 0.
Поскольку Uп ( ×) = 0, то кинетическая энергия молекулы 2 на
большом удалении молекул одной от другой равна полной энергии: Uк ( ×) = U. По мере сближения молекул кинетическая энергия моле-
кулы 2 растет, а Uп(r) падает. При расстоянии между молекулами r = r0 энергия Uк достигает максимального значения. За счет запаса этой энергии молекула 2 «пролетает» положение r = r0 и попадает в зону
преобладания действия сил отталкивания молекул. Следовательно, при дальнейшем сближении молекул (r < r0) кинетическая энергия
молекулы 2 падает, а потенциальная энергия Uп ( r ) растет.
Вточке r = r1 полная энергия системы равна потенциальной: U1 =
=Uп ( r1). В этом положении Uк(r1) = 0. Именно это положение и соот-
ветствует наибольшему сближению молекул. Поскольку при увеличении температуры системы значение U возрастает (U2 > U1), то расстоя-
ние наибольшего сближения молекул становится меньше (r2 < r1). Как оценить расстояние наибольшего сближения молекул?
152

Назовем |
эффективным диаметром |
|
2R |
|||||||
молекулы среднее расстояние между цент- |
|
|||||||||
|
||||||||||
|
|
|
|
|||||||
рами молекул, на |
которое |
две |
молекулы R |
|
|
эф |
|
|||
|
|
|
||||||||
|
|
|||||||||
сближаются |
при |
их |
столкновении |
|
|
2D |
|
|||
|
||||||||||
|
|
|
|
|||||||
(рис. 12.3). О необходимости введения такой |
|
|
|
|
||||||
|
|
|
|
|||||||
|
|
|
|
|||||||
величины говорилось в § 8.5. Площадь |
|
|
|
|
||||||
поперечного сечения «коридора», в который |
|
|
|
|
||||||
должны попасть центры соседних молекул, |
|
Рис. 12. 3 |
||||||||
|
|
|
|
|||||||
чтобы столкнуться с данной, называется |
|
|
|
|
||||||
эффективным сечением столкновения: |
|
|
|
|
||||||
|
|
S |
эф |
= πD2 |
|
= 4πR2 . |
(12.1) |
|||
|
|
|
эф |
|
|
|
|
|
||
Рассчитаем число столкновений молекул за единицу времени. Пусть одна молекула в сосуде движется со скоростью v , а остальные неподвижны. Тогда исследуемая молекула за 1 с испытает соударения со всеми частицами, находящимися в цилиндре длиной v æ1 с и основанием Sэф (рис. 12.3). Число таких молекул, а значит, и число столкновений будет равно:
N = n v Sэф .
Поскольку все столкновения произошли за 1 с, то промежутки времени между столкновениями равны
τ = |
1 |
|
1 |
----- |
|
---------------------- |
|
N |
= |
n v Sэф . |
Назовем средней длиной свободного пробега молекулы расстояние, которое она пролетает между двумя последовательными соударениями:
l |
= |
|
τ = |
1 |
|
v |
------------ |
|
|||
|
n Sэф . |
(12.2) |
Однако мы полагали, что все молекулы системы неподвижны, а движется только одна. Необходимо учесть движение всех молекул, т.е. рассматривая ту же задачу в системе отсчета, связанной с движущейся молекулой, нужно заменить скорость v на относительную скорость движения молекул. Поскольку все направления относительного движения молекул равновероятны, то угол между направлениями скоростей молекул лежит в диапазоне 0 — π, а средний угол равен π / 2. Тогда модуль относительной скорости движения молекул
в соответствии с (1.18) определится как 
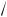 2 v . С учетом этого замечания и формулы (12.1) можно записать выражение (12.2) в виде
2 v . С учетом этого замечания и формулы (12.1) можно записать выражение (12.2) в виде
l = |
1 |
|
|
1 |
|
--------------------- |
|
-------------------------- |
|
||
2 nS |
эф |
= |
4 2 nπR2 . |
(12.3) |
|
|
|
|
|
|
|
153
l
L
0 |
pпр |
p |
Рис. 12. 4
Как известно, в идеальном газе справедливо уравнение состояния в виде соотношения (8.11). Тогда (12.3) перепишем следующим образом:
l |
1 |
|
kT |
(12.4) |
= ------------------- |
= ------------------------ . |
|||
|
2 nS |
эф |
4 2 pπR2 |
|
|
|
|
|
|
Оценим среднюю длину свободного пробега молекулы азота при температуре T = 300 К и давлении p = 105 Па. Принимая во внимание,
° |
= 10 |
– 10 |
м, получаем согласно (12.4) l |
= 2æ10 |
– 7 |
м. |
что R ≈ 1 A |
|
|
||||
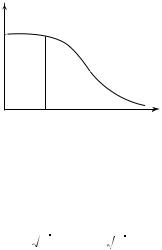
График зависимости средней длины свободного пробега |
l от |
|||||
давления газа р при постоянной температуре изображен на рис. 12.4. При его построении учтено, что если давление газа снижается ниже давления предельно достижимого вакуума рпр, то значение l соот-
ветствует характерному размеру сосуда L, т.е. молекулы будут пролетать весь сосуд без соударения однa с другой.
В соответствии с (12.4) средняя длина свободного пробега l не должна зависеть от температуры газа Т. Однако экспериментально подтверждено, что она слабо растет с увеличением температуры. Происходит это из-за того, что с ростом температуры уменьшается значение R. На рис. 12.2 показано, что расстояние наибольшего сближения молекул уменьшается с увеличением запаса полной энергии системы молекул, т.е. с увеличением температуры: r2 < r1.
12.2. Диффузия
Рассмотрим неравновесное состояние системы молекул, вызванное нарушением равномерного распределения концентрации молекул по объему системы. При этом система может состоять как из молекул одного вещества (одинаковые молекулы), так и из молекул разных веществ (смесь разных молекул). Опыт показывает, что в однофазной системе молекул при постоянной температуре и отсутствии внешних
154
сил происходит выравнивание концентра- |
v t |
v t |
|
||||
ции каждого компонента по всему объему |
|
|
|
||||
системы. Неравновесный процесс, вызыва- |
|
S |
|
||||
емый молекулярным тепловым движением |
|
|
|||||
|
|
|
|||||
и приводящий к установлению равновес- |
n1 |
n2 |
|
||||
ного распределения концентраций путем |
|
||||||
взаимопроникновения |
и |
перемешивания |
O |
x0 |
X |
||
молекул, |
называется |
диффузией. Диф- |
|
|
|
||
фузия — один из процессов переноса. |
Рис. 12. 5 |
|
|||||
|
|
|
|||||
Поскольку в этом процессе рассматрива- |
|
|
|
||||
ется перемещение молекул по объему системы, то диффузия — это |
|||||||
перенос массы. Диффундировать могут и молекулы примесей (компо- |
|||||||
нентов смеси), и молекулы однокомпонентной системы. Диффузия — |
|||||||
необратимый процесс, один из источников диссипации (рассеяния) |
|||||||
энергии в системе. |
|
|
|
|
|
|
|
Выведем уравнение, позволяющее количественно описать про- |
|||||||
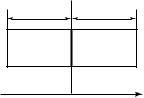
цесс диффузии. Пусть в направлении оси ОХ установилось неравно- |
|||||||
мерное распределение концентрации молекул (рис. 12.5). Выделим |
|||||||
при x = x0 элемент поверхности S, слева от которого концентрация |
|||||||
молекул п1, а справа — п2. Подсчитаем поток частиц, т.е. число |
|||||||
молекул, проходящих в единицу времени через этот элемент поверх- |
|||||||
|
|
|
|
|
º |
направлена |
|
ности. Если средняя скорость движения молекул v |
|||||||
вдоль оси ОХ, то за время t все молекулы, находящиеся слева от |
|||||||
этого сечения, из объема S v |
t уйдут вправо. Число таких молекул |
||||||
n1S v t . Аналогично из такого же объема, находящегося справа от |
|||||||
сечения, за время t все молекулы уйдут влево. Число таких молекул |
|||||||
n2S v |
t . Назовем плотностью потока молекул их число, прохо- |
||||||
дящее через единичное сечение, расположенное перпендикулярно |
|||||||
вектору скорости, за единицу времени: |
|
|
|
||||
Φ = |
N |
|
(12.5) |
--------- . |
|||
|
S |
t |
|
Тогда поток частиц слева направо |
N1 = n1 v S , а поток |
частиц |
|
справа налево N2 = n2 v S . Поскольку эти потоки частиц идут в
разных направлениях, то общий поток в положительном направлении оси ОХ будет определяться их разностью.
Необходимо учесть, что движение молекул вдоль выбранного направления можно рассматривать прямолинейным, если за время t скорость молекул не меняет своего направления. Это возможно, если молекулы пересекают сечение S без столкновений. Следовательно,
155