Материал: Общая физика_под ред. Белокопытова_2016 -506с
В изохорном процессе объем газа не изменяется, поэтому p dV = 0 и δQ = dU. Получаем выражение для молярной теплоемкости идеального газа в изохорном процессе, которую обозначим cV :
i
cV = ---- R . 2
Тогда внутренняя энергия идеального газа может определена по формуле
m
U = ---- cVT .
μ
(10.8)
быть также
(10.9)
В изобарном процессе изменения объема газ совершает работу и тогда выражение для молярной теплоемкости идеального газа в изобарном процессе, которую обозначим cp , приобретает вид:
|
i |
dV |
cp = |
---- |
------ |
2 |
R + p dT . |
Воспользуемся теперь уравнением Менделеева—Клапейрона для 1 моля газа (8.8), выразив элементарную работу газа в изобарном процессе как p dV = R dT. Тогда
|
i |
i + 2 |
|
|
cp = |
---- |
----------- |
R . |
(10.10) |
2 R + R = |
2 |
|||
Нетрудно видеть, что соблюдается соотношение |
|
|||
|
cp = cV + R, |
|
(10.11) |
|
которое было впервые получено Р. Майером в 1842 г. и поэтому называется уравнением Майера.
В изотермическом процессе газ не изменяет свою температуру, поэтому dT = 0. Однако газ расширяется, следовательно, он совершает работу: δA ≠ 0. Тогда молярная теплоемкость идеального газа в изотермическом процессе
|
i |
dV |
= ± |
|
|
cT = |
---- |
------ |
× |
. |
|
2 |
R + p dT |
|
Во всех рассмотренных изопроцессах молярные теплоемкости идеального газа постоянны и зависят только от внутреннего строения его молекул. Процесс, в котором теплоемкость вещества не изменяется, называется политропным. Получим уравнение такого процесса для идеального газа. Используем выражение первого начала термодинамики:
cmν dT = |
i |
νRdT + p dV , |
---- |
||
2 |
гдеν = m ⁄ μ .
131
Из уравнения (8.9) следует, что p dV + V dp = νR dT . Тогда
|
p dV + V dp |
|
p dV + V dp |
|
cm |
------------------------------- |
= cV |
------------------------------- |
+ p dV , |
R |
R |
или
p dV(cm – cV – R) = V dp(cV – cm) . Воспользуемся (10.11) и последнее выражение перепишем в виде
p dV(cm – cp) = V dp(cV – cm) .
Полученное дифференциальное уравнение можно решить методом разделения переменных:
dV |
cm – cp |
dp |
------ |
------------------- = |
----- . |
V |
cV – cm |
p |
Обозначим
n = |
cm – cp |
(10.12) |
------------------- , |
||
|
cm – cV |
|
тогда |
|
|
n ln V = – ln p + const , |
|
|
или |
|
|
pV n = const . |
(10.13) |
|
Полученное соотношение является уравнением политропного процесса, в котором теплоемкость газа остается постоянной величиной. Показатель n, определяемый по (10.12), называется показателем политропы для данного газа. Если из (10.12) выразить молярную теплоемкость газа cm в политропном процессе, то найдем:
c |
|
= c |
|
n – (cp ⁄ cV ) |
= c |
|
m |
V |
------------------------------- |
V |
|||
|
|
n – 1 |
|
где
γ = cp ⁄ cV .
n – γ |
, |
(10.14) |
------------ |
||
n – 1 |
|
|
(10.15)
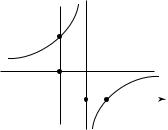
Формальная зависимость теплоемкости газа в политропном процессе от показателя политропы изображен на рис. 10.3. Нетрудно
видеть, что при n = 0 из уравнения (10.13) следует pV n = pV 0 = p = = const, т.е. уравнение изобарного процесса. В соответствии с (10.14),
cm = cp. При n = 1 из уравнения (10.13) получаем pV n = pV 1= pV = const,
т.е. уравнение изотермического процесса. В этом случае, в соответствии с (10.14), cm → ±×. При n = ±× из уравнения (10.13), извлекая корень
п-й степени, можно получить n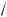 p V = V = const , т.е. уравнение изо-
p V = V = const , т.е. уравнение изо-
132
cm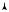
cp
cV
0 |
1 |
|
n |
Рис. 10. 3
хорного процесса. Согласно (10.14), cm = cV . Следовательно, все изопроцессы идеального газа — частные случаи политропного процесса.
Кроме известных изопроцессов можно ввести понятие адиабатического процесса. Адиабатическим (или адиабатным) процессом
называют процесс, который проходит без теплообмена с окружающей средой (δQ = 0). Тогда в этом процессе cm = 0, и из (10.14) можно
получить, что это возможно при n = γ. Уравнение адиабатного про-
цесса имеет вид: pV γ = const. Это уравнение впервые было получено французским математиком и механиком С. Пуассоном и поэтому называется уравнением Пуассона. Показатель степени в этом уравнении называется показателем Пуассона для идеального газа. Нетрудно увидеть, что, согласно (10.8) и (10.10), из (10.15) следует
γ = cp ⁄ cV = (i + 2) ⁄ i . |
(10.16) |
10.4.Анализ изопроцессов идеального газа
спомощью первого начала термодинамики
Рассмотрим описание различных изопроцессов идеального газа с помощью первого начала термодинамики.
Изохорный процесс. Поскольку в этом процессе V = const, то газ не совершает никакой работы над внешними телами: AV = 0. В соот-
ветствии с первым началом термодинамики QV = U . Используя
уравнение Клапейрона — Менделеева, можно выразить изменение внутренней энергии идеального газа следующим образом:
i m i
U = ---- --- R T = ---- V p. 2 μ 2
Подводимое к |
газу количество теплоты можно рассчитать, |
|||
использовав (10.8) |
так: |
|
|
|
|
|
m |
|
|
|
QV = |
--- |
cV |
T . |
|
μ |
|||
133
Изобарный процесс. В данном процессе происходит изменение объема газа, поэтому он совершает работу над внешними силами.
|
m |
|
|
Поскольку p = const то, согласно (10.6), Ap = p V = |
--- |
R T . Из этого |
|
μ |
|||
|
|
выражения следует физический смысл универсальной газовой постоянной: она численно равна работе изобарного расширения 1 моля идеального газа при повышении его температуры на 1 К. Уравнение первого начала термодинамики для изобарного процесса запишем следующим образом: δQp = dU + δAp , или Qp = U + Ap . Исполь-
зуя уравнение Клапейрона — Менделеева, выражаем изменение внутренней энергии идеального газа следующим образом:
i m i
U = ---- --- R T = ---- p V . 2 μ 2
Подводимое к газу количество теплоты определяется с помощью (10.10) так:
|
m |
|
|
Qp = |
--- |
cp |
T . |
μ |
Изотермический процесс. Поскольку в этом процессе T = const, то внутренняя энергия идеального газа не изменяется: U = 0. Уравнение первого начала термодинамики для такого процесса запишем в виде δQT = δAT , или QT = AT . Следовательно, при подведении к
газу теплоты (QT > 0), он расширяется, совершая положительную
работу против внешних сил (A > 0). Получим выражение для расчета работы газа в изотермическом процессе, проинтегрировав (10.6):
V2 |
V2 |
m RT |
|
||
AT = ∫ |
p dV = ∫ |
|
|||
--- ------ |
dV = |
||||
μ |
V |
||||
V1 |
V1 |
|
|||
|
|
|
|||
m |
|
V2 |
|
m |
p1 |
p1 |
--- |
RT |
ln ----- |
= |
--- |
RT ln ----- |
= p1V1 ln ----- . |
μ |
|
V1 |
|
μ |
p2 |
p2 |
Поскольку в данном процессе теплоемкость бесконечна, то для расчета подведенного к газу количества теплоты можно использовать лишь выражение первого начала термодинамики. Основной вывод при анализе превращения энергии в изотермическом процессе: получаемая от внешней среды теплота идет не на увеличение температуры газа, а возвращается обратно в среду в виде механической работы.
Адиабатный процесс. В таком процессе газ не получает теплоты из внешней среды: δQад = 0 , поэтому 0 = dU + δAад . Поэтому при
расширении газа, когда он совершает положительную работу против внешних сил (A > 0), изменение внутренней энергии газа отрицательно ( U < 0). Следовательно, согласно (10.5), температура газа
134
p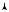
Адиабата
Изотерма
0 |
V |
Рис. 10. 4
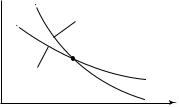
уменьшается. Поэтому на диаграмме ( p,V ) кривая адиабатического расширения газа (адиабата) будет располагаться ниже кривой изотермического расширения (изотермы), проведенной из той же начальной точки (рис. 10.4). Таким образом, адиабата на диаграмме ( p,V ) проходит круче, чем изотерма. В соответствии с (10.7) cад = 0, а поэтому
расчет совершенной газом работы можно провести в соответствии с первым началом термодинамики: Aад = – U. Однако можно полу-
чить выражение для расчета работы в адиабатном процессе и с помощью соотношения (10.6). Для этого воспользуемся уравнением Пуас-
сона pV γ = p1V1γ = const . Тогда
V2 |
V2 |
p |
|
V |
γ |
|
p |
|
V |
γ |
|
|
|
|
|
|
Aад = ∫ |
p dV = ∫ |
|
1 |
|
|
1 |
|
|
1 |
|
1 |
|
1 – γ |
1 – γ |
|
|
------------ |
dV = |
------------ |
|
V2 |
– V1 |
|
. |
|||||||||
|
V |
γ |
|
1 – |
γ |
|
|
|||||||||
V1 |
V1 |
|
|
|
|
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
Поскольку γ > 1, то последнее выражение удобно переписать в виде
|
|
p |
1 |
Vγ |
|
|
1 – γ |
|
1 – γ |
|
|
p |
1 |
V |
1 |
|
V γ – 1 |
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
A |
|
|
1 |
|
V |
– V |
|
= |
|
|
1 |
|
. |
||||||
ад |
= ------------ |
|
1 |
2 |
|
------------ |
|
1 – ----- |
|
||||||||||
|
γ |
– 1 |
|
|
|
|
|
γ |
– 1 |
|
V2 |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Отметим, что в соответствии с (10.16) показатель адиабаты может принимать следующие значения:
γ= 5 ⁄ 3 ≈ 1,67 для одноатомного газа (i = 3);
γ= 7 ⁄ 5 = 1,4 для двухатомного газа (i = 5);
γ= 4 ⁄ 3 ≈ 1,33 для трехатомного газа (i = 6).
Реальный адиабатный процесс должен происходить, с одной стороны, достаточно быстро, чтобы в системе не успел произойти теплообмен с окружающей средой, но, с другой стороны, достаточно медленно, чтобы процесс оставался равновесным.
135