Материал: Общая физика_под ред. Белокопытова_2016 -506с
9.4. Барометрическая формула
Распределение Максвелла — это распределение молекул по скоростям, или по кинетическим энергиям. Действительно, в показателе экспоненты в (9.11) стоит отношение кинетической энергии молекулы к kT. Произведение постоянной Больцмана и температуры характеризует среднюю кинетическую энергию движения молекул, т.е. энергию их теплового движения.
Установим теперь распределение молекул по потенциальным энергиям. Л. Больцман получил барометрическую формулу — зависимость давления газа от высоты в потенциальном поле тяжести Земли.
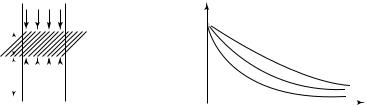
Рассмотрим равновесие некоторого объема газа, находящегося на высоте h от поверхности Земли, уровень которой выберем за условный ноль отсчета потенциальной энергии (рис. 9.6). Атмосферное давление на данном уровне обозначим как p0. Пусть объем газа — это цилиндр
высотой dh. На рис. 9.6 указаны давления, действующие на рассмотренный газовый цилиндр со стороны выше- и нижележащих слоев атмосферы. Поскольку столбик газа находится в равновесии, то
(p + d p)S + dmg – pS = 0 ,
где S — площадь основания столбика; d m — его масса.
Выразив массу объема газа через его плотность как d m = ρS dh,
получим дифференциальное уравнение |
|
ρSg dh + dpS = 0 . |
(9.17) |
Плотность газа, в соответствии с уравнением состояния идеаль-
ного газа, определяется как |
|
m |
= |
pμ |
, тогда уравнение (9.17) |
ρ = ----- |
------ |
||||
|
|
V |
|
RT |
|
запишется в виде |
|
|
|
|
|
|
|
pμ |
|
|
|
dp |
= – |
------ |
|
|
|
RT g dh . |
|
||||
Знак «—» в этом уравнении показывает, что давление газа уменьшается с ростом высоты слоя от поверхности Земли. Разделим пере-
p+dp
p
T1 < T2 < T3
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
dh |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
1 |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
h |
|
|
|
|
|
|
|
|
|
2 |
|
||
|
|
|
p |
p = p0; |
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Wп = 0 |
0 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
h |
|||
|
|
|
|
|
Рис. 9. 6 |
|
|
|
Рис. 9. 7 |
|||||
121
менные в уравнении: |
dp |
|
μg |
dh , а потом проинтегрируем левую |
|||||||
----- |
= – ------ |
||||||||||
|
|
|
|
p |
|
RT |
|
|
|
|
|
и правую части: |
|
|
|
|
|
|
|
|
|
||
p |
|
h |
μg |
|
|
|
|
|
|
|
μgh |
dp |
|
|
p |
|
|
μgh |
|
– ---------- |
|||
∫ |
= –∫ |
dh ; |
|
= – |
; |
p = p0e RT . |
|||||
----- |
------ |
ln ----- |
--------- |
||||||||
p0 |
p |
0 |
RT |
|
|
p0 |
|
RT |
|
|
|
|
|
|
|
|
|
||||||
Так как μ / R = m0 / k, а m0gh = Wп , то последнее выражение перепишем следующим образом:
|
|
Wп |
|
|
|
– ------- |
|
p = p |
0 |
e kT . |
(9.18) |
|
|
|
Полученное соотношение и есть барометрическая формула, которая определяет зависимость давления идеального газа от потенциальной энергии его молекул (от высоты). Поскольку p = nkT, то ее можно записать в виде
|
|
Wп |
|
|
|
– ------- |
|
n = n |
0 |
e kT . |
(9.19) |
|
|
|
Уравнение (9.19) — это распределение концентрации молекул в зависимости от их потенциальной энергии. Из него следует, что наибольшая концентрация молекул там, где Wп = 0, т.е. вблизи
поверхности Земли. График зависимости (9.18) представлен на рис. 9.7.
Справедливость установленного Л. Больцманом закона для земной атмосферы не могла быть проверена в XIX в.: для изменения
|
|
|
Wп |
|
|
атмосферного давления в е раз |
т.е. |
------- |
необходимо подняться |
||
|
kT |
= 1 |
над уровнем Земли на высоту примерно 9 км.
9.5. Распределение энергии молекулы по степеням свободы
Механическая энергия любой молекулы идеального газа — это кинетическая энергия ее движения, так как потенциальное взаимодействие между такими молекулами отсутствует. Энергия движения молекулы определяется, в свою очередь, энергией ее поступательного движения, энергией ее вращения и энергией колебания атомов в молекуле:
Wк = Wпост + Wвращ + Wкол .
122

|
Будем |
рассматривать |
в |
дальнейшем |
Z |
|
только «жесткие» молекулы, атомы в кото- |
|
i = iпост |
||||
рых не совершают колебаний, т.е. Wкол = 0. |
|
|||||
|
i = 3 |
|||||
Ранее (см. § 9.2) определено, что Wк = |
|
|||||
|
|
|||||
|
m0v 2 |
3 |
|
|
O |
Y |
= |
------------- |
---- |
выражение было |
|
|
|
2 |
= 2 kT . Это |
X |
|
|||
|
|
|
|
|
|
|
получено для системы молекул, которые представлялись в виде шариков, упруго соударяющихся один с другим. Такие шарики
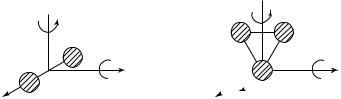
двигались поступательно вдоль любого из направлений трехмерной декартовой системы координат. Положение такой молекулы в пространстве определяется набором трех независимых переменных — координат центра масс шара x, y, z (рис. 9.8). Можно сказать, что шарообразная молекула способна совершать в пространстве три независимых перемещения. Вращением шара вокруг любого из его диаметров при этом можно пренебречь, так как поворот шара вокруг диаметра не изменяет его положения в пространстве.
Минимальное число независимых переменных, однозначно определяющих положение тела в пространстве (или минимальное число независимых перемещений тела в пространстве), называется числом степеней свободы тела. Из приведенных рассуждений ясно, что число степеней свободы шарообразной молекулы равно 3. В дальнейшем будем обозначать число степеней свободы через i. Ясно, что шарообразной молекулу можно считать, если она состоит из одного атома (He, Ar, Ne). Таким образом, для одноатомной молекулы i = 3.
Л. Больцман предположил, что кинетическая энергия молекулы равномерно распределена по степеням ее свободы, т.е. каждому независимому перемещению молекулы соответствует одна и та же энер-
гия. Поскольку для системы одноатомных молекул Wк = |
3 |
|
---- |
kT , |
|
2 |
а i = 3, то можно сделать вывод, что каждому из трех поступатель-
ных движений соответствует энергия εi = |
1 |
|
---- |
kT . Закон Больцмана |
|
2 |
о равномерном распределении энергии молекул по степеням свободы звучит следующим образом: если система молекул находится в тепловом равновесии при температуре Т, то средняя кинетическая энергия молекул равномерно распределена по степеням свободы, при-
чем на каждую степень свободы приходится энергия εi = |
1 |
|
---- |
kT . |
|
2 |
Какие выводы будут следовать из этого закона для неодноатомных молекул? Рассмотрим двухатомную молекулу (H2, O2, CO, N2),
123
Z 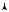
Z 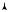
i = iпост + iвр i = 3 + 2 = 5
O 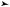 Y
Y 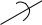 O
O
i = iпост + iвр i = 3 + 3 = 6
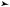 Y
Y
X |
X |
Рис. 9. 9 |
Рис. 9. 10 |
выбрав оси координат таким образом, чтобы одна из осей совпадала с продольной осью молекулы (рис. 9.9). Двухатомная молекула может совершать пять независимых перемещений в пространстве: три поступательных вдоль осей координат и два вращательных вокруг двух осей. Поворот молекулы вокруг третьей оси координат (оси ОХ на рис. 9.9) не приводит к изменению ее положения в пространстве. Таким образом, у двухатомной молекулы три поступательных степени свободы и две вращательных, в целом i = 5. Строение молекулы водяного пара (H2O) таково, что ее поведение в пространстве
соответствует поведению двухатомных молекул, поэтому для водяного пара i = 5.
Если рассмотреть трехатомную молекулу (рис. 9.10), то нетрудно установить, что у нее будет три поступательных степени свободы и три вращательных, в целом i = 6.
124

Г л а в а 10
ПЕРВОЕ НАЧАЛО ТЕРМОДИНАМИКИ
В основе термодинамического метода лежит несколько фундаментальных законов (начал), которые установлены на основании обобщения большой совокупности опытных фактов. Термодинамический метод основан на анализе превращения энергии в системе. При этом в термодинамике не рассматривается внутреннее строение систем и характер движения частиц в этих системах. Выводы термодинамики имеют весьма общий характер. Законы термодинамики можно применить к электрическим и магнитным явлениям, процессам теплового излучения, радиоактивного распада и т.п. Нет такой области физики, химии и биологии, в которой нельзя было бы пользоваться термодинамическим методом. Однако при этом термодинамика не вникает в процессы, происходящие внутри вещества, не рассматривает механизмы этих процессов.
10.1. Внутренняя энергия системы молекул. Работа в термодинамике. Количество теплоты
Полная энергия W термодинамической системы включает в себя кинетическую энергию Wксист механического движения системы как
целого, потенциальную энергию Wпвнеш системы во внешнем потен-
циальном поле и внутреннюю энергию U — энергию всех видов движения и взаимодействия частей системы, зависящую только от внутреннего строения системы. Таким образом,
W = Wксист + Wпвнеш + U.
Вдальнейшем будем рассматривать термодинамические системы, которые макроскопически неподвижны и не находятся во внешних полях. Для таких систем полная и внутренняя энергия совпадают.
Втермодинамике под внутренней энергией понимают лишь кинетическую энергию теплового движения молекул, потенциальную энергию взаимодействия атомов в молекуле, а также потенциальную энергию взаимодействия молекул между собой.
Внутренняя энергия является однозначной функцией состояния термодинамической системы. Это означает, что внутренняя энергия
125