Материал: Общая физика_под ред. Белокопытова_2016 -506с
Таким образом, найдено значение α: α = |
m0n |
. При тепловом рав- |
---------- |
||
|
2p |
|
новесии идеального газа справедливо уравнение его состояния p =
= nkT, поэтому |
α = |
m0n |
= |
m0 |
|
|
|
|
----------- |
-------- . |
|
|
|
||||
|
|
|
2nkT |
|
2kT |
|
|
|
Вернемся к выражению (9.6): |
|
|
|
|||||
|
|
|
|
|
|
3 |
|
2 |
|
|
3 |
2 |
|
|
|
m0v |
|
|
|
---- |
|
m0 |
---- |
– |
------------- |
|
α |
|
2 |
– αv |
|
2 |
|||
|
|
2kT 4πv 2 v . (9.9) |
||||||
P = ---- |
e |
|
æ4πv 2 v = ----------- |
|
e |
|||
π |
|
|
|
|
2πkT |
|
|
|
Полученное выражение позволяет определить вероятность того, что молекула имеет скорость в диапазоне v ÷ v + v. Такое распределение получено при следующих допущениях: все молекулы одинаковы; газ — идеальный, в отсутствиe силовых полей; в газе наблюдается состояние теплового равновесия (принцип детального равновесия). Рассматривая бесконечно малый диапазон скоростей, (9.9) можно записать следующим образом:
|
|
|
3 |
m |
|
2 |
|
|
|
|
|
v |
|
||
|
m |
|
---- |
|
0 |
|
|
|
0 |
2 |
– ------------- |
|
|||
dP = |
|
|
e 2kT 4πv 2 dv . |
(9.10) |
|||
----------- |
|
||||||
|
2πkT |
|
|
|
|
|
|
Тогда плотность вероятности попадания молекулы в интервал скоростей v ÷ v + dv составит:
|
|
|
|
3 |
m |
|
2 |
|
|
|
|
|
|
|
|
|
0 |
v |
|
|
|
|
|
||
|
|
|
|
-- |
|
|
|
|
|
|
|
|
|
|
|
m0 |
2 |
– ------------- |
|
|
|
|
|
||
f |
= |
2kT |
4 |
πv |
2 |
. |
(9.11) |
|||||
|
----------- |
e |
|
|
|
|
||||||
|
|
2πkT |
|
|
|
|
|
|
|
|
|
|
График распределения этой плотности вероятности представлен на рис. 9.2. Поскольку dP = f (v) dv, то площадь под элементом гра-
фика f (v) будет определять вероятность |
обнаружения молекулы |
со скоростью, значение которой лежит в |
интервале v ÷ v + dv |
(на рис. 9.2 эта площадь заштрихована). |
|
Условие (9.5) нормировки плотности вероятности f (v) |
|
× |
|
∫ f (v) dv = 1 |
(9.12) |
0
физически означает то, что всегда найдется молекула, скорость которой лежит в интервале 0 ÷ ×. С изменением температуры график распределения плотности вероятности изменяет свой вид. Например, на рис. 9.3 показано, что с увеличением температуры максимум функции становится менее выраженным и переходит в область бoльших′ скоростей. Это означает, что увеличивается доля молекул, обладающих большими скоростями.
116

f(v) |
|
|
|
|
f(v) |
T1 |
T |
2 |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
T3 > T2 > T1 |
|
|
|
|
|
|
|
|
|
T3 |
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
0 |
dv |
v |
0 |
|
|
|
v |
||
|
Рис. 9. 2 |
|
|
|
Рис. 9. 3 |
||||
Теперь по определению (9.1) запишем максвелловский закон распределения молекул газа по модулям скоростей, который определяет, какое число dN молекул газа из общего числа его молекул N в единице объема имеет при данной температуре скорости, заключенные в интервале от v до v + dv:
dN = N dP = N f (v) dv = N |
|
m0 |
|
|
----------- |
|
|
|
2πkT |
||
3 |
m |
|
2 |
|
v |
||
---- |
|
0 |
|
2 |
– ------------- |
||
e |
2kT 4πv 2 dv . (9.13) |
||
C помощью такого распределения можно, например, рассчитать среднюю кинетическую энергию системы молекул. Воспользуемся определением (9.3). Кинетическая энергия молекулы — это функция
ее скорости ϕ(z) = m0v 2 / 2, поэтому
|
|
|
|
|
|
3 |
|
m |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
v |
|
|
|
|
|
|
||
m0v 2 |
×m0v 2 |
×m0v 2 |
|
-- |
– |
|
|
|
|
|
|
|
|
|||
|
m0 2 |
-------------2kT |
4 |
πv |
2 |
dv = |
3 |
kT . |
||||||||
-------------2 |
= ∫ |
-------------2 |
f (v)dv = ∫ |
-------------2 |
|
----------- |
e |
|
|
|
|
2-- |
||||
0 |
0 |
2πkT |
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
9.3.Наиболее вероятная, средняя
исреднеквадратичная скорости молекул
Проанализируем поведение функции распределения молекул по скоростям. Найдем, при какой скорости наблюдается максимальное значение функции f (v). Такую скорость vв назовем наиболее вероят-
ной скоростью молекул. В единичном интервале скоростей вблизи vв будет находиться больше всего молекул. Для того чтобы найти vв,
продифференцируем выражение (9.11):
|
3 |
|
|
m |
|
2 |
|
m |
|
2 |
|
|
|
|
|
|
|
0 |
v |
|
0 |
v |
|
|
|
|
|||
|
-- |
|
2ve– |
|
|
+ v2e– |
|
|
|
|
|
|
||
f ′ = 4π |
-----------m0 2 |
|
-------------2 k T |
-------------2kT |
– |
-------------2vm0 |
. |
|||||||
|
2πkT |
|
|
|
|
|
|
|
|
|
|
2kT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
117

Приравняв полученную производную к 0, найдем значение vв :
2v |
|
v |
в3m0 |
= 0 |
v |
|
= |
в |
– ------------- |
в |
|||||
|
|
kT |
|
|
|
||
2kT |
(9.14) |
--------- . |
|
m0 |
|
Средняя арифметическая скорость всех молекул будет отличаться от vв , поскольку в соответствии с (9.2)
|
|
|
|
|
|
3 |
|
m |
|
2 |
|
|
|
|
|
|
|
|
|
|
0 |
v |
|
|
|
||
|
|
|
|
|
|
-- |
|
|
|
|
|
|
|
|
|
× |
|
× |
|
m0 2 |
|
– ------------- |
|
|
|
||
|
|
∫ |
|
∫ |
|
2kT æ |
3 |
8kT |
|||||
v |
= |
v f (v)dv = |
|
|
e |
|
|
|
4πv dv = |
---------- . (9.15) |
|||
|
|
|
----------- |
|
|
|
|||||||
|
|
0 |
|
0 |
|
2πkT |
|
|
|
|
|
πm |
0 |
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||
Очень часто в молекулярной физике используется понятие среднеквадратичной скорости молекул. Так называется скорость, равная квадратному корню из среднего значения квадрата скоростей
молекул vср.кв = 
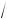 v2 . По определению (9.2) найдем
v2 . По определению (9.2) найдем
|
|
|
|
|
|
|
|
|
3 |
m |
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
0 |
v |
|
|
|
|
||
|
|
|
|
|
|
|
|
|
-- |
|
|
|
|
|
|
|
|
2 |
|
× |
|
2 |
× |
|
m0 |
2 |
– ------------- |
|
|
4 |
|
||
v |
|
= ∫ |
|
f (v)dv = ∫ |
2kT æ |
|
πv |
|
||||||||
|
v |
|
|
----------- |
e |
|
|
|
4 |
|
dv = |
|||||
|
|
|
0 |
|
|
0 |
2πkT |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
3kT
--------- . m0
Тогда
v |
ср.кв |
= v2 = 3kT ⁄ m |
0 |
. |
(9.16) |
|
|
|
|
Сравнивая (9.14), (9.15) и (9.16), отметим, что vв < v < vср.кв .
Эти скорости нанесены на график плотности вероятности на рис. 9.4. Рассматривая кривую плотности вероятности распределения
молекул по скоростям, можно сделать следующие выводы:
1.Функция распределения плотности вероятности (9.11) позволяет найти не число молекул, скорости которых лежат в определенном интервале скоростей, а только долю общего числа молекул.
2.Относительное число молекул (доля общего числа молекул),
обладающих скоростями в определенном интервале, зависит не
f(v) |
f(v) |
|
|
|
|
I |
|
II |
|
0 |
vв vср vср.кв |
v |
0 |
v |
v |
v |
|
Рис. 9. 4 |
|
|
Рис. 9. 5 |
|
|
118
только от размера интервала скоростей, но и от того, какому участку принадлежит данный интервал. Например, на рис. 9.5 видно, что при одном и том же размере интервала скоростей (его ширина составляет v) относительное число молекул, скорости которых попадают в интервал I, будет больше, чем относительное число молекул, скоро-
сти которых попали в интервал II.
3.Максвелловское распределение молекул по скоростям нельзя использовать для анализа систем молекул при очень высоких температурах. При таких температурах максимум кривой распределения резко «сдвигается» в область больших скоростей, и скорости молекул могут даже превысить скорость света.
4.Максвелловское распределение молекул по скоростям нельзя использовать для анализа систем молекул при очень низких температурах. При таких температурах максимум кривой распределения резко «сдвигается» в область малых скоростей, и кривая сильно сужается. Тогда в рассматриваемом интервале скоростей может оказаться очень мало молекул, следовательно, к такому числу частиц нельзя применять методы теории вероятностей.
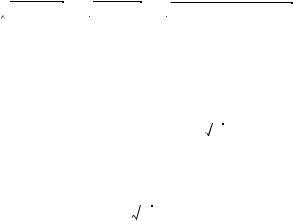
Для примера рассмотрим поведение молекул азота (основной газ, составляющий земную атмосферу) при температуре T = 273 К. Напомним, что молярная масса азота μ = 0,028 кг/моль. При такой температуре наиболее вероятная скорость молекул, в соответствии с (9.14), составит:
vв = 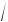 2kT ⁄ m0 =
2kT ⁄ m0 = 
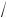 2RT ⁄ μ =
2RT ⁄ μ = 
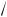 2æ8,31æ273 ⁄ 0,028 = 403 м/с.
2æ8,31æ273 ⁄ 0,028 = 403 м/с.
Подставим выражение для наиболее вероятной скорости (9.14) в функцию распределения (9.11):
|
|
3 |
|
m |
|
2 |
|
|
|
|
|
|
|
|
|
m |
|
2 |
|
|
|
|
|
0 |
v |
|
|
|
|
|
|
|
|
|
0 |
v |
|
|
|||
|
|
-- |
– |
|
|
|
|
|
|
|
|
|
|
3 – |
|
|
|
|
||
f = |
|
m0 2 |
-------------2kT |
4 |
πv |
2 |
|
|
|
1 |
-------------2kT |
2 |
; |
|||||||
|
2-----------πkT |
e |
|
|
|
|
= 4π ---------- |
|
------ |
e |
|
|
v |
|
||||||
|
|
|
|
|
|
|
|
|
|
|
π vв |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
m 0 v |
2 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
– |
|
|
|
|
|
|
|
|
|
|
|
|
|
f |
|
= |
|
4 |
v 2 |
-------------2 k T |
. |
|
|
|
|
|
|
|||
|
|
|
|
|
--------- |
π |
---- |
3- |
e |
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
vв |
|
|
|
|
|
|
|
|
|
|
||
Используя последнее выражение, очень легко находить ответы на вопросы о распределении частиц по скоростям. Найдем долю молекул азота, скорости которых принимают значения от 403 до 413 м/с
119

(ширина интервала скоростей составляет 10 м/с, а середина интервала — 408 м/с):
|
|
|
|
|
|
2 |
|
|
|
v + v |
413 |
|
|
|
m0v |
|
|
N |
4 v 2 |
e– 2kT |
|
4 |
||||
= ∫ |
f dv = ∫ --------- |
dv = |
||||||
N |
|
|
π |
v |
3 |
|
|
π |
v |
403 |
в |
|
|
||||
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
1 |
413 |
----3- |
∫ |
vв |
403 |
m0v
2
– -------------
v2e 2kT dv .
Для вычисления последнего интеграла учтем, что показатель экспо-
|
|
|
|
|
|
|
|
|
m |
0 |
v 2 |
|
v |
2 |
|
ненты можно записать следующим образом: |
|
|
|
= |
|
. Кроме того, |
|||||||||
|
------------- |
----- |
|||||||||||||
|
|
|
|
|
|
|
|
|
2kT |
|
|
2 |
|
||
|
|
|
|
|
|
|
|
|
|
|
|
|
vв |
|
|
воспользуемся теоремой о среднем: |
|
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
m0v |
2 |
|
|
|
|
|
|
|
|
|
|
|
413 |
|
|
|
|
|
|
|
|
|
||
|
N |
4 |
1 |
|
– ------------- |
|
|
|
|
|
|
||||
|
∫ |
v2e |
2kT |
dv = |
|
|
|
|
|||||||
|
-------- |
= ------- |
----- |
|
|
|
|
|
|
||||||
|
N |
π |
3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
vв |
403 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
408 |
2 |
|
|
|
|
|
|
|
|
|
|
4 |
1 |
|
– ----------- |
|
|
|
|
|
|
|
|
|
|
||
æ408 |
2e |
4032 |
(413 – 403) |
= 0,02 . |
|||||||||||
= ------- ----------- |
|
æ |
|||||||||||||
π 4033 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таким образом, только 2 % общего числа молекул имеют скорости, значения которых лежат в выбранном интервале. Если сместить интервал в другой участок скоростей, например выбрать диапазон 1000 ÷ 1010 м / с (ширина интервала скоростей по-прежнему составляет 10 м/с, а середина интервала — 1005 м/с), то только 0,07 % общего числа молекул попадут в этот интервал скоростей.
Весьма любопытен вывод, который получается при ответе на вопрос: «Может ли Земля потерять атмосферу?» Поскольку вторая космическая скорость (скорость «убегания» от поля тяжести планеты) для Земли равна 11 200 м/с, то приведенным выше способом можно определить долю молекул, скорости которых лежат в диапазоне 11 200÷20 000 м / с (ширина интервала скоростей составляет 8800 м / с, а середина интервала — 15 600 м/с). Вычисления в этом случае дают ответ
|
|
|
|
– |
15 6002 |
|
|
N |
|
4 1 |
|
------------------- |
2 |
|
|
= |
3 |
æ15 6002e 403 |
æ8800 = 1,8æ10– 29 . |
||||
N |
|
π 403 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Следовательно, в земной атмосфере все-таки существуют молекулы, скорость которых позволяет им покидать пределы тяготения Земли. Однако сделанный расчет, конечно же, является только оценочным, так как температура на границе атмосферы не равна 273 К. Кроме того, разреженность атмосферы в ее верхних слоях не позволяет говорить о справедливости методов теории вероятностей в подобных условиях.
120