Материал: Общая физика_под ред. Белокопытова_2016 -506с

с другой на расстоянии. В реальных газах существуют силы межмолекулярного притяжения и отталкивания. Силы отталкивания проявляются при взаимных столкновениях молекул и со стенками сосуда. Далее покажем, что при взаимных столкновениях молекулы газа ведут себя как абсолютно упругие шары диаметром Dэфф , зависящим
от химической природы газа. Именно этот эффективный диаметр молекулы свидетельствует о наличии сил отталкивания между молекулами. Межмолекулярные силы притяжения преобладают на бoль′ - ших расстояниях, чем силы отталкивания. Поэтому реальные газы тем ближе по своим свойствам к идеальным газам, чем больше средние расстояния между молекулами, т.е. чем меньше концентрация молекул и соответственно плотность газа. При нормальных условиях, т.е. при давлении p0 = 101 325 Па и температуре T0 = 273,15 К, мно-
гие газы (водород, гелий, неон, азот, кислород, воздух и др.) можно с хорошим приближением считать идеальными. При таких условиях
концентрация молекул газа составляет n0 ≈ 10 25 м– 3, а средние рас-
стояния между молекулами r ≈ 3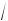 1 ⁄ n0 ≈ 10 – 8 м. Силами притяжения молекул можно пренебречь. Суммарный собственный объем всех молекул газа, содержащихся в 1 м3, составляет Vсобст = nπd 3 / 6 ≈
1 ⁄ n0 ≈ 10 – 8 м. Силами притяжения молекул можно пренебречь. Суммарный собственный объем всех молекул газа, содержащихся в 1 м3, составляет Vсобст = nπd 3 / 6 ≈
≈ 10– 5 м3. Следовательно, собственным объемом всех молекул тоже можно пренебречь по сравнению с объемом газа.
В курсе средней школы рассматривается термическое уравнение состояния идеального газа, называемое уравнением Клапейрона:
pV / T = const, |
(8.7) |
т.е. для данной массы идеального газа отношение произведения давления и объема к термодинамической температуре есть величина постоянная. Запишем это уравнение для 1 моля газа в виде
pVm = RT , |
(8.8) |
где Vm — объем 1 моля газа (молярный объем).
Согласно закону Авогадро, при одинаковых давлениях и температурах молярные объемы различных газов также одинаковы. Из этого закона и (8.8) следует, что постоянная R одинакова для всех газов. Ее называют универсальной газовой постоянной. Экспериментально установлено, что R = 8,31 Дж/(моль К). Для произвольной массы газа выражение (8.7) можно переписать следующим образом:
m
pV = --- RT . (8.9)
μ
106
В такой наиболее общей форме записи термическое уравнение состояния идеального газа называется уравнением Клапейрона— Менделеева. Газ, в точности подчиняющийся уравнению состояния Клапейрона — Менделеева, называется идеальным.
Введем постоянную Больцмана k, равную отношению универсальной газовой постоянной к числу Авогадро:
k = R /NA = 1,38æ10– 23 Дж / К. |
(8.10) |
Тогда из выражения (8.9) легко получить: |
|
p = nkT, |
(8.11) |
где п — концентрация идеального газа.
Примерами простейших термодинамических процессов могут служить следующие процессы:
изотермический процесс, при котором температура системы не меняется (Т = const);
изобарный процесс, при котором давление в системе не меняется (р = const);
изохорный процесс, при котором объем системы не меняется (V = = const).
Эти процессы, происходящие с неизменной массой идеального газа, были изучены и описаны до появления уравнения Клапейрона — Менделеева, и их суть заключена в трех законах идеального газа.
Закон Бойля — Мариотта: если данная масса газа совершает изотермический процесс (Т = const), то произведение давления газа на его объем не изменяется:
pV = const.
Закон Гей-Люссака: если данная масса газа совершает изобарный процесс (p = const), то объем газа изменяется пропорционально его температуре:
V = constæT.
Закон Шарля: если данная масса газа совершает изохорный процесс (V = const), то давление газа изменяется пропорционально его температуре:
p = constæT.
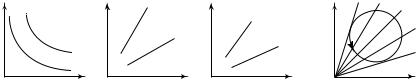
Изохорный, изобарный и изотермический процессы графически изображаются кривыми (соответственно изохорами, изобарами и изотермами) в различных системах координат: ( p,V ); ( p,T ); (V,T ). На рис. 8.2 изображены различные изотермы данной массы газа в координатах (p,V ), различные изобары данной массы газа в координатах (V,T ), различные изохоры данной массы газа в координатах ( p,T ).
107
p |
|
V |
|
|
p |
|
|
p |
V2 |
|
|
T2 |
p1 |
|
|
|
V |
1 |
|
|
|
|
|
p |
|
|
|
|
|
|
||
|
|
2 |
|
|
|
|
|
|
||
|
T1 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
V2 |
|
V |
|
|
|
|
|
|
|
|
|
|
1 |
||
|
|
|
|
|
|
|
|
|
|
|
0 |
V |
0 |
|
T |
0 |
|
T |
0 |
T |
|
|
а) |
|
б ) |
|
|
в) |
|
Рис. 8. 3 |
|
|
|
|
|
|
|
|
|
|
|
|
|
Рис. 8. 2
Отметим то обстоятельство, что график любого изопроцесса разбивает координатную плоскость на две части:
1) во всех состояниях, которые на диаграмме ( p,V ) изображаются точками, лежащими выше изотермы Т1 (рис. 8.2, а), температура газа
больше, чем Т1, т.е. Т2 > Т1;
2) во всех состояниях, которые на диаграмме (V,T ) изображаются точками, лежащими ниже изобары р1 (рис. 8.2, б), давление газа
больше, чем р1, т.е. р2 > р1;
3) во всех состояниях, которые на диаграмме ( p,T ) изображаются точками, лежащими ниже изохоры V1 (рис. 8.2, в), объем газа больше,
чем V1, т.е. V2 > V1.
Эти факты можно использовать, анализируя произвольные процессы. Допустим, на диаграмме ( p,T ) изображен график некоторого произвольного процесса (рис. 8.3). Проведя на диаграмме семейство изохор и рассмотрев пересечение их с графиком процесса, можно определить, как в этом сложном процессе изменялся занимаемый газом объем: изохора V1 соответствует наибольшему объему газа в
данном процессе, а изохора V2 — наименьшему.
При рассмотрении смеси N идеальных газов, находящихся в одном сосуде, уравнение состояния (8.9) можно записать в виде:
N
pV = (m1 ⁄ μ1 + m2 ⁄ μ2 + … + mN ⁄ μN)RT = ∑ (mi ⁄ μi)RT .
i = 1
Вместе с тем смесь идеальных газов можно представить таким идеальным газом, для которого будет справедливо соотношение pV =
N
= (mсм ⁄ μсм )RT . Учтем, что масса смеси mсм = ∑ mi , тогда получим
i = 1
N
∑ mi
μсм = N |
i = 1 |
. |
(8.12) |
|
∑(m ⁄ μ)i
i = 1
108
Выражение (8.12) определяет эффективную молярную массу смеси идеальных газов — молярную массу такого идеального газа, который, имея массу, равную массе смеси газов, в объеме, равном объему смеси, создает давление, равное давлению смеси при температуре, равной температуре смеси.
Модель идеального газа позволяет изучать свойства газов в кинетической теории простейшим образом. Применение всех моделей в физике всегда преследует одну цель — изучить определенную группу физических явлений, абстрагировавшись от ряда реальных условий, усложняющих данные явления. Например, рассматривая модель идеального газа, мы не учитываем, что реальные атомы и молекулы имеют сложную структуру и взаимодействуют между собой.
109

Г л а в а 9
ЭЛЕМЕНТЫ СТАТИСТИЧЕСКОЙ ФИЗИКИ
Макроскопические свойства систем, состоящих из очень большого числа частиц, изучаются статистическим методом. В подобных системах существуют некоторые средние значения физических величин, которые характеризуют всю совокупность частиц в целом (в газе это средние значения скоростей теплового движения молекул, их энергий и т.д.). В системе частиц выполняются законы сохранения энергии, импульса и момента импульса. Все физические процессы в системе протекают непрерывно в пространстве и времени. Любую частицу в системе можно отличить от остальных таких же частиц. Она может иметь произвольные значения координат и импульсов (скоростей).
9.1. Элементарные сведения из теории вероятностей
Статистический метод основан на использовании теории вероятностей и определенных моделей строения изучаемых систем. Основное понятие теории вероятностей — событие, явление, о котором можно говорить, что оно либо произошло, либо нет. Вероятностью данного события P называется отношение числа n* благоприятных исходов опытов (таких, в которых интересующее нас событие произошло) к полному числу опытов n, когда полное число опытов стремится к бесконечности:
n*
P = lim ----- .
n → × n
Суммой двух событий A и B называется событие A B, заключающееся в том, что произошло либо событие A, либо событие B. Вероятность суммы двух несовместных (одновременное осуществление которых невозможно) событий равна сумме вероятностей этих событий.
Произведением двух событий A и B называется событие A∩B, состоящее в появлении совместно и события A, и события B. Вероятность произведения двух событий равна произведению вероятности первого события на вероятность второго (вычисленную в предположении, что первое событие произошло).
110