Материал: Нанотехнологии для всех (Рыбалкина), 2005, c.444
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
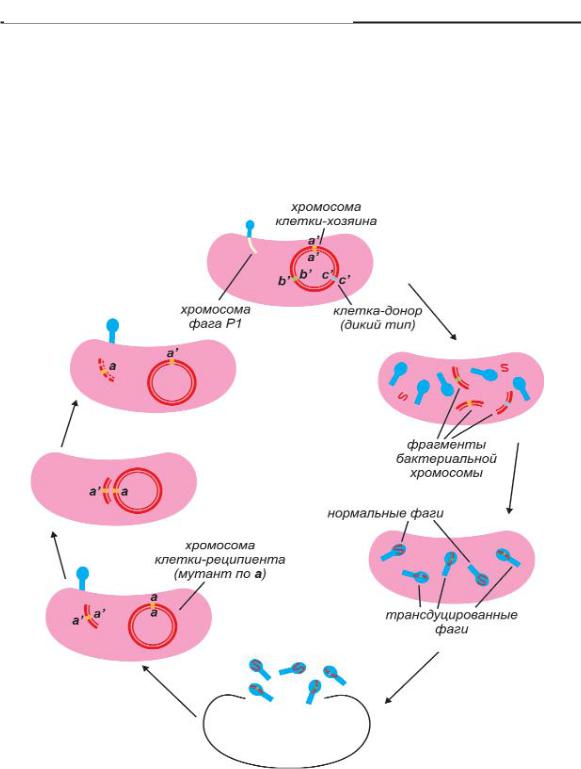
Когда впоследствии такой вирус заражает другую бакте рию, участок бактериальной ДНК проникает в клетку таким же путем, как вирусный. Между трансдуцированной ДНК и участ ком хромосомы может произойти обмен, и как следствие его возникают рекомбинанты, несущие небольшую часть генети ческого материала клетки донора.
Рис 190. Схема общей трансдукции между линиями Е. coli: а) Клетка дикого типа, инфицированная фагом P1;
б) ДНК клетки хозяина деградирует в ходе литического цикла; в) в ходе сборки фаговых частиц некоторые фрагменты бактериальной хромосомы
включаются в несколько фагов потомков, что потом приведет к трансдукции; г) лизис; д) трансдуцирующий фаг инфицирует бактерию реципиента;
е) происходит обмен донорного гена а+ и реципиентного гена а ; ж) образование стабильного трансдуктанта а+.
Итак, мы рассмотрели процесс естественного “горизон тального” обмена генетической информацией между бактерия ми, то есть перемещения генов из одного организма в другой
298
ГЛАВА 6. Биотехнологии и наномедицина
посредством мобильных генетических посредников. Рассмот ренный механизм получил название трансдукции, а понимание его сути привело к рождению генной инженерии.
Как уже было сказано, суть генной инженерии заключается в том, что в генотип организма встраиваются или исключаются отдельные гены или их группы. Для этого используют метод по лучения рекомбинантных, т. е. содержащих чужеродный ген, ДНК, которые затем вводятся в организм реципиента и стано вятся составной частью его генетического аппарата.
Этот процесс состоит из нескольких этапов:
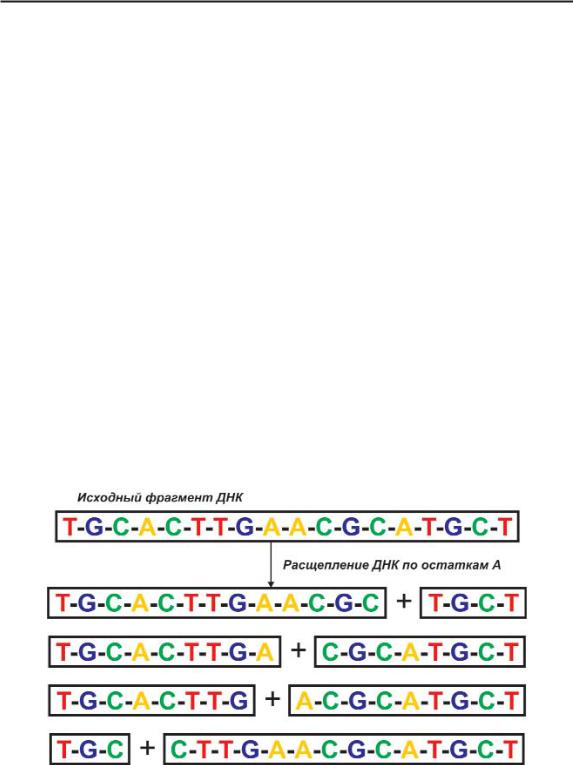
1. Чтобы выделить тот или иной ген из цепочки ДНК, ис пользуется рестрикция – разрезание ДНК на фрагменты уже знакомыми нам ферментами рестриктазами. Они попросту «шинкуют» ДНК: режут на отрезки, но не как попало, а в опре деленных местах. Всякая рестриктаза может опознать лишь од ну стандартную последовательность из нескольких нуклеоти дов. Молекулы рестриктазы химически связываются с ними и в этих местах рвут цепь ДНК. На рисунке изображена схема рас щепления ДНК по остаткам А (аденин).
Рис 191. Схема получения фрагментов ДНК в результате расщепления по определенному нуклеотиду (А)
В настоящее время известно более 400 рестриктаз, способ ных расщеплять ДНК по 120 различным последовательностям нуклеотидов.
2. Лигирование – процесс «сшивания» генов с помощью особых ферментов, называемых лигазами. Лигазы сшивают участки ДНК, образовывая между их крайними нуклеотидами химическую связь.
www.nanonewsnet.ru |
299 |

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
3. После того как рекомбинантная ДНК сшита, ее вводят в
живые клетки. Этот процесс называется трансформацией. Для того, чтобы рекомбинантная ДНК стала частью генетического аппарата клетки, она должна либо встроиться в ее геном и реп лицироваться за ее счет, либо быть способной к автономной репликации. Для этого используют векторы – мобильные гене тические элементы: вирусы, плазмиды и транспозоны. Эти эле менты могут присоединять те или иные гены к своей ДНК, а за тем, оказавшись в клетке хозяине, встраиваться вместе с «отор ванным» чужеродным геном в хромосому хозяина, которая по том реплицируется уже вместе со всей этой новой последова тельностью. В общих чертах это напоминает трансдукцию, имеющую, как мы убедились, место и в природе.
Итак, мы познакомились с общими принципами искусствен ного конструирования молекул ДНК. Рассмотрим теперь нес колько примеров практического применения генной инженерии.
Получение инсулина
Инсулин – гормон поджелудочной железы, регулирующий углеводный обмен и уровень сахара в крови. Его недостаток в организме приводит тяжелейшему заболеванию – сахарному диабету, самой распространенной форме заболеваний эндок ринной системы. Самая тяжелая форма диабета, для лечения которой больному необходим инсулин, вызвана гибелью кле ток, синтезирующих этот гормон.
Раньше инсулин могли выделять только из поджелудочной железы телят и свиней. Для получения 100 г кристаллического инсулина требовалось 800 1000 кг исходного сырья. Однако с развитием генно инженерных методов в 1978 г. был получен штамм бактерий Е. coli (кишечной палочки), способных про дуцировать инсулин. В ДНК бактерии был встроен человечес кий ген, отвечающий за его синтез. Теперь почти весь инсулин в мире производят трансгенные бактерии.
Получение соматотропина
За синтез соматотропина (гормона роста человека) отвечает передняя доля гипофиза. Его недостаток приводит к гипофизар ному нанизму – карликовости (в среднем 1 случай на 5000 чело век). Пригодный для лечения людей соматотропин можно выде лить лишь из гипофиза человека, поэтому раньше его получали
300

ГЛАВА 6. Биотехнологии и наномедицина
из трупов, но в ничтожных количествах: гормона хватало лишь для лечения 1/3 случаев карликовости, и то лишь в развитых странах. Препарат, выделяемый из трупов, имеет некоторые спе цифические особенности, приводящие к тому, что у 30% боль ных, получавших препарат, против гормона вырабатывались ан титела, что сводило на нет его биологическую активность.
Сейчас гормон роста синтезируют с помощью специально сконструированных бактерий Е. coli. Впервые такую бактерию удалось получить в 1979 году.
Получение интерферонов
В 1957 году в Национальном институте медицинских иссле дований в Лондоне было установлено, что клетки человека и животных, подвергнутые воздействию вируса, выделяют веще ства, придающие непораженным клеткам устойчивость к ви русной инфекции. Они как бы препятствуют (интерферируют) размножению вирусов в клетке и поэтому были названы интер* феронами. Интерфероны помогают нашему организму бороться со множеством вирусных заболеваний.
Препараты на основе различных видов интерферонов ис пользуются как иммуномодуляторы – для нормализации и уси ления иммунной системы, в т. ч. для лечения различных тяже лых заболеваний – острого вирусного гепатита, рассеянного склероза, остеосаркомы, миеломы и некоторых видов лимфом. Их применяют и для лечения меланом, ряда опухолей гортани, легких и мозга.
Традиционно интерфероны извлекали из крови человека. Из 1 л крови можно выделить всего 1 мкг интерферона, то есть примерно одну дозу для инъекции. На современном этапе ин терфероны получают с помощью генетически модифицирован ных микроорганизмов. Удалось получить штаммы бактерий, способные синтезировать до 5 мг интерферона на литр бакте риальной суспензии, содержащей примерно 1011 бактерий, что заменяет кровь 25 000 доноров.
Трансгенные животные
Применение методов генной инженерии в животноводстве позволяет повышать продуктивность животных (например, удои молока), сопротивляемость их организма к болезням и т. д. Жи вотных, имеющих в своем геноме чужой ген, принято называть
www.nanonewsnet.ru |
301 |

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
трансгенными. Благодаря переносу генов у трансгенных живот ных возникают новые качества, а дальнейшая селекция позволя ет закрепить их в потомстве и создавать трансгенные линии.
Так, были получены животные*биореакторы, способные выделять ценные биологические вещества. Например, в России группой ученых под руководством Л. К. Эрнста была выведе на трансгенная овечка, которая с молоком выделяет химозин – фермент, используемый в производстве сыра. Не так давно для сыроваренной промышленности требовалось огромное коли чество желудков телят. В последние несколько десятков лет практически все сыроделы пользуются химозином, получен ным методом микробиологического синтеза из культур бакте рий и микроскопических грибков. Очевидно, что такое получе ние химозина не только гуманнее, но и выгоднее традицион ных способов, требующих убийства сотни телят. Всего из 3 л молока трансгенной овцы можно получить достаточно химози на для производства тонны сыра – и при этом не тратиться ни на работу ферментера, ни на выделение из культуральной жид кости нужного фермента и его очистку.
Другой пример – трансгенная корова, которая выделяет с молоком лекарственный препарат эритропоэтин, применяе мый в терапии лейкозов. Ведутся исследования по получению многих других лекарств из молока животных. Применяемые для этого биотехнологические методы с использованием бакте рий дороги и сложны. А трансгенные животные быстро размно жаются, и выход полезных веществ с их молоком превосходит таковой у бактерий.
Другая важная задача – выведение животных, устойчивых к заболеваниям. Потери в животноводстве, вызванные болезня ми, достаточно велики, но уже созданы популяции трансген ных коров и кур, устойчивых к некоторым паразитам.
Трансгенные растения
Тысячи лет люди выводят новые сорта растений путем от бора экземпляров с новыми свойствами, полученными в ре зультате случайных мутаций. С начала ХХ века стали целенап равленно применять облучение и химические мутагены, слия ния соматических клеток и т. д., а скрещивание и отбор стали проводить с учетом законов Менделя. При этих традиционных
302