Материал: Нанотехнологии для всех (Рыбалкина), 2005, c.444

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
ми первых двух атомов, что дает еще одну молекулярную орби таль. Когда атомов много, возникает огромное число трехмер ных молекулярных орбиталей, простирающихся во всех нап равлениях. Вследствие многократного перекрывания орбита лей валентные электроны каждого атома испытывают влияние многих атомов.
Металлическая связь объясняет свойства металлов, в част ности, их прочность. Под действием деформирующей силы ре шетка металла может изменять свою форму, не давая трещин, в отличие от ионных кристаллов.
Рис 57. Действие деформирующей силы на кристаллическую решетку металла
Высокая теплопроводность металлов объясняется тем, что если нагреть кусок металла с одной стороны, то кинетическая энергия электронов увеличится. Это увеличение энергии расп ространится в “ электронном море” по всему образцу с боль шой скоростью.
Становится понятной и электрическая проводимость ме таллов. Если к концам металлического образца приложить раз ность потенциалов, то облако делокализованных электронов будет сдвигаться в направлении положительного потенциала: этот поток электронов, движущихся в одном направлении, и представляет собой всем знакомый электрический ток.
Ван дер ваальсовы силы
Кроме рассмотренных типов химической связи говорят также о сравнительно слабых силах Ван дер Ваальса. В 1873 го ду этот человек выдвинул предположение о существовании сил межмолекулярного притяжения, подобных тем, что существу ют в связях между атомами. В дальнейшем гипотеза подт вердилась – были открыты различные типы межмолеку
лярного взаимодействия, где Рис 8. Схема диполь дипольного притяжения
128
ГЛАВА 3. Нанохимия и наноматериалы
наиболее распространено так называемое диполь*дипольное при* тяжение.
Некоторые молекулы (преимущественно с ковалентными связями) обладают так называемым дипольным моментом. Его суть в том, что в одной части молекулы “скапливается” больше электронов, чем в другой. Это приводит к возникновению раз ности потенциалов на ее концах. Сила притяжения между раз личными зарядами связывает молекулы между собой, как пока зано на рисунке.
В настоящий момент термин “Ван дер ваальсовы силы” распространяется на все слабые межмолекулярные силы, кроме водородной связи.
Водородная связь
Несмотря на то, что водородная связь, возникающая вслед ствие силы притяжения между атомом водорода и электроотри цательным атомом, представляет собой пре дельный случай диполь дипольного притя жения, ее, как правило, не относят к силам
Ван дер ваальса. Во первых, пото
му что она гораздо сильнее обычных
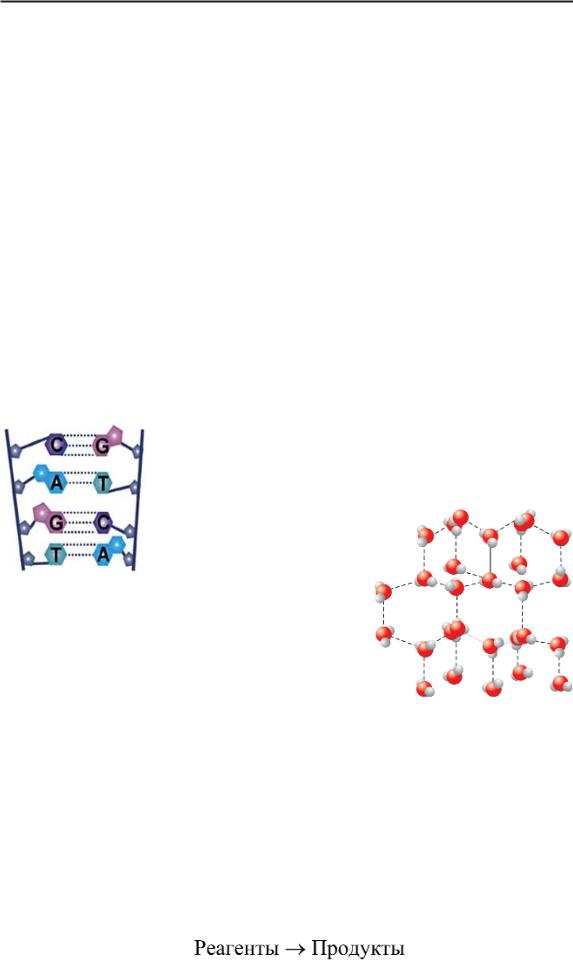
Рис 59. Схема водородной межмолекулярных свя
связи в молекуле ДНК |
зей (рис. 60), а во вто |
|
рых, потому что она может возникать и в виде внутримолекулярных связей (рис 59).
Именно водородные связи объясня ют многие уникальные свойства воды и Рис 60. Схема водородной связи в
льда. |
кристалле льда |
|
Что такое нанохимия?
Не требует пояснений, что химическая связь образуется в результате химических реакций. При этом вещества, подверга ющиеся превращению, называются реагентами, а вновь обра зующиеся вещества называют продуктами. Таким образом, лю бую реакцию можно записать так:
www.nanonewsnet.ru |
129 |

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
Например:
На ход реакции влияет множество факторов: температура, давление, состояние и концентрация исходных веществ и пр.
Балк технология (традиционные химия, физика, механи ка) имеет дело с макроскопическими количествами вещества, содержащими такое громадное количество атомов, что вещест во кажется сплошным и мы редко вспоминаем о его атомарной структуре. Триллионы соединенных вместе атомов образуют так называемое компактное вещество.
Стремительное развитие прецизионной техники, в част ности, сканирующих микроскопов, позволило изучать вещест ва на уровне отдельных атомов и молекул. И вот тут то ученых ждало множество сюрпризов! Оказалось, что одно и то же ве щество может значительно изменять свои химические свойства и реакционную способность в зависимости от количества ато мов в исследуемом образце и его размера.
Первым обратил на это внимание известный ученый XIX века Майкл Фарадей, сумевший получить коллоидную суспен* зию5, состоящую из крошечных частиц золота. В отличие от своего компактного состояния, имеющего всем знакомый жел товатый блеск, полученный образец был фиолетового цвета. Это говорит о том, что отражающие свойства золота изменяют ся при уменьшении размеров его частиц.
Количество атомов в частице даже назвали "третьей координатой" таблицы Менделеева (наряду с группой и рядом).
Следует отметить, что именно первые опыты по получению наноскопических частиц привели к бурному росту интереса к нанохимии в научных кругах. Оказалось, что частицы наномет ровых размеров обладают повышенной химической актив ностью и реакции с их участием протекают гораздо быстрее. Это свойство наночастиц привело к созданию новых эффек тивных катализаторов6.
5 Суспензией (или взвесью) называется гетерогенная смесь двух компонентов. Она состоит из более крупных частиц одного компонента, взвешенных в среде второго компонента. По истечении некоторого времени частицы суспензии осаждаются на дно сосуда. Суспендированные (взвешенные) частицы обычно имеют диаметр порядка 1000 нм. и больше.
6 Катализатор это вещество, которое повышает скорость химической реакции, но само не расходуется в этом процессе.
130

ГЛАВА 3. Нанохимия и наноматериалы
Сегодня ученые умеют получать наноструктуры практичес ки всех химических элементов, что дает огромную свободу для исследований. В последнее время стало известно, что наночас тицы серебра гораздо лучше убивают бактерии, чем серебро в компактном состоянии, что делает их полезными для очистки воды и борьбы с инфекциями. На сегодняшний день наночас тицы являются наиболее изученной областью нанохимии.
Частицы металлов размером менее 10 нм, называемые клас* терами, обладают высокой химической активностью и способ ны вступать в реакции с другими веществами практически без какой либо дополнительной энергии. Избыточность энергии таких частиц объясняется нескомпенсированностью связей их поверхностных атомов. Дело в том, что доля поверхностных атомов у наночастицы значительно больше, чем у вещества в компактном состоянии, и растет с уменьшением частицы. Со ответственно увеличивается и вклад поверхностных атомов в энергию системы.
Рис 61. Большинство атомов наночастицы (слева) лежат на ее поверхности, в отличие от компактного вещества (справа)
Из школьного курса физики мы знаем, что поверхностные атомы обладают некоторой избыточной энергией по сравне нию с внутренними – это объясняет поверхностное натяжение и капиллярный эффект. Избыточность энергии существенно влияет на температуру плавления, растворимость, электропро* водность, окисленность, токсичность, взрывоопасность и т.д. Все это позволяет утверждать, что размер частицы является актив ной переменной, определяющей наряду с другими факторами ее свойства и реакционную способность.
Свойства наносистем настолько отличаются от свойств макроскопических количеств тех же веществ, что их изучает особое научное направление под названием физикохимия наносистем или нанохимия.
www.nanonewsnet.ru |
131 |

НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
В первой половине ХХ века наибольший вклад в нанохи мию внесли специалисты, изучавшие коллоиды7, а во второй по ловине – полимеры, белки, природные соединения, фуллерены и нанотрубки.
Активно развиваясь в последние десятилетия, нанохимия занимается изучением свойств различных наноструктур, а так же разработкой новых способов их получения, изучения и мо дификации.
Одна из приоритетных задач нанохимии установление связи между размером наночастицы и ее свойствами.
В нанохимии чрезвычайно велика роль квантовых размер* ных эффектов, вызывающих изменение свойств вещества в за висимости от размера частиц и количества в них атомов или молекул. Роль размерных эффектов настолько велика, что предпринимаются попытки создать таблицы зависимости свойств кластеров и наночастиц от их размера и геометрии на подобие периодической таблицы элементов Д.И. Менделеева.
Для промышленного получения наночастиц существует много способов: биохимический, радиационно химический, фотохимический, электровзрывной, микроэмульсионный, де тонационный, лазерная абляция в жидкости, конденсация, ва куумное испарение, ионная имплантация и др. Позже мы рас смотрим некоторые способы подробнее.
Объекты нанохимии. Классификации наночастиц
Поскольку нанохимия – наука сравнительно молодая, пока нет ни единой терминологии, ни классификации того, что она изучает. Более того: можно сказать, что классификаций столько же, сколько ученых. Относительно общепризнанным считает ся, что нанохимия исследует получение и свойства различных
наносистем.
Под наносистемой здесь понимается взвесь наночастиц размером не более 100 нм в некоторой среде. При этом сами на ночастицы следует понимать как системы, состоящие из еще
7 Коллоиды занимают промежуточное место между растворами и суспензиями. Они состоят из диспергированных частиц (от "dispetsio" рассеяние) и дисперсионной среды, в которой распределены частицы, и отличаются меньшими, по сравнению с суспензий, размерами частиц (1 500 нм.) В отличие от суспендированных частиц, коллоидные частицы не осаждаются и не отделимы от дисперсионной среды обычными методами. Примеры коллоидов: дым, все виды аэрозолей, взбитые сливки, фруктовое желе, молоко, майонез, мыльная пена и т.п.
132