Материал: Нанотехнологии для всех (Рыбалкина), 2005, c.444

ГЛАВА 3. Нанохимия и наноматериалы
(полностью заполнить свою внешнюю электронную оболочку). Впервые эту гипотезу выдвинули в 1916 г. ученые Коссель и Ль юис, а впоследствии она была доказана и экспериментально.
Вглаве, посвященной квантовым явлениям, говорилось о том, что атомы так называемых “благородных газов” (гелия, не она, аргона и др.) упорно избегают химических связей. Такая “неприступность” этих элементов обусловлена тем, что каждый из них сам по себе имеет устойчивую электронную конфигура цию. Конфигурация гелия – 1s2, а остальных – Ns2Np6, где N – номер соответствующего химического ряда.
Вотличие от инертных газов, остальные атомы имеют неус тойчивую электронную конфигурацию и охотно вступают в хи мические связи с другими элементами. Способность образовы вать связи называется валентностью.
Ионная связь
Ионная связь представляет собой электрическое притяже ние между противоположно заряженными ионами (частицами, несущими электрический заряд).
"Ion" в переводе с греческого, означает "идущий" это подчеркивает, что ионы движутся в электрическом поле.
Согласно гипотезам Планка и Бора, энергия каждого электрона в атоме квантована и принимает лишь определенные значения, соответствующие конкретным энергетическим уров ням (орбитам). Электроны могут переходить с одного уровня на другой, поглощая или излучая фотоны. Поглотив фотон, элект рон переходит на более высокую орбиту, а сила, связывающая его с ядром, уменьшается.
Если электрону удается полностью “освободиться” от сил притяжения ядра и покинуть атом, то происходит ионизация атома. Атом превращается в положительный ион, именуемый катионом и обозначаемый знаком “плюс”.
Na+, Аg+ катионы натрия и серебра
Если же атом, наоборот, принимает в себя дополнительные электроны, то их избыток превращает его в отрицательный ион
– анион, который изображается с “минусом”, например:
Cl , O анионы хлора и кислорода
www.nanonewsnet.ru |
123 |
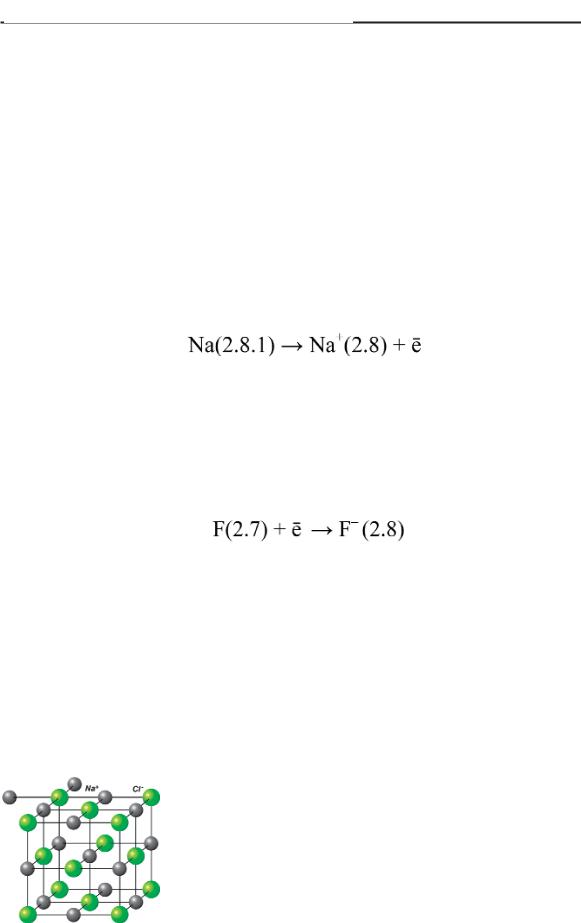
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
Напомним, что химическая связь объясняется стремлени ем атомов приобрести устойчивую электронную конфигура цию, подобную конфигурации “ближайшего” к ним инертного газа. Рассмотрим некоторую последовательность элементов в таблице Менделеева, среди которых имеется неон (1s12s22p6).
В скобках рядом с символом элемента указано число элект ронов в K*, L* и М оболочках.
F(2.7); Ne(2.8); Na (2.8.1)
Атом натрия может приобрести устойчивую электронную конфигурацию неона, избавившись от одного электрона.
Образовавшаяся частица – положительно заряженный ион натрия.
У фтора на один электрон меньше, чем у неона. Следова тельно, если фтор присоединит один электрон (например, от атома натрия), он приобретает заполненную внешнюю оболоч ку из восьми электронов:
Между полученными частицами – анионом фтора и катио ном натрия – будет действовать сила электростатического при тяжения, связывающая их между собой. Это и называется ион* ной химической связью.
Одно из свойств ионных соединений – способность обра зовывать кристаллическую решетку, в узлах которой располо жены положительные и отрицательные ионы. Типичный представитель вещества с ионной связью – всем известная по варенная соль. Ее формула – NaCl.
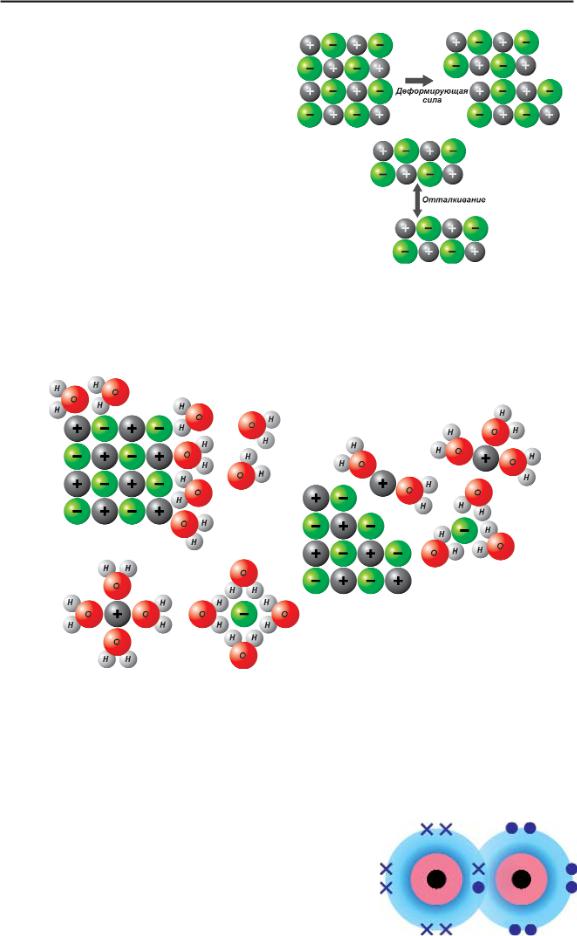
Большинство ионных соединений легко разрушаются под внешним воздействием или в химических реакциях. На рисунке 52 пока зано, что происходит, если на ионный крис талл действует деформирующая сила. Не большие сдвиги в кристаллической решетке сближают одинаково заряженные ионы. При этом силы отталкивания между одноименны ми зарядами создают трещины в кристалле.
124
ГЛАВА 3. Нанохимия и наноматериалы
Рисунок 53 хорошо иллю стрирует, что происходит с кристаллами соли, когда им приходится иметь дело с моле кулами воды. Атомы, из кото рых состоит вода имеют раз личный заряд, (кислород боль ше и тянет электронное “одея ло” на себя, что делает его от рицательнее, чем водород). По
этому атомы кислорода притя Рис 52.. Схема поведения кристаллической решетки NaCl под действием деформирующей силы
гивают положительно заря женные катионы натрия, а атомы водорода – анионы хлора,
растаскивая кристаллическую решетку NaCl.
Рис 53. Иллюстрация процесса растворения соли вводе
Ковалентная связь
Ионная связь – не единственный тип химической связи. В молекуле хлора Cl2 (3s23p5) мы встречаемся с так называемой ко
валентной связью между атомами. В такой связи каждый из двух атомов делится с другим одним из своих внешних электронов. При этом оба при обретают восьмой электрон в свою внеш нюю оболочку и обретают устойчивую конфигурацию. Каждую ковалентную
связь удобно схематически представить Рис 54. Схема ковалентной связи палочкой (С С) или в виде точки и крести
www.nanonewsnet.ru |
125 |
НАНОТЕХНОЛОГИИ ДЛЯ ВСЕХ
ка. Каждая точка или крестик изображают электрон в валентной оболочке атома.
Электроны, образующие общую пару, называются валент* ными. Образуя ковалентную связь, они занимают одну и ту же орбиталь, а их спины, согласно принципу Паули, направлены в противоположные стороны. Таким образом, орбитали атомов при ковалентной связи перекрываются между собой.
Для того чтобы орбитали перекрывались, расстояние меж ду атомами должно быть очень маленьким. Этому препятству ют силы отталкивания между их ядрами. Но ковалентная связь достаточно сильна, чтобы удержать атомы в таком положении. Благодаря этому нелегко оторвать атомы с общей орбиталью друг от друга.
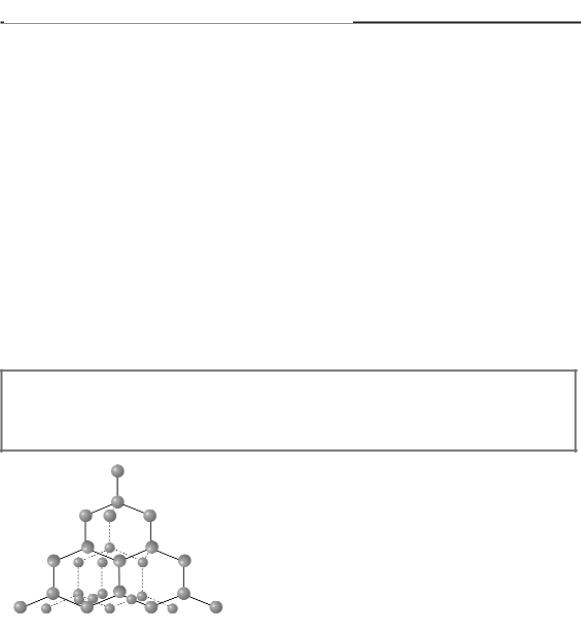
Именно большая энергия ковалентной связи объясняет феноменальную прочность алмаза, в котором каждый атом углерода ковалентно связан с четырьмя другими
Ковалентная связь наиболее ха рактерна для молекул, состоящих из одинаковых атомов (например, H2
или Cl2), либо каркасных структур
(алмаз). Двойная, и, тем более, трой ная ковалентные связи прочнее обычной.
Ионная и ковалентная связи являют сядвумяпредельнымислучаямимножества реально существующих химических связей, которые в действительности имеют проме жуточный характер. Однако можно утверждать, что некоторые соединения являются преимуще ственно ионными, а некото рые – преимущественно ковалентными.
Проводя шутливую аналогию, можно заметить, что стрем ление атомов отнять, отдать или поделить между собой элект роны, чтобы достичь электронной устойчивости, сильно напо минает социальное поведение людей, манипулирующих день гами для достижения своего комфорта (морального либо мате риального). Есть “атомы–меценаты”, вступающие в химичес кую связь путем безвозмездной отдачи “лишних” электронов. В противоположность им существуют и настоящие “рэкетиры”, которые так и норовят оторвать какой нибудь электрон у зазе
126
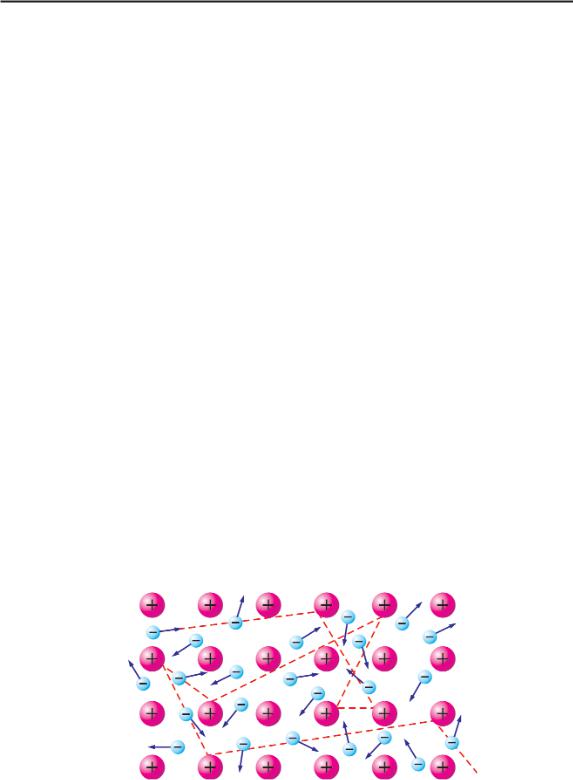
ГЛАВА 3. Нанохимия и наноматериалы
вавшегося соседа. Но есть и “добропорядочные граждане”, объединяющие свои электроны для совместного достижения электронной устойчивости. В подобном контексте неудиви тельно, что ковалентная связь гораздо стабильнее, чем ионная, а также обладает гораздо большей энергией (прочностью)!
Впрочем, стоит заметить, что поведение отдельных атомов во многом зависит “от обстоятельств” – в разных реакциях од ни и те же вещества (как и люди) могут вести себя совершенно по разному.
Металлическая связь
Металлы – очень распространенный материал современ ной промышленности. Большая часть машин, станков, инстру ментов и транспортных средств изготовлена из металла. Метал лы хорошо проводят тепло и электричество, они достаточно прочны, их можно деформировать без разрушения. Некоторые металлы ковкие (их можно ковать), некоторые тягучие (из них можно вытягивать проволоку). Эти уникальные свойства объ ясняются особым типом химической связи, соединяющей ато мы металлов между собой – металлической связью.
Металлы в твердом состоянии существуют в виде кристал лов из положительных ионов, как бы “плавающих” в море сво бодно движущихся между ними электронов.
Рис 6. Кристаллическая решетка металла. Показана траектория одного из свободно движущихся электронов
Электроны в металлах делокализованы, то есть не принад лежат какому либо конкретному атому. Как получается такое уникальное электронное “море”?
Когда два атома металла сближаются, орбитали их внешних оболочек перекрываются, образуя молекулярные орбитали. Если подходит третий атом, его орбиталь перекрывается с орбиталя
www.nanonewsnet.ru |
127 |