Материал: Национальная+программа+Недостаточность+витамина+Д+2018
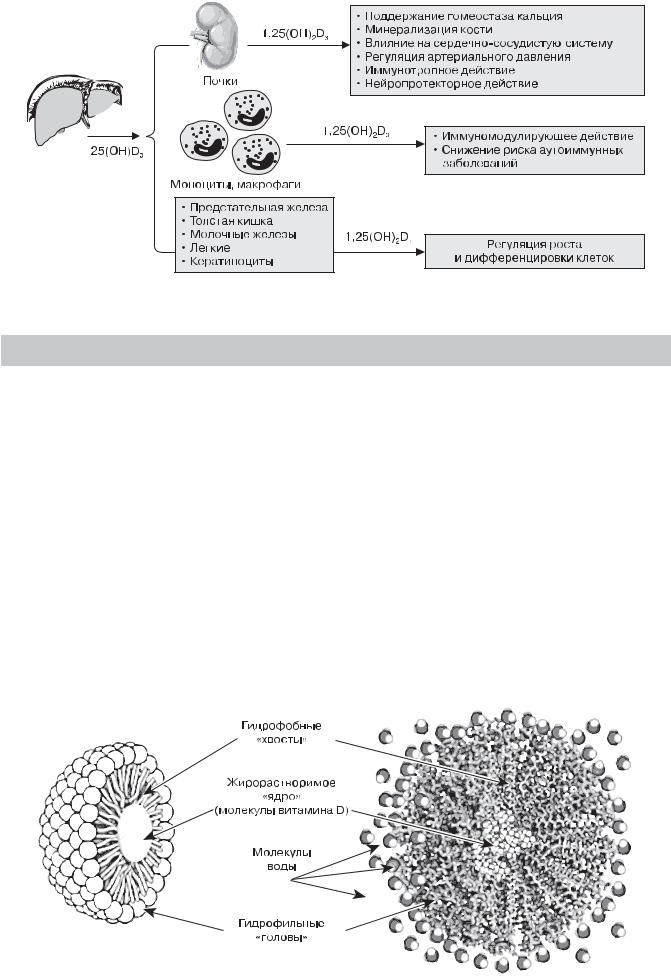
Рис. 2.2. Эффекты витамина D [1]
Таблица 2.2. Физиологические системы и процессы, регулируемые активной формой витамина D [14–16]
Физиологические |
Физиологические процессы |
Нарушения и болезни, |
|
||
системы |
и влияние на них 1,25(ОН)2D |
связанные с дефицитом витамина D |
|
|
|
15 |
|||||
Гомеостаз кальция |
Всасывание кальция в кишечнике, |
Рахит, остеомаляция, остеопороз |
|
||
|
|
||||
|
ремоделирование костей скелета |
|
|
|
|
|
|
|
|
||
Все клетки организма |
Регуляция клеточного цикла |
Повышение риска рака простаты, молочной железы, |
|
||
|
|
колоректального рака, лейкемии и других видов рака |
|
||
|
|
|
|
||
Иммунная система |
Стимуляция функции макрофагов |
Повышенная частота инфекционных заболеваний, |
|
||
|
и синтеза антимикробных пептидов |
в т. ч. туберкулеза, а также аутоиммунных |
|
||
|
|
заболеваний, в частности сахарного диабета 1-го типа, |
|
||
|
|
рассеянного склероза, псориаза, язвенного колита, |
|
||
|
|
болезни Крона |
|
||
|
|
|
|
||
-Клетки |
Секреция инсулина |
Нарушение секреции инсулина, толерантности |
|
||
поджелудочной железы |
|
к глюкозе; сахарный диабет |
|
||
|
|
|
|
||
Сердечно-сосудистая |
Регуляция ренин-ангиотензиновой |
Высокорениновая (почечная) гипертония, повышенный |
|
||
система |
системы, свертывание крови, фибринолиз, |
тромбогенез; повышенный риск сердечно-сосудистых |
|
||
|
функционирование сердечной мышцы |
заболеваний, инфаркта миокарда |
|
||
|
|
|
|
||
Мышечная система |
Развитие скелетной мускулатуры |
Повышенная частота миопатий |
|
||
|
|
|
|
||
Мозг |
Наличие рецептора витамина D |
Недостаток витамина D в период внутриутробного |
|
||
|
и 1 -гидроксилазы витамина D в тканях |
развития приводит к нарушениям поведенческих |
|
||
|
мозга человека |
реакций во взрослом состоянии (исследования |
|
||
|
|
на мышах); у взрослых и пожилых людей повышает |
|
||
|
|
риск болезни Паркинсона и умственной деградации |
|
||
|
|
|
|
|
|
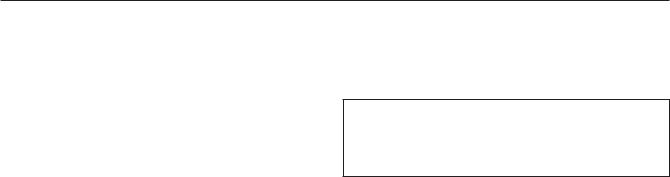
Рис. 2.3. Мицеллярные структуры, образуемые поверхностно активными веществами в водном растворе [18]

Рекомендуемым препаратом для профилактики и лечения дефицита витамина D является холекальциферол (D3)
В норме мицеллы, содержащие витамин D, образуются при транзите в кишечнике под действием природных эмульгаторов — желчных и жирных кислот. Благодаря процессу мицеллообразования (эмульгации) происходит всасывание в тонкой кишке не только витамина D, но и сложных липидов (например, лецитина), других жирорастворимых витаминов (А, Е и К).
Исследование свойств мицелл, образованных различными жирными кислотами, показало, что длинноцепочечные жирные кислоты в концентрациях порядка 500 мкмоль/л снижают всасывание холекальциферола, а омега-9 олеиновая кислота и омега-3 эйкозапентаеновая кислота значительно повышают всасывание холекальциферола [19].
У пациентов с муковисцидозом, холестазом и другими нарушениями функции печени (стеатогепатоз и др.) секреция желчных кислот снижается. Это затрудняет мицеллообразование и, следовательно, резко снижает усвоение витамина D (в т. ч. из масляных растворов) и других жирорастворимых витаминов. Синтез жирных кислот снижается в пожилом возрасте, при соблюдении определенных диет, при включении в рацион блокаторов мицеллирования и усвоения витамина D (пальмитиновой кислоты, насыщенных жиров, маргарина).
16 Мицеллированные (водорастворимые) растворы витамина D (к ним относится препарат «Аквадетрим») обеспечивают хорошую степень всасывания практически во всех возрастных группах пациентов (дети, взрослые, пожилые) с минимальной зависимостью от состава рациона, приема лекарственных препаратов, состояния печени и биосинтеза желчных кислот.
ЛИТЕРАТУРА
1.Захарова И. Н., Яблочкова С. В., Дмитриева Ю. А. Известные и неизвестные факты о витамине D. Вопросы современной педиатрии. 2013;12(2):26–31.
2.Desai N. S., Tukvadze N., Frediani J. K., Kipiani M., Sani-
kidze Е., |
Nichols M. M., |
Hebbar G., |
Kempker R. R., |
Mirtskhulava V., Kalandadze I., Seydafkan S., Sutaria N., |
|||
Chen T. C., |
Blumberg H. M., |
Ziegler T. R., |
Tangpricha V. |
Effects of sunlight and diet on vitamin D status of pulmonary tuberculosis patients in Tbilisi, Georgia. Nutrition. 2012;28(4):362–6.
3.Prosser D. E., Jones G. Enzymes involved in the activation and inactivation of vitamin D. Trends Biochem Sci. 2004; 29(12):664–673.
4.Holick MF. Vitamin D status: measurement, interpretation, and clinical application. Ann Epidemiol. 2009;19(2):73–78.
5.Holick M. F. Resurrection of vitamin D deficiency and rickets. J Clin Invest. 2006;116:2062–72.
6. Holick M. F. High prevalence of vitamin D inadequacy and implications for health. Mayo Clin Proc. 2006;81:353–73.
7.Camille E. Powe, Michele K. Evans, Julia Wenger, et al. Vitamin D — Binding Protein and Vitamin D Status of Black Americans and White Americans. N Engl J Med. 2013;369:1991–2000.
8.Norman A.W. From vitamin D to hormone D: fundamentals of the vitamin D endocrine system essential for good health.
American Journal of Clinical Nutrition. 2008;88(2):491–499.
9.de Borst M. H., de Boer R. A., Stolk R. P., et al. Vitamin D deficiency: universal risk factor for multifactorial diseases?
Curr Drug Targets. 2011;12(1):97–106.
10. Ramagopalan S. V., et al. A ChIP-seq-defined genomewide map of vitamin D receptor binding: Associations with disease and evolution. Genome Research. 2010. Doi: 10.1101/gr.107920.110.
11.Торшин И. Ю., Громова О. А. Экспертный анализ данных в молекулярной фармакологии. М.: МЦНМО. 2012. 768 с.
12.Шварц Г. Я. Витамин Д и Д-гормон. М.: Анахарсис. 2005.
13.Giovannucci Е. Expanding Roles of Vitamin D. J Clin Endocrin Metab. 2009;94(1):418–420.
14.Norman A.W., Bouillon R. Vitamin D nutritional policy needs a vision for the future. Exp Biol Med. 2010;235:1034–1045.
15.Grundmann M, von Versen-Höynck F. Vitamin D-roles inwomen’s reproductive health? Reprod Biol Endocrinol. 2011;9:146.
16.Шилин Д. Е. Витамин-гормон D в клинике XXI века: плейотропные эффекты и лабораторная оценка (лекция).
Клиническая лабораторная диагностика. 2010;12:17–23.
17.Lenormand Y, Rautureau M, Mary JY, Rambaud JC. Intestinal absorption of vitamin D, linoleic acid and cholesterol from micellar solutions: study in normal humans by the
«in situ» perfusion method]. Biol Gastroenterol (Paris). 1975;8(3):207–221.
18.Carre M, Miravet L, Hioco D. Solubilization of vitamin D3 in a micellar solution. C R Seances Soc Biol Fil. 1972;
166(6):807–811.
19.Goncalves A, Gleize B. Fatty acids affect micellar properties and modulate vitamin D uptake and basolateral efflux in Caco-2 cells. J Nutr Biochem. 2013;24(10):1751–7.
3. СОДЕРЖАНИЕ АКТИВНЫХ МЕТАБОЛИТОВ ВИТАМИНА D В СЫВОРОТКЕ КРОВИ КАК ПОКАЗАТЕЛЬ ОБЕСПЕЧЕННОСТИ ОРГАНИЗМА ВИТАМИНОМ D
Ранняя диагностика недостаточности витамина D возможна только при измерении определенных биохимических параметров, прежде всего уровней его метаболитов в крови. Клинические симптомы недостаточности витамина D в виде рахита, остеомаляции, остеопороза и внескелетных проявлений в результате дефицита этого витамина возникают в течение длительного периода времени.
Наиболее информативным показателем обеспеченности организма витамином D является содержание кальцидиола [25(OH)D] как в сыворотке, так и плазме крови [1]. 25(OH)D имеет период полураспада около 2–3 недель. Кальцидиол включает в себя витамин D, полученный из пищевых продуктов, и витамин D, который синтезируется в коже после пребывания на солнце. Время полураспада в кровотоке другой активной формы витамина D — кальцитриола [1,25(ОН)2D] — составляет всего 4 часа. Кальцитриол циркулирует в 1000 раз более низкой концентрации, чем 25(ОН)D, а уровень его в крови жестко регулируется сывороточными уровнями паратиреоидного гормона (ПТГ), кальция и фосфатов [2–4].
Таким образом, 25(OH)D (кальцидиол) является метаболитом витамина D, который используется для определения его статуса в организме человека [1].
Вопрос о том, какой уровень 25(OH)D в сыворотке является нормальным, а какие показатели следует расценивать как гиповитаминоз, продолжает активно обсуждаться. К настоящему времени пересмотрена точка зрения об оптимальном содержании витамина D в сыворотке крови
[5].В течение многих лет считали, что дефицит витамина D
ворганизме человека имеет место тогда, когда его концентрация в крови составляет менее 8 нг/мл. Тем не менее
в1997 году M. C. Chapuy с соавт. оценили соотношение между количеством 25(OH)D и уровнем ПТГ, определив, что только при концентрации 25(OH)D от 30 до 40 нг/мл достигается баланс данных биологически активных веществ
ворганизме [6].
Фармакологические пробы показали значительное повышение уровней ПТГ, если исходные уровни 25(ОН)D были ниже 20 нг/мл. Уровни ПТГ демонстрируют обратную связь
с уровнем 25(ОН)D и достигают плато у взрослых при уровнях 25(ОН)D в крови 30–40 нг/мл. Уровень витамина D должен быть такой, при котором блокируется избыточный синтез ПТГ [7].
Адекватный уровень витамина D определяется как концентрация 25(ОН)D более 30 нг/мл (75 нмоль/л), недостаточность —
как 21–30 нг/мл (51–75 нмоль/л), дефицит — менее 20 нг/мл (50 нмоль/л) [8]
ЛИТЕРАТУРА |
|
|
|
1. |
Holick M. F. Vitamin D status: measurement, interpretation, |
|
|
|
and clinical application. Ann Epidemiol. 2009;19(2):73–78. |
|
|
2. |
Holick M. F. High prevalence of vitamin D |
inadequacy |
|
|
and implications for health. Mayo Cli. |
Proc. 2006; |
|
|
81(3):353–373. |
|
|
3. |
Bouillon R. Vitamin D: from photosynthesis, |
metabolism, |
17 |
and action to clinical applications. Endocrinology / Ed. by L. J. de Groot, J. L. Jameson. Philadelphia: WB Saunders. 2001. Р. 1009–1028.
4.Bischoff-Ferrari H. A., Giovannucci E., Willett W. C., et al. Estimation of optimal serum concentrations of 25-hydroxyvi- tamin D for multiple health outcomes. Am J Clin Nutr. 2006;84(1):18–28.
5.Chun Rene F, Adams John S, Hewison, Martin Back to
the future: a new look at vitamin D. J Endocrin. 2008; 198(2):261–9.
6.Chapuy M. C., Preziosi P., Maamer M., Arnaud S., Galan P., Hercberg S., Meunier P. J. Prevalence of vitamin D insufficiency in an adult normal population. Osteoporosis Int. 1997;7:439–443.
7.Holick M. F. Variations in 25-hydroxyvitamin D assay
results. J Clin Endocrinol Metab. 2005;90(5):210.
8. Holick M. F., et al. Evaluation, Treatment, and Prevention of Vitamin D Deficiency: an Endocrine Society Clinical Practice Guideline. J Clin Endocrin Metab. July 2011; 96(7):1911–1930.
4. КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ НИЗКОГО СТАТУСА ВИТАМИНА D
|
|
В последние годы отмечается резкое повышение инте- |
||||||
|
реса к изучению роли витамина D в организме человека. |
|||||||
|
Это связано с тем, что накоплены и вновь появляются |
|||||||
|
данные не только о костных (кальциемических) эффектах |
|||||||
|
витамина D, но и о совершенно новых его проявлениях — |
|||||||
|
внекостных (некальциемических). Согласно современным |
|||||||
|
представлениям, дефицит витамина D связан с повышен- |
|||||||
|
ным риском развития сахарного диабета, артериальной |
|||||||
|
гипертензии, сердечной |
недостаточности, заболеваний |
||||||
|
периферических артерий, острого инфаркта миокарда, |
|||||||
|
различных форм рака, аутоиммунных и воспалительных |
|||||||
|
заболеваний, снижением иммунной защиты организма |
|||||||
|
и повышением уровня смертности (рис. 4.1) [1]. Эти иссле- |
|||||||
|
дования являются результатом понимания, что витамин D |
|||||||
|
не является витамином в классической интерпретации. Он |
|||||||
|
представляет собой стероидный прегормон с аутокрин- |
|||||||
|
ным, паракринным и эндокринным действием, который |
|||||||
|
с помощью ферментативных процессов последовательно |
|||||||
|
превращается в организме в биологически активные мета- |
|||||||
|
болиты, влияющие на различные органы и ткани посред- |
|||||||
|
ством геномных и негеномных эффектов [2]. |
|||||||
18 |
||||||||
|
|
|
|
|
|
|
||
|
Рис. 4.1. Возможные последствия костных и внекостных |
|||||||
|
проявлений недостаточности и дефицита витамина D [1] |
|||||||
|
|
|
|
|
|
|
||
|
|
|
Возможные последствия |
|
||||
|
|
|
низкого статуса витамина D |
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Костные проявления |
|
Внекостные проявления |
|
|||
|
|
|
|
|
|
|
|
|
Рахит |
|
Остеомаляция |
|
и остеопороз |
|
|
|
|
|
|
|
Повышенный риск воспалительных, аутоиммунных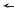 и инфекционных заболеваний
и инфекционных заболеваний
Повышенный риск метаболического синдрома и сердечно-сосудистых заболеваний
Повышенный риск психических заболеваний
Повышенный риск онкопатологии
4.1. Костные (кальциемические) проявления низкой обеспеченности организма витамином D
Основными проявлениями низкой обеспеченности витамином D в классическом понимании остаются рахит, остеомаляция и остеопороз.
4.1.1. Рахит
Рахит — нарушение минерализации растущей кости, обусловленное временным несоответствием между потребностями растущего организма в фосфоре и кальции и недостаточностью систем, обеспечивающих их доставку в организм ребенка [3–8].
В2016 году принят Глобальный консенсус по профилактике и лечению рахита алиментарной этиологии, который дает схожее определение рахита: нарушение дифференцировки хондроцитов, минерализации зон роста и остеоида у детей, вызванное дефицитом витамина D и/или недостаточным поступлением кальция [9]. Таким образом, основным этиологическим фактором возникновения рахита являются дефицит поступления витамина D с пищей, дефицит кальция, дефицит фосфора и ацидоз дистальных почечных канальцев [10].
Вданной Национальной программе рассматривается рахит, возникший в результате недостаточного поступления витамина D и кальция с пищей или рахита алиментарной этиологии.
Случаи рахита описаны во всех странах мира, включая страны Африки и Азии. Учитывая костные проявления рахита, его частота среди детей раннего возраста колеблется, по данным разных авторов, от 1,6 до 35% [10]. В последние годы нарушения минерализации нередко выявляются
удетей подросткового возраста, особенно при дефектах питания, а также у темнокожих жителей южных регионов, переехавших в европейские страны.
Существуют группы риска по развитию рахита (табл. 4.1).
Всилу быстрого роста и активности процессов перестройки костной ткани у детей первых лет жизни, особенно
унедоношенных, имеется высокая потребность в фосфатнокальциевых солях и витамине D при относительной незрелости механизмов, осуществляющих доставку и отложение этих минеральных веществ в кость. Отмечается недостаточная минерализация костного матрикса, прежде всего в метафизарных зонах роста [10–13].
Таблица 4.1. Группы риска по развитию рахита алиментарной этиологии
Фоновые состояния |
Патологические состояния |
|
|
Отягощенная наследственность по нарушениям фосфорно-кальциевого обмена. |
Синдром мальабсорбции (целиакия, |
Недоношенность. |
гастроинтестинальная форма |
Морфофункциональная незрелость. |
пищевой аллергии, экссудативная |
Внутриутробная гипотрофия. |
энтеропатия и др.). |
Многоплодная беременность. |
Применение антиконвульсантов |
Повторные роды с малыми промежутками между ними. |
у детей с судорожным синдромом. |
Вскармливание неадаптированными смесями. |
Хроническая патология почек, |
Снижение двигательной активности (тугое пеленание, длительная иммобилизация). |
печени, желчевыводящих путей. |
Недостаточная инсоляция. |
Частые респираторные заболевания |
Смуглая кожа. |
|
Заболевания эпидермиса |
|
|
|

Остеомаляция — нарушение минерализации костного |
|
вых 6 месяцев жизни составляет не менее 400 мг/сут- |
|
|||
матрикса в уже созревшей костной ткани — хотя и присут- |
|
ки. Содержание фосфора в грудном молоке колеблется |
|
|||
ствует у детей с рахитом, данный термин обычно исполь- |
|
от 5 до 15 мг/дл, и дети первых месяцев жизни за сутки |
|
|||
зуется для описания нарушений минерализации костной |
|
получают от 50 до 180 мг фосфора. Для детей первого |
|
|||
ткани после завершения роста [9]. |
|
полугодия необходимое количество фосфора составляет |
|
|||
|
|
|
не менее 300 мг. Дефицит кальция и фосфора в рационе |
|
||
Факторы, обусловливающие развитие рахита у детей |
|
и нарушение их соотношения возможны при несоблю- |
|
|||
1. Высокие темпы роста и развития детей в раннем возрас- |
|
дении принципов рационального питания у детей, нахо- |
|
|||
те и повышенная потребность в минеральных компонен- |
|
дящихся на искусственном вскармливании, или при |
|
|||
тах, особенно у недоношенных детей. Увеличение темпов |
|
пролонгировании естественного вскармливания [10]. |
|
|||
роста у детей происходит весной (по сравнению с осенни- |
|
Длительное вскармливание грудным молоком на фоне |
|
|||
ми месяцами), что в условиях высоких темпов прибавки |
|
позднего введения прикорма (в 7–8 месяцев и позже) |
|
|||
массы у детей раннего возраста, особенно на первом году |
|
не позволяет избежать развития у ребенка гиповитами- |
|
|||
жизни, повышает их потребность в минеральных компо- |
|
ноза даже при соблюдении кормящими матерями полно- |
|
|||
нентах в этот период и способствует развитию рахита. |
|
ценной сбалансированной диеты [15]. |
|
|||
2. Дефицит кальция и фосфора в пище, связанный с |
|
В табл. 4.2 представлены основные продукты, являющи- |
|
|||
дефектами питания. Обмен кальция и фосфатов име- |
|
еся источником витамина D. |
|
|||
ет особое значение в антенатальном периоде жизни. |
|
Данные о содержании витамина D в некоторых отече- |
|
|||
Повышенный риск недостаточности кальция у беремен- |
|
ственных пищевых продуктах представлены в табл. 4.3. |
|
|||
ной и, как следствие, у ребенка в период его внутриутроб- |
|
Накоплены факты, подтверждающие существенное зна- |
|
|||
ного развития возникает, если женщина не употребляет |
|
чение в патогенезе рахита и других пищевых веществ. Так, |
|
|||
по разным причинам молочные продукты (вегетариан- |
|
доказано отрицательное влияние дефицита в пищевом |
|
|||
ство, аллергия на белки молока, лактазная недостаточ- |
|
рационе витаминов А, С, группы В (особенно В1, В2, В6), |
|
|||
ность и др.), при ограничении в питании мяса, рыбы, яиц |
|
фолиевой кислоты, таких микроэлементов, как цинк, |
|
|||
(дефицит белка), при избытке в пище клетчатки, фосфа- |
|
медь, железо, магний, марганец и др. Кроме того, рахит |
|
|||
тов, жира, приеме энтеросорбентов [14]. |
|
легче возникает и тяжелее протекает при избыточном |
|
|||
Достаточных запасов кальция и фосфора во время бере- |
|
употреблении однообразной пищи, в том числе муч- |
|
|||
19 |
||||||
менности, как правило, не бывает, так как энергети- |
|
ных изделий (макароны, каши и т. д.), из-за наличия |
||||
|
|
|||||
ческая ценность среднесуточных рационов питания |
|
в зерновых продуктах фитиновой кислоты, образующей |
|
|||
обследованных женщин составляет 1500–1800 ккал при |
|
в кишечнике нерастворимые соли с кальцием, уменьшая |
|
|||
рекомендуемом потреблении 2500–3000 ккал/сутки. Они |
|
тем самым его всасывание [19]. |
|
|||
употребляют недостаточное количество мяса, молочных |
3. Нарушение всасывания кальция и фосфатов в кишеч- |
|
||||
продуктов, животного масла, овощей и фруктов. В резуль- |
|
нике, повышенное выведение их с мочой или наруше- |
|
|||
тате остеопения (по данным УЗ-остеометрии) выявляет- |
|
ние утилизации в кости, обусловленные незрелостью |
|
|||
ся у 10% новорожденных, родившихся от здоровых мате- |
|
транспортных систем в раннем возрасте или заболевани- |
|
|||
рей, и у 42% детей, родившихся у женщин с гестозом [10]. |
|
ями кишечника, печени и почек. У детей с низкой массой |
|
|||
В грудном молоке содержание кальция колеблет- |
|
тела при рождении развитие рахита связано с дефици- |
|
|||
ся от 15 до 40 мг/дл, и дети первых месяцев жизни |
|
том фосфатов на фоне усиленного роста и малого коли- |
|
|||
за сутки получают от 180 до 350 мг кальция. В то же |
|
чества этого иона в пище, причем успешное излечение |
|
|||
время необходимое количество кальция для детей пер- |
|
рахита обеспечивается увеличением фосфатов в пище |
|
|||
Таблица 4.2. Источники витамина D [16, 17] |
|
|
|
|
||
|
|
|
|
|
|
|
|
Продукты |
|
Содержание витамина D3 |
|
|
|
|
Рыбий жир |
|
400–1000 МЕ/1 ч. л. |
|
|
|
|
|
|
|
|
|
|
|
Печень трески |
|
4000 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
Необогащенные |
Лосось свежий, дикий |
|
600–1000 МЕ/100 г |
|
|
|
|
|
|
|
|
||
Лосось свежий, аквакультура |
|
100–250 МЕ/100 г |
|
|
||
|
|
|
|
|||
|
|
|
|
|
|
|
|
Лосось консервированный |
|
300–600 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Сардина консервированная |
|
300 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Макрель консервированная |
|
250 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Тунец консервированный |
|
236 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Грибы шиитаке свежие |
|
100 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Желток куриного яйца |
|
20 МЕ/1 желток |
|
|
|
|
|
|
|
|
|
|
|
Молоко |
|
100 МЕ/230 мл |
|
|
|
|
|
|
|
|
|
|
Обогащенные |
Детская молочная смесь |
|
100 МЕ/230 мл |
|
|
|
|
|
|
|
|
||
Йогурт |
|
100 МЕ/230 мл |
|
|
||
|
|
|
|
|||
|
|
|
|
|
|
|
|
Сливочное масло |
|
56 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Маргарин |
|
429 МЕ/100 г |
|
|
|
|
|
|
|
|
|
|
|
Сыр |
|
100 МЕ/85 г |
|
|
|
|
|
|
|
|
|
|
|
Злаки для завтрака |
|
~100 МЕ/1 порция |
|
|
|
|
|
|
|
|
|
|
|
Апельсиновый сок |
|
100 МЕ/230 мл |
|
|
|
|
|
|
|
|
|
|