Материал: Молекулярно-генетическая характеристика рекомбинантных форм вируса иммунодефицита человека 1 типа, выявленных на территории Республики Беларусь
Наконец, для закрепления рекомбинации такие вирусы должны эффективно реплицироваться в новых клетках-мишенях. Большинство случаев переключения между РНК-матрицами являются комплементарными, то есть точки разрыва у матричной и синтезируемой молекулами совпадают [57, 78]. Однако, поскольку рекомбинанты содержат участки геномов каждого из «родителей», эти последовательности могут или не могут работать вместе эффективно [69, 79]. Особенно это выражено в случае, когда два родительских вирусных генома разделены большим генетическим расстоянием (например, когда родительские вирусы относятся к различным субтипам или группам). По этой причине многие вновь созданные межсубтипные рекомбинантные формы вирусов устраняются путем естественной селекции во время репликации вируса [59]. Создание жизнеспособной межсубтипной рекомбинантной формы сталкивается с множеством проблем: возможное снижение эффективности соупаковывания РНК, относительно неэффективное переключение между РНК-матрицами, а также снижение репликации. Тем не менее, согласно консервативной оценке, около 20% всех циркулирующих в настоящее время вариантов ВИЧ являются межсубтипными рекомбинантными формами ВИЧ[80]. Это доказывает, что рекомбинация является основной движущей силой эволюции в популяцииВИЧ.
1.6 Рецепторы и тропизм ВИЧ
Первый рецептор ВИЧ, CD4 (clusterofdifferentiation 4), был идентифицирован уже в 1984 г.[81-83]. Вскоре после этого выяснилось, что одного CD4 недостаточно для проникновения ВИЧв клетку-мишень. Первым результатом поиска других рецепторов, важных для проникновения ВИЧ, стало открытие в 1995 г. трех хемокинов подсемейства СС: RANTES (CCL5), MIP-1a (CCL3) и MIP-1b (CCL4), которые продемонстрировали сильное ингибирование ВИЧ-инфекции in vitro[84]. В марте следующего года хемокиновый рецептор CXCR4 был идентифицирован, как необходимый для связывания ВИЧкорецептор [85]. Эти открытия стимулировали целую серию исследований, и в этом же году был открыт второй корецептор ВИЧ- CCR5[86-89]. Также был открыт и специфический лиганд для CXCR4 - SDF-1 (CXCL12) [90, 91]. Третьим важным открытием в этот короткий период стало обнаружение, что делеция размером в 32 нуклеотида в участке, кодирующем ген CCR5 (CCR5-D32), приводит к резистентности к ВИЧ[92, 93].
ВИЧможет инфицировать различные клетки, такие как Т-лимфоциты и макрофаги, которые экспрессируют молекулу CD4 на поверхности мембраны. Тропизм ВИЧраньше обозначал тип клетки, которую ВИЧинфицировал и в которой размножался. Так, в исследованиях биологических свойств ВИЧбыло обнаружено, что изоляты ВИЧ, выделенные от пациентов на ранней стадии ВИЧ-инфекции, обычно способны инфицировать макрофаги и первичные культуры CD4+ Т-лимфоцитов, но не способны размножаться в трансформированных Т-клеточных линиях[94, 95]. Для обозначения таких вирусов применялись термины М-тропный (макрофаготропный), NSI-изолят (от англ. non-sincytium inducting), то есть не способный образовывать синцитий, а также SL-изолят (от англ. slow/low - медленно/низко) - из-за низкой скорости репликации в Т-клеточных линиях [96, 97]. Спустя несколько лет после инфицирования, у пациентов образуются штаммы ВИЧ, которые способны размножаться в Т-клеточных линиях, при этом либо сохраняя, либо теряя способность инфицировать макрофаги. Такие штаммы ВИЧназывались Т-тропными, SL-изолятами (от англ. sincytium inducting), RH-изолятами (от англ. rapid/high - быстро/высоко) [98], или вирусами с двойным тропизмом [99]. После открытия корецепторов ВИЧстали понятны причины различия биологических свойств вируса: М-тропный вирус использует в качестве корецептора CCR5, T-тропные штаммы ВИЧиспользуют в качестве корецептора CXCR4 или оба корецептора. [100]. Современная фенотипическая классификация ВИЧоснована на использовании этих корецепторов: корецептор CCR5 - R5 вирус, CXCR4 - Х4 или R5X4 вирус, если ВИЧ использует 2 корецептора [101]. Использование того или иного корецептора вирусом определяется областью V3 белка gp120[102-104].
.7 Патогенез ВИЧ-инфекции
Течение ВИЧ-инфекции при отсутствии антиретровирусной терапииможно
разделить на 3 стадии: острую, хроническую и СПИД (рисунок 1.5)[105].
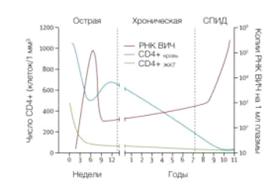
Острая (симптомная) фаза обычно начинается спустя две недели с момента инфицирования и длитсяоколо месяца. Наблюдаются симптомы, характерные для гриппа: повышение температуры тела, ломота, а также увеличение лимфатических узлов. В этой фазе ВИЧстремительно распространяется к лимфоузлам желудочно-кишечного тракта, в котором происходит быстрое истощение пула CD4+ЖКТ Т-лимфоцитов. Это возникает как из-за естественного истощения пула, так и в результате опознавания натуральными киллерами (НК) инфицированных клеток с помощью киллер-подобных иммуноглобулиновых рецепторов (KIRs) [106].
Острая фаза также характеризуется значительным ростом количества вируса в крови (вирусной нагрузки), доходящей до 105-106копий РНК ВИЧ/мл плазмы крови. В конце острой фазы наступает стабилизация ВИЧ-инфекции вследствие антивирусного иммунного ответа и переход ее в хроническую (латентную) фазу.
Иммунный ответ снижает вирусную нагрузку до ~3x104 копий РНК ВИЧ/мл плазмы (так называемый сет-поинт) [107]. Тем не менее уровень CD4+ Т-лимфоцитов периферической крови продолжает снижаться из-за постоянного восполнения пула погибших клеток, что приводит к истощению иммунной системы. Кроме этого, в хронической фазе ВИЧ-инфекции создается вирусный резервуар из пула инфицированных клеток. Это долгоживущие, невосприимчивые к ВААРТ Т-клетки памяти, макрофаги и дендритные клетки [108]. Хроническая фаза может длиться до 10 лет, на продолжительность времени влияют как генетические особенности организма, так и вирусные факторы. Сам пациент не испытывает каких-либо симптомов, однако наблюдается хроническая активация иммунной системы, в частности повышение уровня активированных клеток иммунной системы и воспалительных цитокинов.
Когда уровень CD4+ Т-лимфоцитов снижается до 200 клеток в 1 мкл крови и менее, наступает стадия СПИД. Развитие данной стадии характеризуется прогрессивной генерализированной лимфаденопатией, оппортунистическими инфекциями (напр. пневмоцистная пневмония) и нетипичными онкологическими заболеваниями (напр. саркома Капоши). Без ВААРТ пациенты со СПИД обычно живут не более трех лет, а при диагностировании опасной оппортунистической инфекции ожидаемый период жизни пациента снижается до одного года [105].
.8 Терапия ВИЧ-инфекции
В 1987 г. появился первый антиретровирусный препарат зидовудин, нуклеозидный ингибитор обратной транскриптазы (НИОТ). Изначально он был синтезирован как средство против рака, но в дальнейшем было обнаружено, что он блокирует обратную транскрипцию ВИЧ[109,110]. Однако к данному препарату очень быстро развивалась резистентность, и в первые годы, когда зидовудин назначали в очень высоких дозах (1500 мг/сутки), наблюдалось выраженное угнетение кроветворения [111]. В начале 1990-х годов были синтезированы и начали применяться первые ингибиторы протеазы (ИП) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ), однако только в 1997 г. были опубликованы статьи [112, 113], в которых говорилось о существенном преимуществе комбинированной терапии, включающей 2 НИОТ и ИП(индинавир). Такая комбинированная терапия минимум трех различных антиретровирусных препаратов стала называться высокоактивной антиретровирусной терапией (ВААРТ), поскольку она значительно снижала заболеваемость оппортунистическими инфекциями и, как следствие, смертность от ВИЧ-инфекции [114].
По состоянию на март 2011 г. для лечения ВИЧ-инфекции разрешены к применению 30 отдельных и комбинированных препаратов, направленных на подавление репликации вируса. Эти препараты принадлежат к пяти фармакологическим группам:
. нуклеозидные и нуклеотидные ингибиторы обратной транскриптазы (НИОТ);
. ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ);
. ингибиторы протеазы (ИП);
. ингибиторы проникновения (блокаторы корецепторов и ингибиторы слияния);
. ингибиторы интегразы (ИИ).
В Республике Беларусь до недавнего времени применялись только 3 из 5 групп препаратов: НИОТ, ННИОТ и ИП. В 2015 году началось применение одного препарата из группы ИИ.
Несмотря на свою высокую эффективность, ВААРТ не приводит к полномуизлечению пациента от ВИЧ, поэтомуприем препаратов необходим на протяжении всей жизни ВИЧ-инфицированного. В настоящее время исследования в области терапии ВИЧ-инфекции направлены как раз на то, чтобы элиминировать латентные клетки, содержащие провирус ВИЧв своем геноме [115].
.9 Генетическое разнообразие ВИЧ
Одними из основных особенностей ВИЧявляются высокие генетическое разнообразие и скорость эволюции вируса. Это обусловлено, по крайней мере, тремя факторами: множественным проникновением ВИЧв человеческую популяцию, низкой точностью и высокой рекомбиногенностью вирусной обратной транскриптазы, а также высокой скоростью размножения вируса [116]. Время жизни ВИЧв плазме крови и ВИЧ-продуцирующих клетках составляет 1-2 дня, и за это время образуется порядка 1010 новых копий вируса [117, 118]. Особенностью обратной транскриптазы ВИЧявляется отсутствие репарационной активности и, как следствие, генерация большого числа «ошибок» при репликации: 1-4 нуклеотидных замены/геном/раунд репликации [119]. Другая особенность обратной транскриптазы ВИЧ- способность «перескакивать» с одной цепи РНК на другую, вызывая рекомбинацию генома вируса [55]. Рекомбинация - один из наиболее значимых факторов, ускоряющих эволюцию ВИЧ, и она происходит, по разным расчетам, от 2 до 9 раз/геном/раунд репликации [27, 57, 120, 121].
Высокий уровень генетического разнообразия ВИЧпривел к тому, что стало необходимо классифицировать различные генетические варианты вируса. Для классификации ВИЧиспользуется метод филогенетического анализа нуклеотидных последовательностей их геномов. Данная методика позволяет определить степень родства нуклеотидов и, как следствие, самих вирусов.
Согласно современной филогенетической классификации, ВИЧделится на типы, группы, субтипы и рекомбинантные формы (рисунок 1.6). Различают 2 типа ВИЧ: первый и второй (ВИЧ-1 и ВИЧ-2 соответственно). ВИЧ-1 родственен с вирусами, найденными у горилл и шимпанзе, обитающих в Западной Африке, а источником ВИЧ-2 являются черные мангобеи [2]. Филогенетический анализ показал, что внутри первого типа изоляты ВИЧ-1 образуют 4 кластера, названных группами M, N, O и P [1, 122, 123].
Группа М (major) - в нее входит подавляющее большинство штаммовВИЧ-1. В свою очередь, группа М разделяется на субтипы (подгруппы) и рекомбинантные формы. В настоящее время выделяют 9 субтипов ВИЧ, обозначающихся A (A1-A4), B, C, D, F (F1 и F2), G, H, J и K. Сиквенсы внутри субтипа или суб-субтипа более близки между собой, чем с сиквенсами других субтипов на протяжении всего их генома. Рекомбинантные формы ВИЧ-1 являются результатом рекомбинации геномов различных субтипов. Рекомбинантная форма ВИЧ-1 называется циркулирующей, если описано не менее трех, эпидемиологически не связанных случаев инфицирования вирусом с идентичной рекомбинантной структурой и охарактеризовано не менее двух полноразмерных геномов данного вируса. Циркулирующим рекомбинантным формам присваивается название по очередности их открытия с последующим указанием субтипов, из которых состоит данный геном. Сегменты, для которых невозможно определить родительский субтип, обозначаютсябуквой U (от англ. unclassified). Если рекомбинантная форма состоит из трех и более различных субтипов ВИЧ, то такой форме присваивается аббревиатура «cpx»(от англ. complex). В настоящее время выявлено 72 ЦРФ ВИЧ-1 и 1 ЦРФ ВИЧ-2 [124]. Уникальные рекомбинантные формы выявлены только у единичных, эпидемиологически связанных пациентов (например: мать-ребенок).
Вирусы группы О (outlier), вероятнее всего, передались в человеческую популяцию от диких горилл [125] и наиболее распространены в Камеруне, где в 1997 году более 2% пациентов были заражены вирусами данной группы,и в соседних центральноафриканских странах [126].
Группа N (non-M, non-O) представлена вирусами, циркулирующими только в Камеруне [127]. В 2011 г. единичный случай выявлен также во Франции.
Вирус группы P был впервые обнаружен в 2009 г. в Камеруне у ВИЧ-инфицированной женщины. Генетически этот вариант ВИЧ-1 близок к вирусу иммунодефицита горилл (SIVgor) и не проявлял никаких признаков рекомбинации с другими известными группами[122].Исследователи предположили, что данный вирус образует новую группу ВИЧ, не относящуюся к уже известным группам M, N или O. Позже данное предположение было подтверждено другой группой исследователей, которые обнаружили второй ВИЧ, принадлежащий к группе P. Этот вирус был выявлен у ВИЧ-серопозитивного пациента мужского пола в больнице Камеруна, подтверждая таким образом, что ВИЧ-1 группы P реплицируется в организме человека [123].
Различные генетические формы ВИЧ-1 зачастую локализованы в отдельных географических регионах. Наиболее часто встречаемые формы вируса - ВИЧ-1 субтипа А1 (12,3% всех случаев ВИЧ-инфекции в мире), субтипы B (10,2%), C (49,9%) и G (6,3%), а также CRF01_AE (4,7%) и CRF02_AG (4,8%) (рисунок 1.7)[128].В Северной Америке, Западной Европе и Австралии превалирующим является ВИЧ-1 субтипа B, в странах бывшего СССР - субтипа А1 и CRF03_AB. Доминирующий в пандемии ВИЧ-1 субтипа С локализованв основном в Южной и Восточной Африке, а также в Индии, где наблюдается наиболее сложная ситуация с эпидемией ВИЧ-1 в мире. Среди ЦРФ ВИЧ-1 превалирующей считается CRF02_AG, которая является наиболее часто встречаемой формой ВИЧ-1 в Западной Африке. Для сравнения, в других регионах нигде не наблюдается такой высокой превалентности рекомбинантных форм над «чистыми» субтипами ВИЧ-1. Очевидным исключением из регионального превалирования субтипов ВИЧ-1 является регион Западной и Центральной Африки, в котором наблюдается широкая вариабельность генетических форм ВИЧ-1 [124]. Это также может свидетельствовать о попаданииВИЧ-1 в человеческую популяцию именно в этом районе [129, 130].
Распространение ВИЧ-1 на территории стран бывшего СССР
Первые случаи ВИЧ-инфекции на территории СССР были зарегистрированы в 1987 г. в Ленинграде (совр. Санкт-Петербург) [131] и до 1994 г., уже после распада СССР, эпидемия ВИЧна этой территории носила случайный характер. У пациентов, выявленных в данный период на территории Российской Федерации, было обнаружено 8 субтипов ВИЧ-1: А1, В, С, D, E, F, G и H, доминирующим из которых являлся ВИЧ-1 субтипа B[132]. Вторым по значимости был субтип G, вызвавший вспышку ВИЧ-инфекции в Элисте, Республика Калмыкия[133]. Остальные субтипы выявлялись значительно реже и были связаны в основном с половым путем передачи [134].Все выявляемые вирусы не были генетически близкими друг другу, что свидетельствовало о множественном проникновении вируса на территорию России [135].
Эпидемия ВИЧ на территории бывшего СССР началась в 1994-1996 гг. и была вызвана стремительной передачей вируса среди потребителей инъекционных наркотиков. Эпидемия началась в южных городах Украины: г. Одесса (3500 случаев ВИЧ-инфекции среди ПИН) и г. Николаев (2000 случаев передачи среди ПИН,зарегистрированных с 1994 по 2000 гг.) [136, 137]. В дальнейшем эти варианты вируса вызвали вспышки эпидемии ВИЧв других городах Украины (Киев, Донецк), России (Санкт-Петербург, Саратов, Пермь и др.) [138, 139] и Беларуси (Светлогорск) [140]. Позже вспышки ВИЧ-инфекции среди ПИН выявились на территориях других стран бывшего СССР, включая Балтийский регион: Латвия, Литва и Эстония[141-143], Кавказ: Азербайджан и Грузия [144,145], Центральная Азия: Казахстан, Узбекистан, Дагестан и Таджикистан [146-148], a также на территории Молдовы [149]. Подавляющее большинство вирусов было выявлено среди потребителей инъекционных наркотиков, и эти варианты вируса относились к крайне генетически гомогенному варианту ВИЧ-1 субтипа А1, названному AFSU (или AIDU) [136]. Данный вариант вируса быстро стал преобладающим на территориях всех этих государств, за исключением Эстонии, в которой доминирующим является рекомбинантная форма CRF06_cpx [150]. Хотя первые вспышки ВИЧ-инфекции были зарегистрированы в конце 1994 г. на юге Украины, ретроспективный анализ образцов, собранных в Одессе в 1993 г., выявил несколько случаев инфицирования вариантом ВИЧ, филогенетически близким к AFSU, однако данный вариант имел более низкий уровень распространения и передавался в основном половым путем [151].
Вариант вируса AFSU впоследствии стал одним из родительских форм вируса для рекомбинантной формы, вызвавшей вспышку ВИЧ-инфекции в Калининграде - CRF03_AB. Позже был идентифицирован второй родительский вариант: ВИЧ-1 субтипа B - популяция вирусов, названная BFSU (или BIDU) [152]. Данная популяция вирусов была выявлена в другом южном украинском городе - Николаеве. Штаммы данного вируса также отличались чрезвычайно низким уровнем генетического разнообразия, характерным для общего источника заражения. При этом не удалось показать близкое генетическое родство данного варианта ни с одним штаммом субтипа В, обнаруженным ранее в странах бывшего СССР, Западной Европе или США. Предположительно, источником этой вспышки мог быть штамм ВИЧ-1 из Польши [153].
На сегодняшний день ВИЧ-1 субтипа А1 по-прежнему остается доминирующим на территории стран бывшего СССР:в Латвии[154], Литве, Украине [155], Российской Федерации[156], стран Кавказского региона[146, 148, 157, 158]. Исключениеиз этого списка - Эстония, где превалирующим вариантом ВИЧ-1 является циркулирующая рекомбинантная формаCRF06_cpx. Ожидаемо, генетические дистанции между вирусами субтипа А1 увеличились, с 1-3 до 6-8%, как из-за естественного вирусного разнообразия, так и из-за изменения основного пути передачи вируса с внутривенного введения наркотических средств на гетеросексуальный путь [160, 161].
Происхождение варианта ВИЧ-1 AFSU
Вариант AFSUпредставляет одну из самых больших групп ВИЧ, идентифицированных в глобальной пандемии, что привело к одной из самых быстро растущих эпидемий ВИЧ-1 в мире. Происхождение этого варианта до сих пор вызывало вопросы из-за противоречивых предложенныхгипотез. В 2007 г. М. Томсон с соавторами филогенетически выявили сиквенсы из Демократической Республики Конго (ДРК), которые формировали кластер вместе с образцами ВИЧ-1 из Санкт-Петербурга, Россия, полученными в 1992-1994 гг. от пациентов, заразившихся ВИЧ-1 гетеросексуальным путем. Образцы из ДРК находились в основании кластера, что свидетельствовало об их анцестральности по отношению к AFSU[151].