Материал: Меледина Т.В., Давыденко С.Г. Дрожжи Saccharomyces cerevisiae. Морфология, химический состав, метаболизм
Кроме того, после предварительного гидролиза до моносахаров дрожжи утилизируют сахарозу, мальтозу, мальтотриозу, а также внутренние углеводные резервы трегалозу и гликоген.
Гликолиз (рис. 5.1) начинается с фосфорилирования глюкозы и образования за счет макроэргической связи АТФ глюкозо-6- фосфата (Гл-6-Ф).
Источником D-глюкозы также служит гликоген, который является субстратом для фермента, отщепляющего гликозидные остатки с концов полисахаридных цепей гликогена. Следующая реакция на этом пути – изомеризация Гл-6-Ф во фруктозо-6-фосфат (Ф-6-Ф), осуществляемая глюкозофосфат изомеразой (ЕС 5.3.1.9). Эта реакция обратима.
Фр-6-Ф также образуется из фруктозы, поступающей непосредственно из питательной среды, а также при гидролизе сахарозы.
Третий фермент гликолитического пути, 6-фосфофруктокиназа, осуществляет образование Фр-1,6-дифосфата (Ф-1,6-Ф) из Фр-6-Ф и АТФ.
При этом на каждую молекулу глюкозы, вошедшую в цепь, потребляется две молекулы АТФ. Затем фруктозо-дифосфат-альдолаза
– фермент, содержащий цинк, катализирует обратимое расщепление шестиуглеродной молекулы на две трехуглеродные – дегидроацетонфосфат и D-глицеральдегид-3-фосфат. Только последняя молекула подвергается дальнейшим превращениям по пути ЭМП,
иравновесие между двумя триозофосфатами поддерживается триозофосфатизомеразой.
Далее D-глицеральдегид-3-фосфат идет на образование 1,3-дифосфоглицерата при участии фермента глицеральдегид-фосфат дегидрогеназы. Для этой реакции требуется источник неорганического фосфата. Это первая реакция в гликолитической цепи, которая включает окисление субстрата. Более того, это первая реакция, в которой образуется макроэргическая связь и свободная энергия окислительного процесса запасается в этой связи. На следующей ступени происходит перенос энергии этой связи на АДФ, так что образуется АТФ и 3-фосфо-D-глицерат, реакция катализируется фосфоглице- рат-киназой. На этом участке цепи из каждой вошедшей в нее молекулы D-глюкозы или D-фруктозы образуются две молекулы АТФ
идве молекулы НАДН2.
41
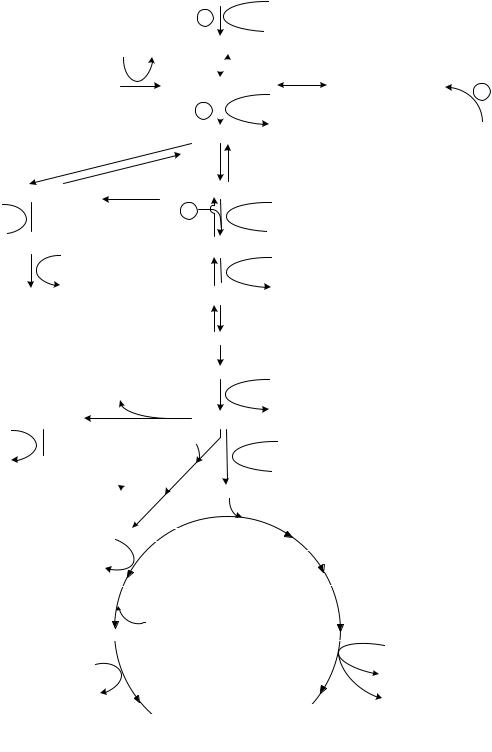
Метаболизм глюкозы в анаэробных условиях глюкоза АТФ
АТФ |
АДФ |
фруктоза
P
 АДФ
АДФ
глюкозо- 6-фосфат
|
|
|
|
[Zn] |
Глюкозо-1-фосфат |
|
|
|
|
|
|
||
|
|
|
||||
|
|
|
|
|||
Фруктоза-6-фосфатАТФ |
P |
|||||
P |
|
|
|
|
+(гликоген)n-1 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
АДФ |
|
(Гликоген)n |
|
фруктоза-1,6-дифосфат |
|
|||||
диоксиацетон-фосфат НАДН2
НАД 
 глицеро-3-фосфат
глицеро-3-фосфат
Н2О
Н3РО4
глицерин
ацетальдегид НАДН2
 глицеральдегид-3-фосфат
глицеральдегид-3-фосфат
НАД
P
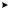 НАДН2
НАДН2
1,3-дифосфоглицерат АДФ
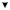 АТФ 3-Ф-глицерат
АТФ 3-Ф-глицерат
2-Ф-глицерат
фосфоенолпируватАДФ
СО 2
|
пируват |
АТФ |
СО |
|
|
[Zn] |
|
|
АТФ 2 |
НАД |
НАД 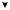 спирт
спирт
АДФ 
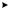 НАДН 2
НАДН 2
ацетил-КоА
й |
|
ы |
|
н |
|
ь |
|
л |
|
е |
|
т |
путь |
о |
|
и |
|
в |
|
н |
|
а |
|
т |
|
с |
|
с |
|
во |
|
|
НА |
|
|
|
|
|
|
|
|
|
|
|
оксалоацетат |
||||
|
Д |
Н |
|
|||||
|
|
|
2 |
|
|
|
||
|
НАД |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
малат |
|
|
|
|
|
|
|
|
Н2О |
||
|
|
|
|
фумарат |
||||
ДН |
|
|
|
|
|
|
||
ФА |
2 |
|
|
|
|
|
|
|
|
АД |
|
|
|
|
|
|
|
Ф |
|
|
|
|
|
|
|
|
|
|
|
|
сукцинат |
|
|||
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
цитрат |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
цис-аконитат |
|
о |
|||
|
|
|
|
|
|
|
|
к |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
и |
|
|
|
|
|
|
|
путь |
сл и |
|
|
|
|
|
|
|
|
те |
|
|
|
|
|
|
|
|
л |
|
|
|
|
|
|
|
|
ь |
|
|
|
изоцитрат |
|
|
|||
|
|
|
|
|
н |
|||
|
|
|
|
|
|
|
НА |
ы |
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
й |
|
|
|
|
|
|
|
|
ДФ |
|
|
|
|
|
|
|
|
НАДФН |
|
|
|
|
|
|
|
|
2 |
|
|
2-оксоглутарат |
|
С |
|
||||
|
|
|
|
|
|
|
О |
|
|
|
|
|
|
|
|
2 |
|
Рис. 5.1. Метаболизм этанола и глицерина
42

С помощью фосфоглицеромутазы 3-фосфо-D-глицерат превращается в 2-фосфо-D-глицерат. Затем энолаза (ЕС 4.2.1.11) в качестве посредника способствует удалению воды из 2-фосфо-D-глицерата, что приводит к образованию фосфоэнолпировиноградной кислоты (ФЕП). Богатая энергией связь в фосфоэнолпирувате (до = – 61,9 кДж/моль) используется затем для фосфорилирования АДФ, в результате чего образуются АТФ и пировиноградная кислота. В этой точке на каждую молекулу включенной в метаболизм глюкозы возникают две молекулы АТФ и 2 молекулы НАДН2.
Таким образом, в результате прохождения гликолитического пути образуется запас энергии в виде двух молекул АТФ.
Глюкоза 2 Пируват + 2 АТФ + 2 НАДН2
В табл. 5.1 указаны ферменты, принимающие участие в гликолизе, их коферменты, активаторы и ингибиторы. Эти данные можно использовать для регулирования гликолиза при разработке технологии дрожжей, а также в других производствах, где используются дрожжи.
Таблица 5.1
Активаторы и ингибиторы гликолиза
Фермент |
Кофермент, |
|
Активатор, |
Ингибитор |
|
кофактор |
|
стимулятор |
|
|
|
|
|
|
Гексокиназа |
Mg+2 |
|
Mg+2, АДФ |
Г-6-Ф, |
|
|
|
|
ацетил-КоА, |
|
|
|
|
ФЕП, ЖК* |
Глюкозофосфат |
Mg+2 |
|
– |
АТФ, |
изомераза |
|
|
|
цитрат, |
|
|
|
|
ЖК* |
6-фосфофруктокиназа |
Mg+2 |
|
АДФ. АМФ, |
ФЕП, |
|
|
|
К+, NН4+ |
НАДН |
Фруктозо-дифосфат- |
– |
|
Zn+2 , Со+2, |
Цистеин |
альдолаза |
|
|
Fe+2, К+ |
|
Триозофосфат- |
Mg+2 |
|
– |
Hg+2 |
изомераза |
|
|
|
|
Глицеральдегид- |
Zn+2, НАД+ |
|
– |
Иодацетат, |
фосфатдегидрогеназа |
|
|
|
Mg+ |
|
|
43 |
|
|
|
|
|
Окончание табл. 5.1 |
|
|
|
|
Фермент |
Кофермент, |
Активатор, |
Ингибитор |
|
кофактор |
стимулятор |
|
|
|
|
|
Фосфоглицерат-киназа |
– |
Mg+2 |
– |
Фосфоглицеромутаза |
Mg+2, |
– |
– |
|
2,3-диф- |
|
|
|
глицерат |
|
|
Енолаза |
Mg +2, Mn+2 |
– |
F-, Ca+2 |
Пируватдекарбоксила- |
K+, Mg+2 |
Фр-1,6-Ф, |
Ca+2 |
за |
или Mn+2 |
Г-6-Ф |
АТФ, НАДН, |
|
|
|
ЖК*, ацетальдегид |
Гликогенфосфорилаза |
Р (неорга- |
Фосфосерин |
|
|
нический) |
|
|
|
пиридок- |
|
|
|
саль- |
|
|
|
фосфат |
|
|
Фосфоглюкомутаза |
Zn+2, |
Серин |
|
|
Гл-1,6 -Ф |
|
|
*ЖК – жирные кислоты. |
|
|
|
5.2. СПИРТОВОЕ БРОЖЕНИЕ
Гликолиз является первым этапом спиртового брожения. Образовавшаяся пировиноградная кислота декарбоксилируется при участии декарбоксилазы в ацетальдегид, который затем восстанавливается до этанола. Эта реакция осуществляется алкогольдегидрогеназой с участием НАДН2 (табл. 5.2). В ходе этой реакции НАДН2 окисляется до НАД+ (см. рис. 5.1), который далее вновь участвует в гликолизе. Именно за счет использования ацетальдегида в качестве конечного акцептора электронов клетка обеспечивает дальнейшее функционирование гликолитического пути и вследствие этого – дальнейшее образование АТФ для использования в биосинтетических реакциях.
Энергетический и химический баланс брожения:
С6 Н12 О6 + 2 АДФ + 2Фн 2СО2 + 2 СН3СН2 ОН + 2АТФ + +2 Н2О + 61 кДж
44
Таким образом, выход АТФ в пути ЭМП составляет 2 молекулы на молекулу глюкозы. Эффективность брожения составляет 26 %; 74 % энергии не удерживается клеткой и в основном рассеивается в виде тепла, поэтому следует применять охлаждение аппаратов. Скорость брожения непостоянна, и наибольшая активность наблюдается первые 24–36 ч. Затем ввиду ингибирования клеток этанолом этот процесс замедляется.
Таблица 5. 2
Активаторы и ингибиторы спиртового брожения
Фермент |
Кофермент, |
Активатор, |
Ингибитор |
|
кофактор |
стимулятор |
|
|
|
|
|
Пируватдекарбоксилаза |
Тиаминпирофосфат |
Тиамин, |
Ацеталь- |
|
|
Mg+2, Mn+2 |
дегид, |
|
|
или Со+2 |
О2 |
|
|
|
|
Алкогольдегидрогеназа |
НАДН, Zn+2 |
– |
– |
|
|
|
|
Для протекания спиртового брожения в питательной среде должны присутствовать тиамин (витамин В1), а также ионы Zn+2, Co+2, Mg+2 и Mn+2 (см. табл. 5.2). Например, увеличение концентрации ацетальдегида вследствие замедления его восстановления в этанол происходит из-за недостатка ионов Zn+2 в среде, в результате Ф-1,6-Ф идет на биосинтез глицерина (см. рис. 5.1). Кислород является ингибитором брожения (эффект Пастера), механизм этого процесса будет рассмотрен ниже.
Гликолитическая последовательность реакций является примером амфиболического пути, в ходе которого в биосинтетических реакциях клеткой используются различные промежуточные продукты:
–фосфорилированная глюкоза (Гл-1-Ф) является предшественником в синтезе полимеров клеточной стенки и резервных углеводов;
–триозофосфаты используются в синтезе жиров;
–фосфоенолпируват и пируват являются предшественниками некоторых аминокислот (рис. 5.2).
45