Материал: магістерський іспит з хімії 1
39. Фізико-хімічні методи дослідження речовин.
Усі фізичні і фізико-хімічні методи: Електрохімічні методи. Електроваговий аналіз ґрунтується на виділенні з розчинів електролітів речовин, що осаджуються на електродах при проходженні через розчин постійного електричного струму. Кондуктометрія ґрунтується на вимірюванні електропровідності розчинів, яка змінюється у результаті хімічної реакції і яка залежить від природи електроліту, його температури та концентрації розчину. Потенціометрія ґрунтується на вимірюванні потенціалу електроду, який змінюється внаслідок хімічної реакції і який занурений у розчин, що аналізується.
Спектральні (оптичні) методи. Емісійний спектральний аналіз ґрунтується на вивченні емісійних спектрів елементів речовини, яка аналізується (спектри випромінювання). Абсорбційна спектроскопія ґрунтується на вивченні спектрів поглинання речовини, яка аналізується, і являються її індивідуальною характеристикою.Інфрачервона спектроскопія – молекулярна оптична спектроскопія, яка вивчає спектри поглинання та відбиття електромагнітних хвиль в ІЧ-області. Фотоколориметрія ґрунтується на визначенні спектра поглинання або вимірюванні світлопоглинання у видимій ділянці спектра і на порівнянні інтенсивності забарвлення досліджуваного забарвленого розчину. Люмінесцентний або флуоресцентний метод ґрунтується на опромінених ультрафіолетовим світлом і вимірюванні інтенсивності випромінюваного ними видимого світла.
Хроматографічні методи ґрунтуються на вибірковому поглинанні (адсорбції) окремих компонентів суміші, яка аналізується, різними адсорбентами. При фронтальному аналізі досліджуваний розчин суміші речовин безперервно подають у верхню частину колонки і збирають окремі фракції фільтрату. Газовою хроматографією є процес, де рухомою фазою є газ (чи пар). Рідинною хроматографією є процес, де рухомою фазою є рідина. Тонкошарову хроматографію, що являє собою різновидність розподільної хроматографії, яка здійснюється на пластинках вкритих тонким шаром носія (алюміній оксид). Паперова хроматографія – різновид розподільної хроматографії, в якій носієм для нерухомого розчинника є смужки чи аркуші фільтрувального паперу, що не містить мінеральних домішок.
Радіометричні методи ґрунтуються на вимірюванні випромінювання атомами радіоактивних елементамів. Метод ізотопного розведення ґрунтується на розведенні сполуки, яка мічена радіоактивним ізотопом, неактивним компонентом суміші.Принцип методу радіоактиваційного аналізу, полягає в переводі стабільних ізотопів елемента у радіоактивні.
Мас-спектрометричні методи аналізу ґрунтуються на визначенні окремих йонізованих атомів, молекул та радикалів за допомогою розділення потоку йонів, що містять частинки з різним відношенням маси до заряду, в результаті комбінованої дії електричного та магнітного полів. Застосовують для визначення ізотопного складу елементів, вмісту різних радикалів, окремих компонентів в складних сумішах або домішок.
Ядерно-фізичні методи. Метод ядерного магнітного резонансу (ЯМР) ґрунтується на використанні резонансного поглинання електромагнітних хвиль досліджуваною речовиною у постійному магнітному полі, яке обумовлено ядерним магнетизмом. Метод ядерної гама-резонансної (ЯГР) спектроскопії ґрунтується на спостереженні мессбауровського ефекту. Метод ЯГР-спектроскопії використовується для встановлення характера хімічних зв’язків в речовинах, а також для дослідження комплексних та елементорганічних сполук.
40. Будова атома Карбону.
Положення Карбону у Періодичній системі елементів Д.І.Менделєєва обумовлює унікальні властивості цього елементу. Це єдиний елемент, у якого на зовнішньому електронному шарі кількість електронів дорівнює кількості орбіталей. Він може утворювати довгі і міцні карбонові ланцюги, утворювати подвійні і потрійні зв’язки як з другим атомом Карбону, так і з атомами інших елементів. Карбон утворює молекули різноманітної геометрії. В своїх сполуках Карбон знаходиться у збудженому стані:
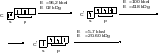
При утворенні хімічних зв’язків електрони мають невизначену орієнтацію своїх спінів. Переорієнтація спінів також потребує значної затрати енергії. Атом Карбону в сполуках може бути нейтральним, або мати заряд:
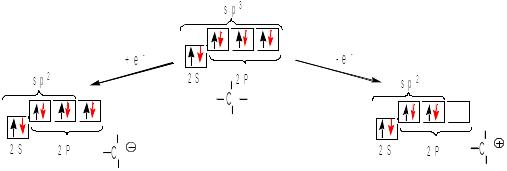
Електрони
атому С, що розміщені на зовнішньому
електронному рівні (валентні електрони),
знаходяться на різних орбіталях (S-
іP-).Орбіталь
– ділянка
простору, в якій на 95%
проявляються властивості даного
електрону.Л.Полінг
і Ж.Слейтер,
які увели в науку поняття «гібридизації»
валентних орбіталей. SP3-
гібридизація (І валентний стан карбону)
– тетраедрична;SP2-
гібридизація (ІІ валентний стан карбону)
– тригональна;SP
– гібридизація (ІІІ валентний стан
карбону) – діагональна
(лінійна).
Найбільш високий запас внутрішньої
енергії карбон має в стані SP3-гібридизації.
Вихідним моментом для визначення типу
гібридизації є просторова
будова молекули
(але не навпаки!) Ковалентні
зв’язки
утворюються внаслідок взаємодії
орбіталей двох атомів при виконанні
таких умов: на кожній із орбіталей
розташований один електрон, причому
спіни обох електронів протилежні
(звичайний механізм утворення зв’язку);
на одній орбіталі знаходиться пара
електронів, а друга орбіталь – вакантна
(донорно-акцепторний механізм утворення
зв’язку). При утворенні ковалентного
зв’язку виділяється певна кількість
енергії. В теорії МО-ЛКАО міцність
ковалентного зв’язку визначається
ступенем взаємного перекривання
орбіталей відповідних атомів. Чим більша
ділянка перекриття, тим більше енергії
виділяється і тим міцнішим буде зв’язок,
що утворюється. Розрізняють два
принципово відмінних один від одного
типи ковалентного зв’язку:
95%
проявляються властивості даного
електрону.Л.Полінг
і Ж.Слейтер,
які увели в науку поняття «гібридизації»
валентних орбіталей. SP3-
гібридизація (І валентний стан карбону)
– тетраедрична;SP2-
гібридизація (ІІ валентний стан карбону)
– тригональна;SP
– гібридизація (ІІІ валентний стан
карбону) – діагональна
(лінійна).
Найбільш високий запас внутрішньої
енергії карбон має в стані SP3-гібридизації.
Вихідним моментом для визначення типу
гібридизації є просторова
будова молекули
(але не навпаки!) Ковалентні
зв’язки
утворюються внаслідок взаємодії
орбіталей двох атомів при виконанні
таких умов: на кожній із орбіталей
розташований один електрон, причому
спіни обох електронів протилежні
(звичайний механізм утворення зв’язку);
на одній орбіталі знаходиться пара
електронів, а друга орбіталь – вакантна
(донорно-акцепторний механізм утворення
зв’язку). При утворенні ковалентного
зв’язку виділяється певна кількість
енергії. В теорії МО-ЛКАО міцність
ковалентного зв’язку визначається
ступенем взаємного перекривання
орбіталей відповідних атомів. Чим більша
ділянка перекриття, тим більше енергії
виділяється і тим міцнішим буде зв’язок,
що утворюється. Розрізняють два
принципово відмінних один від одного
типи ковалентного зв’язку:
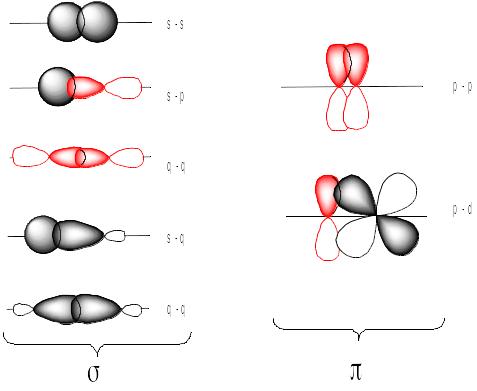
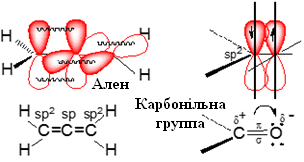
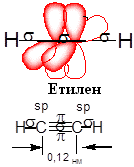 Квантово-механічне
пояснення природи кратних зв’язків
було дано в 1930 році Є.Хюккелем. Саме він
увів у науку поняття
Квантово-механічне
пояснення природи кратних зв’язків
було дано в 1930 році Є.Хюккелем. Саме він
увів у науку поняття
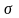 -
і
-
і
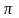 -
зв’язків. В залежності від валентного
стану атому карбону він утворює різні
за фізичними властивостями ковалентні
хімічні зв’язки.
-
зв’язків. В залежності від валентного
стану атому карбону він утворює різні
за фізичними властивостями ковалентні
хімічні зв’язки.
41. Природа хімічних зв'язків.
Рушійною силою утворення хімічного зв’язку є прагнення ізольованих атомів до виграшу в енергії, який досягається при їх об’єднанні в систему; стійкість системи забезпечується виникненням області підвищеної густини негативного електричного заряду в між’ядерному просторі, яка притягує до себе позитивно заряджені ядра атомів.
При утворенні хімічного зв’язку найважливішими є електрони зовнішнього шару, тобто валентні електрони, які утримуються ядром найменш міцно. Будова електронної конфігурації атомів є визначальним чинником при утворенні хімічного зв’язку.
Зв’язок атомів за допомогою спільних електронних пар називається ковалентний зв’язок. (Ковалентний неполярний – спільна електронна утворена між атомами з однаковою електронегативністю і не зміщується. Ковалентний полярний– спільна електронна пара зміщується в бік більш електронегативного атома).Зміна полярності зв’язку молекули внаслідок зміщення електронної густини під дією зовнішнього електричного поля іншої молекули називається поляризованість.
Спільна електронна пара, належить обом хімічно сполученим атомам, оскільки перебування двох електронів у полі дії двох ядер енергетично вигідніше, ніж знаходження кожного електрона у полі свого ядра. Однак виникнення спільної електронної пари зв’язку може проходити за різними механізмами: частіше – за обмінним, а інколи – за донорно-акцепторним.
Обмінний механізм утворення ковалентного зв’язку полягає в тому, що кожний із взаємодіючих атомів постачає на утворення спільних двохелектронних хмар однакову кількість електронів з антипаралельними спінами
![]()
Механізм утворення ковалентного зв’язку за рахунок двохелектронної хмари одного атома та вакантної орбіталі іншого називається донорно-акцепторним.
Частинка, яка надає для утворення зв’язку двохелектронну хмару (неподілену пару електронів), називається донор, а частинка з вільною орбіталлю, яка приймає цю електронну пару, – акцептор.
Сигма-зв’язок (σ-зв’язок) – це таке перекривання електронних орбіталей, при якому максимальна електронна густина концентрується у між’ядерному просторі вздовж вісі зв’язку. Ознакою сигма-зв’язку є наявність однієї області перекривання, зосередженої між ядрами хімічно сполучених атомів
Пі-зв’язок – це перекривання електронних орбіталей, при якому максимальна електронна густина концентрується з обох боків від умовної вісі, що з’єднує ядра атомів.π-зв’язок відрізняєється боковим перекриванням валентних орбіталей
σ-Зв’язок міцніший порівняно з π-зв’язком,
σ-Зв’язок сприяє можливості внутрішньо-молекулярного обертання атомів без розриву зв’язку, а π-зв’язок такого обертання не допускає (без розриву зв’язку);
Електрони при π-перекриванні, мають більшу рухливість, ніж σ-електрони, тому π-зв’язок здатний сильно деформуватися під впливом зовнішнього силового поля.
Дипольний момент утворюється за рахунок зміщення центрів позитивного і негативного зарядів на деяку величину l, звану довжиною диполя.
Не слід плутати дипольний момент зв'язку і дипольний момент молекули, так як в молекулі можуть існувати декілька зв'язків, дипольні моменти яких підсумовуються як вектори. На величину дипольного моменту молекули можуть впливати магнітні поля орбіталей, що містять електронну пару, - "неподілені" електрони . Великий вплив на полярність молекули надає її симетрія.
42. Сучасні уявлення про взаємний вплив атомів у молекулі. Індукційний ефект.
Взаємний вплив атомів в органічних молекулах визначається розподілом електронної густини в молекулі та поляризовністю ковалентних зв’язків. В молекулах органічних речовин під впливом наявних в них різних за своєю природою атомів або атомних груп відбувається перерозподіл електронної густини хімічних зв’язків двох ефектів: індукційнго (по s-зв’язку) та мезомерного (по p-зв’язку).
Індуктивний (індукційний)ефект
![]() Унаслідок
різної електронегативності елементів
зв'язок sp3-гібридизованого
атома Карбону з іншими атомами може
поляризуватися. Так, в алкілхлориді
електронна густина дещо вища біля атома
Хлору, ніж біля атома Карбону, оскільки
Хлор більш електронегативний:
Унаслідок
різної електронегативності елементів
зв'язок sp3-гібридизованого
атома Карбону з іншими атомами може
поляризуватися. Так, в алкілхлориді
електронна густина дещо вища біля атома
Хлору, ніж біля атома Карбону, оскільки
Хлор більш електронегативний:
![]() Якщо
атом Карбону, сполучений із Хлором,
сполучається ще й з іншими атомами
Карбону, то такий ефект може передаватися
по ланцюгу. Зміщення s-електронної
густини позначають стрілкою
Якщо
атом Карбону, сполучений із Хлором,
сполучається ще й з іншими атомами
Карбону, то такий ефект може передаватися
по ланцюгу. Зміщення s-електронної
густини позначають стрілкою
Більшість атомів і груп, сполучених з атомом Карбону, виявляють такий самий вплив і в тому самому напрямку, що й атом Хлору, тобто вони відтягують електрони від атома Карбону {акцептори електронів) внаслідок більшої, порівняно з ним, електронегативності.
![]() Однак
якщо біля одного з атомів Карбону зв'язку
С—С міститься атом із цілим або частковим
негативним зарядом {донори
електронів),
Однак
якщо біля одного з атомів Карбону зв'язку
С—С міститься атом із цілим або частковим
негативним зарядом {донори
електронів),
![]() то
електрони s-зв'язку С—С зміщуються в
протилежному напрямку:
то
електрони s-зв'язку С—С зміщуються в
протилежному напрямку:
Атоми металів, наприклад у реактивахГриньяра,також є донорами електронів, тобто атом Карбону стає негативно поляризованим
Такий вплив на розподіл електронів у s-зв'язках відомий як індукційний ефект, зумовлений здатністю атома або групи атомів зміщувати s-електрони.
Група атомів (замісник), які відтягують на себе електронну густину, мають негативний індукційний ефект -І-ефект (електроноакцепторний індукційний ефект).
Коли атом або групи атомів (замісник) відштовхує електронну густину від себе, йдеться про позитивний індукційний ефект +І-ефект (електронодонорний індукційний ефект).
Переважна більшість атомів і атомних груп проявляють негативний індуктивний ефект: F, Cl, Br, I, -NO2, -COH, -COOH, -OH, -NH2.
Існують певні правила для визначення знака і величини І-ефекту замісників.
-І-Ефект тим сильніший, чим більша електронегативність відповідногоатома.
Ненасичені замісники виявляють -І-ефект, який зростає зі збільшеннямступеня ненасиченості замісника.
+І-ефект алкільних груп збільшується зі зростанням розгалуженості ланцюга алкілу СН3< СН2СН3< СН(СН3)2< С(СН3)3.
При введенні в молекулу електронодонорних замісників понижується знижується кислотність, а основність посилюється. З електроноакцепторними замісниками навпаки
43. Мезомерний ефект.
Мезомерний ефект(ефект супряження, резонансний ефект) – це зміщення електронної густини по p-зв’язку в напрямку більш елекронегативного атома або групи атомів. Розрізняють позитивний (+М) і негативний (–М) мезомерні ефекти
В залежності від того, які електрони (електронні орбіталі) приймають участь в спряженні, розрізняють: π,π-Спряження відбувається, коли прості і кратні (подвійні чи потрійні) зв’язки розміщуються в молекулі почергово та в ароматичних сполуках – у молекулах бензені та його гомологів.; р,π-Спряження виникає в системі з таким чергуванням фрагментів: подвійний зв’язок – одинарний s-зв’язок – р-орбіталь. Причому, р-орбіталь може містити неподілену електронну пару, один неспарений електрон чи бути вакантною (у хлорвінілі). та s-p-супряження(перекривання s-орбіталі зв’язку С–Н і p-орбіталі).
44. Ізомерія органічних сполук.
Ізомерія – явище, при якому різні сполуки, що мають однаковий якісний і кількісний склад, відрізняються своїми властивостями. Ізомерія пояснюється різною будовою молекул таких сполук (ізомерів). Відомо два основні типи ізомерії: структурна і просторова (стереоізомерія).
Структурна ізомерія– це перебування органічних сполук, що мають однаковий якісний і кількісний склад, в різних молекулярних формах, які відрізняються між собою порядком сполучення атомів в молекулі і, як наслідок цього, різними фізичними та хімічними властивостями.
Такі сполуки називаються ізомерами, для яких існує два основних види ізомерії – структурна та просторова ізомерія.
Структурна ізомерія підрозділяється на:
- ізомерію карбоноаого скелету, положення функціональних груп;
- Просторова ізомерія поділяється на:конформаційну ізомерію;конфігураційну.
Конформаційна (поворотна) ізомерія обумовлена можливістю відносно вільного обертання атомів або груп атомів навколо простого - зв’язку – атоми С–С-зв’язку знаходяться в sp3-гібридному стані, що характерно, наприклад, для алканів
Конфігураційна ізомерія поділяється на:- геометричну ізомерію, - оптичну ізомерію.
Геометрична ізомерія пов’язана із неможливістю вільного обертання атомів або груп атомів навколо кратного зв’язку. Це обумовлено наявністю подвійного ( + -зв’язку) > C = C < для атомів Карбону в sp2-гібридному стані.(цис-ізомерія (однакові замісники), транс-ізомерія(різні замісники у сполуці))
Оптична ізомерія пов’язана із наявністю в молекулі атома Карбону (sp3-гібридний стан), що має чотири різних замісники. Такий атом називається хіральним або асиметричним.
енантіомери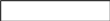
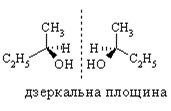
Таутомерія — особлива форма ізомерії, за якої два або більше ізомери легко переходять один в одного.

Етаналь–Етанол
45. Кислотно-основні властивості органічних сполук
Важливими аспектами реакційної здатності органічних сполук є їх кислотні та основні властивості. Для опису кислотних і основних властивостей хімічних сполук існує кілька теорій.
Сучасна теорія кислот-основ починається з 1887 р., з робіт Сванте Арреніуса, присвячених дисоціації сполук у водних розчинах. За Арреніусом сполука, що при дисоціації утворює йон H+, є кислотою, а йон OH– — основою. Звідси випливає поняття про реакцію нейтралізації як сполучення йонів H+ і OH– з утворенням води:
H+(aq) + OH–(aq) = H2O,
внаслідок якої також утворюється сіль. Пізніше цю теорію було узагальнено на неводні розчинники.
За теорією Бренстеда - Лоурі кислоти - це нейтральні молекули або іони, здатні віддавати протон (донори протона).
За теорією Льюїса кислоти - це нейтральні молекули або іони, здатні приєднувати електронну пару (акцептори електронної пари).