Материал: магістерський іспит з хімії 1
Кислоти Бренстеда. Сила кислот Бренстеда залежить від розчинника. Це пов'язано з тим, що молекули розчинника самі є кислотами або основами Бренстеда. Наприклад, при розчиненні кислоти Н-А у воді відбувається іонізація цих речовин: Н-А + Н2О А- + Н3О+
Залежно від природи елемента, з яким пов'язаний відщеплюється протон, бренстедовскі кислоти діляться на ОН-кислоти (карбонові кислоти, спирти, феноли), SH-кислоти, NH-кислоти (аміак, аміни, аміди), СН-кислоти ( вуглеводні та їх похідні).
За зростанням кислотності кислоти Бренстеда розташовуються в ряд: СН-кислоти <NH-кислоти <ОН-кислоти <SH-кислоти.
Основи Бренстеда. Основи для утворення зв'язку з протоном повинні містити або неподільну пару електронів, або електрони p-зв'язку. Відповідно до цього підстави Бренстеда діляться на дві групи: n-основи (містять вільну електронну пару) і p-основи. До p-основ відносять алкени, алкадієни, арени, тобто сполуки, що містять p-зв'язок. p-основи за рахунок електронної пари p-зв'язку можуть приєднувати протон (s-орбіталь протона перекривається з p-орбіталю). Ця нестійка частка носить назву p-комплексу. Протон при цьому не приєднується до жодного з атомів. Надалі p-комплекс перетворюється в s-комплекс.n-основи зв'язок з протоном утворюють за рахунок вільної електронної пари атома азоту (в амінах, гетероциклічних сполуках), атома кисню (в спиртах, простих ефірах, карбонових кислотах, альдегідах, кетонах), атом сірки (в тіоспирти, тіоефіри).
Сила n-основ зменшується в ряду: R-NH2> R-OH> R-SH.
На силу кислот і основ впливають будова речовини і природа розчинника. Кислотність органічних сполук залежить:
· від електронегативності атомів, відповідальних за прояв кислотних властивостей,
· від поляризуємих зв'язків в кислотному центрі;
· від чинників, які визначають високу стабільність утворюються при дисоціації.
Згідно з теорією Льюїса, кислотами є часточки (атоми, молекули, іони), що приєднують до себе електронну пару, а основами – часточки, що відають електронну пару, акцептору (кислоті). Кислоти Льюїса – це акцептори електронної пари, а основи Льюїса – донори електронів. За хімічною будовою: кислотами Льюїса є хімічні часточки, що мають вакантну електрону пару АО або МО. Вони виступають електрофільними реагентами (катіони металів, протони, галогеніди деяких металів – AlCl3, BF3, SnCl4, FeCl3); основами Льюїса є хімічні частинки, що містять на зовнішній орбіталі пару валентних електронів, які вони можуть передавати акцептору з утворенням ковалетного зв’язку, вони є нуклеофільними реагентами (сполуки в яких є гетероатоми N, O, S; з парою не подільних електронів – аміни, спирти, прості ефіри).
35. Окиснення і відновлення. Окисно-відновні потенціали.
Окисно-відновна реакція – хімічна реакція, яка відбувається зі зміною ступеня окиснення атомів, що входять до складу реагентів, і реалізується перерозподілом електронів між атомом-окисником та атомом-відновником. У процесі окисно-відновної реакції відновник віддає електрони, тобто окиснюється; окисник приєднує електрони, тобто відновлюється. Причому будь-яка окисно-відновна реакція являє собою єдність двох протилежних перетворень – окисненнята відновлення, що відбуваються одночасно та без відриву одне від одного. А=А++е- Окиснення: Речовина A як відновник віддає один електрон. В+е-=В- Відновлення: Речовина В як окисник приймає електрон. А+В=А++В-Окисно-відновна реакція: Речовина А віддає електрон речовині В.
Види окисно-відновних реакцій міжмолекулярні – реакції, в яких атоми, що відновлюються та окиснюються знаходяться в різних молекулах, наприклад: H2S+Cl2=S+2HCl внутрішньомолекулярні – реакції, в яких атоми, що відновлюються та окиснюються знаходяться в одній і тій ж самій молекулі, наприклад: 2H2O=2H2+O2репропорціонування (компропорціонування) NH4NO3=N2O+2H2O диспропорціонування (самоокиснення-самовідновлення) – реакції, в яких атоми одного елементу перетворюються на речовину (речовини) зі змінною ступенів окиснення, наприклад: Cl2+H2O=HClO+HCl. Окисно-відновна реакція між воднем та фтором H20+F20=2H+1F-1 Поділяється на дві напівреакції 1) Окиснення: H20-2e-=2H+2) Відновлення: F20+2e-=2F-Атоми та йони, які в даній реакції приєднують електрони є окисниками, а які віддають електрони – відновниками.
Гальванічний елемент – хімічне джерело живлення, в якому використовується різниця електродних потенціалів двох металів, занурених у електроліт. Такий елемент складається з двох різних металів, з'єднаних за допомогою сольового містка, а окремі половини комірки відокремлені пористою мембраною. Це може бути цинковий і мідний електроди, занурені в розчин сірчаної кислоти. Кожен із електродів зокрема разом із електролітом, в який він занурений, утворює напівелемент. Якщо з'єднати електроди провідником, то заряд стікатиме від електрода з більшим потенціалом, до електрода з меншим потенціалом, утворюючи електричний струм. Електродний потенціал – різниця електричних потенціалів між електродом та електролітом, в контакті з яким він знаходиться. Водневий електрод – відновлювально-окисний електрод, що береться за основу термодинамічної шкали відновлювально-окисних потенціліалів і = 0.
Рівняння
Нернста
– рівняння, що описує залежність
рівноважного потенціалу електрода від
термодинамічної активності (концентрації)
потенціал-визначальних компонентів
розчину електроліту. Е=Е0+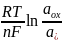 , де Е – електродний потенціал, Е0
–стандартний електродний потенціал,
R
– універсальна газова стала, T
– абсолютна температура, n
– кількість електронів, що беруть
участь, F
– число Фарадея 96485,33 Кл ٭моль,
а – активності відповідно ок.і від.
форм системи, якщо підставити числові
значення R, F, то при Т=298К отримаємо Е=Е0+
, де Е – електродний потенціал, Е0
–стандартний електродний потенціал,
R
– універсальна газова стала, T
– абсолютна температура, n
– кількість електронів, що беруть
участь, F
– число Фарадея 96485,33 Кл ٭моль,
а – активності відповідно ок.і від.
форм системи, якщо підставити числові
значення R, F, то при Т=298К отримаємо Е=Е0+
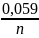 lg
lg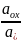
Електроліз – розклад речовин постійним електричним струмом, полягає в електрохімічних процесах окиснення та відновлення на електродах. При електролізі позитивно заряджені йони (катіони) рухаються до катода, на якому електрохімічно відновлюються. Негативно заряджені йони (аніони) рухаються до анода, де електрохімічно окиснюються. В результаті на електродах виділяються речовини в кількостях, пропорційних кількості пропущеного струму. Електроліз застосовується для одержання багатьох речовин (металів, водню, хлору), при гальваностегії (нанесенні металічних покриттів).
36. Стереоізомерія.
Стереоізомери – молекулярні структури з однаковими атомами й характером зв'язків, які відрізняються розміщенням у просторі. До них відносяться енантіомери, діастереомери й геометричні ізомери.
Оптична активність – здатність речовини повертати площину поляризації світла.
Речовини, які можуть повертати площину поляризації світла, називаються оптично активними. Такі речовини не повинні мати симетрії інверсії. Оптична активність може бути природною і наведеною зовнішніми полями. Явище оптичної активності поширене серед органічних речовин, особливо природних (гідрокси- й амінокислот, білків, вуглеводів, алкалоїдів). Однією з причин виникнення оптичної активності органічних молекул є наявність у структурі sp3-гібридизованого атома карбону, зв’язаного з чотирма різними замісниками. Такий атом карбону називається хіральним або асиметричним (хіральний центр). У структурних формулах асиметричний атом вуглецю позначають зірочкою – С*.
А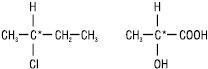 симетричними
можуть бути й інші атоми, нітрогену,
сульфуру, фосфору. Оптичну активність
виявляють також сполуки, які не містять
асиметричного атома – це похідні алену,
адамантану, фероцену, ізомерія яких
викликана відсутністю обертання навколо
простого зв’язку, так звана атропізомерія.
Оптична активність характерна також
для спіральних конформацій білків,
нуклеїнових кислот, гексагеліценів.
Сполуки, які містять один асиметричний
атом карбону, існують у вигляді двох
ізомерів, котрі співвідносяться як
предмет до свого дзеркального відображення.
Такі ізомери називають енантіомерами.
симетричними
можуть бути й інші атоми, нітрогену,
сульфуру, фосфору. Оптичну активність
виявляють також сполуки, які не містять
асиметричного атома – це похідні алену,
адамантану, фероцену, ізомерія яких
викликана відсутністю обертання навколо
простого зв’язку, так звана атропізомерія.
Оптична активність характерна також
для спіральних конформацій білків,
нуклеїнових кислот, гексагеліценів.
Сполуки, які містять один асиметричний
атом карбону, існують у вигляді двох
ізомерів, котрі співвідносяться як
предмет до свого дзеркального відображення.
Такі ізомери називають енантіомерами.
Для відображення просторової будови оптичних ізомерів на площині можуть бути використані стереохімічні формули – енантіомери бутанолу-2:
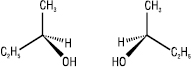

Частіше оптичні ізомери зображують на площині за допомогою проекційних формул Фішера. Енантіомери схожі між собою, але не тотожні, вони мають однаковий склад і послідовність зв’язування атомів у молекулі, але відрізняються один від одного відносним розташуванням атомів у просторі, тобто конфігурацією. Енантіомери мають однакові фізичні і хімічні властивості, обертають площину поляризації поляризованого променя на один і той же за величиною, але протилежний за напрямком кут; вони з різною швидкістю реагують з іншими хіральними сполуками і відрізняються за фізіологічною дією.
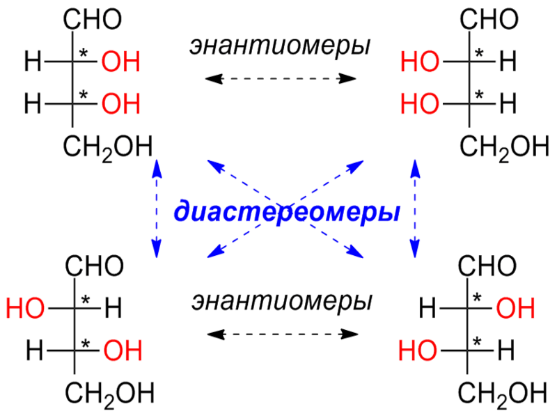 До
діастереоізомерів
належать усі стереоізомери, які не є
енантіомерами, тобто дзеркальними
відображеннями один одного. Діастереомери
молекули виникають при наявності у ній
декількох стереоцентрів. До діастереомерів
належать також стереоізомери, які
відрізняються конфігурацією подвійного
зв'язку (π-діастереомери, або геометричні
ізомери). Діастереомери відрізняються
за фізичними властивостями, зокрема за
оптичною активністю.
До
діастереоізомерів
належать усі стереоізомери, які не є
енантіомерами, тобто дзеркальними
відображеннями один одного. Діастереомери
молекули виникають при наявності у ній
декількох стереоцентрів. До діастереомерів
належать також стереоізомери, які
відрізняються конфігурацією подвійного
зв'язку (π-діастереомери, або геометричні
ізомери). Діастереомери відрізняються
за фізичними властивостями, зокрема за
оптичною активністю.
37. Енергетика хімічних реакцій.
Об'єктом вивчення в термодинаміці є термодинамічна система, під якою розуміють умовно виділену з простору сукупність тіл. Системи, які можуть обмінюватися з навколишнім середовищем і енергією і речовиною називаються відкритими. Системи, які обмінюються тільки енергією, називаються закритими. Якщо між середовищем та системою відсутній і тепло- і масообмін – це ізольована система. Розрізняють також гомогенні системи, що складаються з однієї фази та гетерогенні, що складаються з декількох фаз. Реакції, які протікають на межі розділу фаз – гетерогенні. Параметри діляться на інтенсивні та екстенсивні. Інтенсивні не залежать від розміру системи, а залежать від температури і тиску, екстенсивні залежать від маси та об'єму. Зміна одного з параметрів призводить до зміни стану в цілому. Стан системи називається рівноважним, якщо параметри системи в часі мимоволі не змінюються. Нерівноважна система –параметри в часі змінюються. Функції стану – внутрішня енергія, ентропія, ізобарний, ізотермічний потенціал.Перехід системи з 1-го стану під другим називається процесом.
40. Будова атома Карбону.
Положення Карбону у Періодичній системі елементів Д.І.Менделєєва обумовлює унікальні властивості цього елементу. Це єдиний елемент, у якого на зовнішньому електронному шарі кількість електронів дорівнює кількості орбіталей. Він може утворювати довгі і міцні карбонові ланцюги, утворювати подвійні і потрійні зв’язки як з другим атомом Карбону, так і з атомами інших елементів. Карбон утворює молекули різноманітної геометрії. В своїх сполуках Карбон знаходиться у збудженому стані:
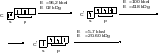
При утворенні хімічних зв’язків електрони мають невизначену орієнтацію своїх спінів. Переорієнтація спінів також потребує значної затрати енергії. Атом Карбону в сполуках може бути нейтральним, або мати заряд:
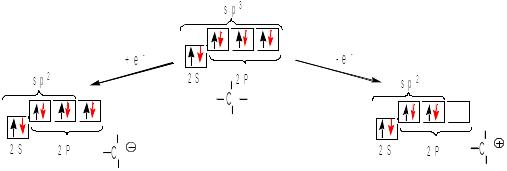
Електрони
атому С, що розміщені на зовнішньому
електронному рівні (валентні електрони),
знаходяться на різних орбіталях (S-
іP-).Орбіталь
– ділянка
простору, в якій на 95%
проявляються властивості даного
електрону.Л.Полінг
і Ж.Слейтер,
які увели в науку поняття «гібридизації»
валентних орбіталей. SP3-
гібридизація (І валентний стан карбону)
– тетраедрична;SP2-
гібридизація (ІІ валентний стан карбону)
– тригональна;SP
– гібридизація (ІІІ валентний стан
карбону) – діагональна
(лінійна).
Найбільш високий запас внутрішньої
енергії карбон має в стані SP3-гібридизації.
Вихідним моментом для визначення типу
гібридизації є просторова
будова молекули
(але не навпаки!) Ковалентні
зв’язки
утворюються внаслідок взаємодії
орбіталей двох атомів при виконанні
таких умов: на кожній із орбіталей
розташований один електрон, причому
спіни обох електронів протилежні
(звичайний механізм утворення зв’язку);
на одній орбіталі знаходиться пара
електронів, а друга орбіталь – вакантна
(донорно-акцепторний механізм утворення
зв’язку). При утворенні ковалентного
зв’язку виділяється певна кількість
енергії. В теорії МО-ЛКАО міцність
ковалентного зв’язку визначається
ступенем взаємного перекривання
орбіталей відповідних атомів. Чим більша
ділянка перекриття, тим більше енергії
виділяється і тим міцнішим буде зв’язок,
що утворюється. Розрізняють два
принципово відмінних один від одного
типи ковалентного зв’язку:
95%
проявляються властивості даного
електрону.Л.Полінг
і Ж.Слейтер,
які увели в науку поняття «гібридизації»
валентних орбіталей. SP3-
гібридизація (І валентний стан карбону)
– тетраедрична;SP2-
гібридизація (ІІ валентний стан карбону)
– тригональна;SP
– гібридизація (ІІІ валентний стан
карбону) – діагональна
(лінійна).
Найбільш високий запас внутрішньої
енергії карбон має в стані SP3-гібридизації.
Вихідним моментом для визначення типу
гібридизації є просторова
будова молекули
(але не навпаки!) Ковалентні
зв’язки
утворюються внаслідок взаємодії
орбіталей двох атомів при виконанні
таких умов: на кожній із орбіталей
розташований один електрон, причому
спіни обох електронів протилежні
(звичайний механізм утворення зв’язку);
на одній орбіталі знаходиться пара
електронів, а друга орбіталь – вакантна
(донорно-акцепторний механізм утворення
зв’язку). При утворенні ковалентного
зв’язку виділяється певна кількість
енергії. В теорії МО-ЛКАО міцність
ковалентного зв’язку визначається
ступенем взаємного перекривання
орбіталей відповідних атомів. Чим більша
ділянка перекриття, тим більше енергії
виділяється і тим міцнішим буде зв’язок,
що утворюється. Розрізняють два
принципово відмінних один від одного
типи ковалентного зв’язку:
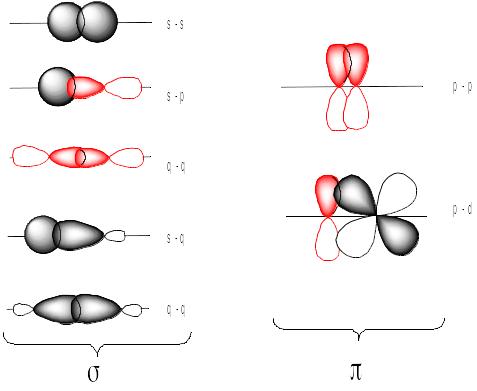
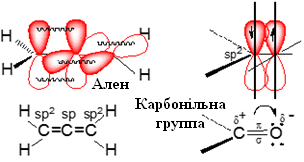
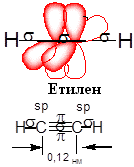 Квантово-механічне
пояснення природи кратних зв’язків
було дано в 1930 році Є.Хюккелем. Саме він
увів у науку поняття
Квантово-механічне
пояснення природи кратних зв’язків
було дано в 1930 році Є.Хюккелем. Саме він
увів у науку поняття
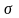 -
і
-
і
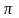 -
зв’язків. В залежності від валентного
стану атому карбону він утворює різні
за фізичними властивостями ковалентні
хімічні зв’язки.
-
зв’язків. В залежності від валентного
стану атому карбону він утворює різні
за фізичними властивостями ковалентні
хімічні зв’язки.
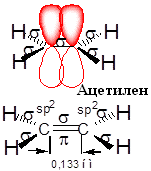
39. Фізико-хімічні методи дослідження речовин.
Усі фізичні і фізико-хімічні методи: Електрохімічні методи. Електроваговий аналіз ґрунтується на виділенні з розчинів електролітів речовин, що осаджуються на електродах при проходженні через розчин постійного електричного струму. Кондуктометрія ґрунтується на вимірюванні електропровідності розчинів, яка змінюється у результаті хімічної реакції і яка залежить від природи електроліту, його температури та концентрації розчину. Потенціометрія ґрунтується на вимірюванні потенціалу електроду, який змінюється внаслідок хімічної реакції і який занурений у розчин, що аналізується.
Спектральні (оптичні) методи. Емісійний спектральний аналіз ґрунтується на вивченні емісійних спектрів елементів речовини, яка аналізується (спектри випромінювання). Абсорбційна спектроскопія ґрунтується на вивченні спектрів поглинання речовини, яка аналізується, і являються її індивідуальною характеристикою.Інфрачервона спектроскопія – молекулярна оптична спектроскопія, яка вивчає спектри поглинання та відбиття електромагнітних хвиль в ІЧ-області. Фотоколориметрія ґрунтується на визначенні спектра поглинання або вимірюванні світлопоглинання у видимій ділянці спектра і на порівнянні інтенсивності забарвлення досліджуваного забарвленого розчину. Люмінесцентний або флуоресцентний метод ґрунтується на опромінених ультрафіолетовим світлом і вимірюванні інтенсивності випромінюваного ними видимого світла.
Хроматографічні методи ґрунтуються на вибірковому поглинанні (адсорбції) окремих компонентів суміші, яка аналізується, різними адсорбентами. При фронтальному аналізі досліджуваний розчин суміші речовин безперервно подають у верхню частину колонки і збирають окремі фракції фільтрату. Газовою хроматографією є процес, де рухомою фазою є газ (чи пар). Рідинною хроматографією є процес, де рухомою фазою є рідина. Тонкошарову хроматографію, що являє собою різновидність розподільної хроматографії, яка здійснюється на пластинках вкритих тонким шаром носія (алюміній оксид). Паперова хроматографія – різновид розподільної хроматографії, в якій носієм для нерухомого розчинника є смужки чи аркуші фільтрувального паперу, що не містить мінеральних домішок.
Радіометричні методи ґрунтуються на вимірюванні випромінювання атомами радіоактивних елементамів. Метод ізотопного розведення ґрунтується на розведенні сполуки, яка мічена радіоактивним ізотопом, неактивним компонентом суміші.Принцип методу радіоактиваційного аналізу, полягає в переводі стабільних ізотопів елемента у радіоактивні.
Мас-спектрометричні методи аналізу ґрунтуються на визначенні окремих йонізованих атомів, молекул та радикалів за допомогою розділення потоку йонів, що містять частинки з різним відношенням маси до заряду, в результаті комбінованої дії електричного та магнітного полів. Застосовують для визначення ізотопного складу елементів, вмісту різних радикалів, окремих компонентів в складних сумішах або домішок.
Ядерно-фізичні методи. Метод ядерного магнітного резонансу (ЯМР) ґрунтується на використанні резонансного поглинання електромагнітних хвиль досліджуваною речовиною у постійному магнітному полі, яке обумовлено ядерним магнетизмом. Метод ядерної гама-резонансної (ЯГР) спектроскопії ґрунтується на спостереженні мессбауровського ефекту. Метод ЯГР-спектроскопії використовується для встановлення характера хімічних зв’язків в речовинах, а також для дослідження комплексних та елементорганічних сполук.