Материал: магістерський іспит з хімії 1
29. Інноваційні технології навчання хімії.
Серед інноваційних технологій, виокремлюють технологію групової навчальної діяльності школярів. “Групова навчальна діяльність – це форма організації навчання в малих групах учнів, об’єднаних загальною навчальною метою при опосередкованому керівництві вчителем і в співпраці з учнями”. Учитель у груповій навчальній діяльності керує роботою кожного учня опосередковано, через завдання, які він пропонує групі та які регулюють діяльність учнів. Групова навчальна діяльність сприяє активізації й результативності навчання школярів, вихованню гуманних стосунків між ними, самостійності, уміння доводити і відстоювати свою точку зору, а також прислуховуватися до думки товаришів, культури ведення діалогу, відповідальності за результати своєї праці.
Проектна технологія навчання. Застосування проектної технології у навчально-виховному процесі здійснюється відповідно до загальнодидактичних принципів: науковості, наочності, природовідповідності, системності, зв’язку навчання з життям та принципів навчального проекту, дотримання яких забезпечує найбільшу ефективність проектної діяльності учнів.Основні підходи до її впровадження
1) виконання проекту на уроці (чи декількох уроках, або тижні проектів);
2) робота над проектом об’єднує урок та позаурочну діяльність учнів;
3) проектна діяльність школярів організується у позаурочний час, уключається у роботу позашкільних закладів освіти.
Технологія портфоліо – спосіб фіксування, накопичення й оцінювання (та самооцінювання) індивідуальних досягнень учня в певний період навчання; персональнаколекція робіт учня, що всебічно демонструє не тільки його навчальні і творчі результати, але й зусилля, докладені для їх досягнення.
Відповідно до поставленої мети розрізняють наступні види портфоліо:
1. Папка досягнень (представлення власних здобутків)
2. Рефлексивне П. (аналіз того, що вдалося та не вдалося)
3. Проблемно-тематичне П. (інформація та творчі роботи)
4. Презентаційне П. (представлення себе)
5. Комплексне П. (поєднання всіх видів портфоліо)
Портфоліо є інструментом моніторингу, оскільки дозволяє вчителю відстежувати і коригувати індивідуальний прогрес учня упродовж тривалого часу навчання;
Технологія формування критичного мислення, яка передбачає:
• акцент на пошук і самостійне отримання знань;
• активне використання попереднього досвіду і знань учнів;
• заохочення висловлювань власної точки зору, власної позиції, обмін думками на всіх рівнях взаємодії;
• створення умов для аргументації зроблених висновків, суджень, позицій;
• стимулювання спроб перевірки і застосування нових знань і досвіду.
Три стадії технології формування критичного мислення:
Стадія виклику. Актуалізація наявних в учнів знань і уявлень; пробудження інтересу до досліджуваної теми; активізація інтелектуальної діяльності; постановка учнем власних напрямків у вивченні проблеми.
Стадія осмислення. Отримання нової інформації по темі; класифікація отриманої інформації; коректування учнем напрямків вирішення проблеми.
Стадія рефлексії. Придбання нового знання; спонукання до подальшого розширення інформаційного поля; співвіднесення нової інформації і наявних знань; вироблення власної позиції, оцінка процесу.
30. Сучасні форми і методи оцінювання у старшій і вищій школі.
Оцінювання навчальних досягнень у старшій і вищій школі – це цілеспрямована керована діяльність учителя(викладача) хімії зі збирання інформації про процес і результат навчання як рух учня від свого попереднього рівня до нового через порівняння засвоєння ним змісту навчальної програми з хімії через організацію оцінювальних заходів (вибір форм, методів, засобів, критеріїв оцінювання, форм вираження результатів навчально-пізнавальної діяльності учнів); через організацію рефлексії навчальної діяльності, самоконтролю та самооцінювання навчальних результатів для їх якісного аналізу
Тестова система оцінювання навчальних досягнень студентів з хімії. Як показує практика, якісні тести стали важливим інструментом оцінювання якості знань, підвищення рівня підготовки фахівців.
Як метод контролю тести виконують функції:
- діагностичну - виявляють рівень знань;
- навчальну - стимулюють пізнавальну активність студентів;
- виховну - дисциплінують студентів, допомагають виявити і подолати прогалини в навчанні
Портфоліо як метод оцінювання навчальних досягнень студентів з хімії. З метою оцінювання індивідуальних досягнень учнів у допрофільній і профільній школі може бути використаний метод оцінювання портфоліо. Основна суть технології портфоліо – «показати все, на що ти здібний». Педагогічна ідея портфоліо передбачає зміщення акценту з незнання учнів на індивідуальні досягнення, їх активну участь у накопиченні різних видів робіт, що засвідчують рух в індивідуальному розвитку; інтеграцію кількісних і якісних оцінок; підвищення ролі самооцінки. Таке оцінювання передбачає певну підготовку: визначення критеріїв для включення учнівських напрацювань до портфоліо; форми подання матеріалу; спланованість оцінного процесу; елементи самооцінки з боку учня тощо.
кейс метод оцінювання – це спеціально підготовлений навчальний матеріал, що містить структурований опис ситуацій, запозичених з реальної практики. Кейс повинен відображати реальну життєву ситуацію, містити проблему або ряд прямих або непрямих труднощів, протиріч, прихованих завдань. Даючи студентам завдання у формі кейсів, ми відкриваємо їм значно більшу можливість поділитися своїми знаннями, досвідом і уявленнями, тобто навчитися не тільки у викладача, а й один у одного. Такий метод піднімає впевненість студентів у собі, у своїх здібностях. Вони активно вчаться слухати один одного і точніше висловлювати свої думки.
Поряд з іншими формами оцінювання ефективною у старшій школі є рейтингова система,яка сприяє формуванню ключових компетентностей і створює можливості для:
підвищення мотивації учнів до само навчання та само оцінювання;
розширення можливості в індивідуальній підготовленості учнів на кожному етапі навчального процесу;
підвищення об'єктивності оцінювання не лише протягом навчального року, а й за весь період навчання у старшій школі;
градації значущості балів, які отримують учні за виконання різних видів робіт (самостійна робота, підсумкова робота, творча робота, олімпіади, виставки, конкурси творчих робіт
Упровадження рейтингу навчальних досягнень передбачає побудову учнем (студентом) індивідуальної освітньої програми, яка дозволить учителям і батькам учнів аналізувати їхній освітній поступ та його (її) досягнення, виявляти помилки, а також регулювати форми й види освітньої діяльності.
32. Будова молекул і хімічний зв’язок.
Структури Льюїса – графічне зображення зв'язків між атомами, молекулами або йонами, яка базується на правилі октету. Побудувати формулу Льюїса можна за схемою: порахувати всі валентні електрони кожного елемента молекули, і сумується їхня кількість; отримана сума ділиться на 2, і отримується кількість електронних пар, які будуть в структурі; будується «скелет» формули, записуючи хімічні елементи і розподіляючи електронні пари між ними; потім переміщаючи електронні пари, утворюємо схему, яка задовольняє правило октету (кожен елемент мав 8 електронів, або 4 електронні пари.
Хімічний зв'язок – енергія взаємодії між атомами, яка утримує їх у молекулі чи твердому тілі. Хімічні зв'язки є результатом складної взаємодії електронів та ядер атомів і описуються квантовою механікою. Серед типів хімічного зв'язку розрізняють: Ковалентний зв'язок здійснюється у результаті узагальнення валентних електронів з утворенням спільної електронної пари. Електрони, які беруть участь в утворенні хімічного зв'язку, називають валентними електронами. Ковалентний неполярнийзв'язок в : H2, F2, Cl2, O2, N2.Ковалентний полярний (спільна електронна пара хім. зв'язку)
Водневий зв'язок – різновид хімічного зв'язку, що реалізується за донорно-акцепторним механізмом між двома ковалентно зв'язаними атомами з великим значенням електронегативності (О, N, F), що виступають в ролі донора за посередництвом атома Гідрогену Н (акцептор).
Йонний хімічний зв'язок– це тип зв'язку, при якому електрони переходять із одного атома до іншого, й основний вклад в притягання вноситься електростатичною взаємодією. Утворюється між атомами або групами атомів зі значною різницею в електронегативностях. Характерний для сполук металів з найтиповішими неметалами. Металічний зв'язок – тип хімічного зв'язку, при якому валентніелектрониатомів делокалізуються і починають взаємодіяти з атомними основами усього тіла.
Властивості зв’язків: Довжина зв’язку – рівноважна відстань між ядрами атомів, які з’єднані хімічним зв’язком. Енергія хімічного зв’язку визначає її міцність. Енергія яка, необхідна, для того, щоб розірвати хімічний зв’язок і роз’єднати атоми.Полярність хімічного зв’язку показує, наскільки електронна щільність зміщена до одного з атомів. Здатність атомів зміщувати до себе електронну щільність називають електронегативністю.Порядок хімічного зв’язку (кратність хімічного зв’язку) – це число електронних пар, що вступають в хімічний зв’язок.
Метод валентних зв'язків (ВЗ) – електрони, які не беруть участі в утворенні зв'язків, розміщені на тих самих орбіталях, що й в ізольованих атомах. Ковалентний зв'язок утворюється двома електронами з протилежно напрямленими спінами.
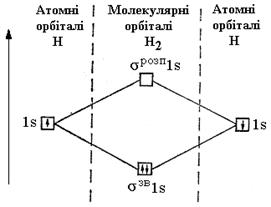 Метод
МО ЛКАО –
квантово хімічний метод, який пояснюється
хімічним зв'язком і який розглядає
молекулу як багатоядерну, в яку електрони
заселяються.
Метод
МО ЛКАО –
квантово хімічний метод, який пояснюється
хімічним зв'язком і який розглядає
молекулу як багатоядерну, в яку електрони
заселяються.
Основні положення: 1. Кожен електрон в молекулі характеризується повною хвильовою функцією – МО. 2. МО – дво- або багатоцентрова електронна хмара одночасно належить кільком атомним ядрам. 3. Форма хвильової функції та енергія відповідного рівня визначається чотирма молекулярними квантовими числами (n,l,λ,ms). 4. Електрони заповнюють МО згідно з принципом Паулі і правилом Гунда, в міру підвищення їх енергетичного рівня.Тверді тіла поділяють на кристалічні й аморфні. У кристалахсередні положення атомів чи молекул строго впорядковані. В аморфних тілах порядок не зберігається.
33. Симетрія молекул.
Розгляд просторової будови молекул засноване на стереохімічних уявленнях про молекулу як геометричному тілі в тривимірному просторі. Це вимагає залучення в стереохімію деяких геометричних понять, зокрема, елементів і операцій симетрії. Елементи симетрії є геометричні місця, щодо яких здійснюються операції симетрії. При цьому розрізняють: елементи симетрії 1 роду – осі симетрії (осі обертання); елементи симетрії 2 роду – площині симетрії (дзеркальні площини), центри симетрії (центри інверсії) і осі дзеркального відображення.
Операції симетрії – геометричні операції, здійснювані на елементах симетрії і переводять об'єкт (молекулу), еквівалентну або ідентичну орієнтацію.
Розрізняють чотири основних операції симетрії: обертання на кут 2π/n = 360° /n навколо осі обертання; відображення в площині симетрії;інверсія (відображення в точці) в центрі симетрії;обертання з відображенням навколо осі дзеркального відображення (обертання на кут 2π/n і відображення в площині, перпендикулярній до осі обертання).
Найбільш важливими елементами симетрії є вісь і площину симетрії. З операцій симетрії частіше використовуються дві: обертання навколо осі симетрії і відображення в дзеркальній площині.
Вісь симетрії. Якщо обертання молекули навколо будь-якої проходить через неї осі на кут 2π /n = 360 °/n призводить до структури, яка не вирізняється від вихідної, то таку вісь називають віссю симетрії n-го порядку З n. Якщо в молекулі є кілька осей симетрії різного порядку, то в якості головної осі (осі порівняння) вибирається вісь симетрії найвищого порядку. У молекулі бензолу, це вісь шостого порядку З 6, а в разі ацетилену –вісь З ∞.
Площина симетрії (дзеркальна площина) являє собою уявну площину, яка проходить через молекулу і ділить її на дві дзеркально-рівні частини.
Молекули несумісні зі своїм дзеркальним зображенням, ця властивість називається хіральністю, а самі молекули – хіральними. Термін "хіральність" означає, що два предмета ставляться один до одного як ліва і права руки і являють собою дзеркальні зображення, що не збігаються при спробі поєднати їх в просторі.
Таким чином, бромфторхлорметан може існувати у вигляді двох просторово несумісних (хіральних) молекул. Будь-яка молекула Хіральна, якщо вона не схожа на своє дзеркальне відображення. Молекули, не схожі зі своїм дзеркальним відображенням, є ахіральнимі.
За наявністю або відсутністю хіральності стереоізомери підрозділяються на енантіомери і діастереомери.
Енaнтіомeри – це стереоізомери, хіральні молекули яких відносяться між собою як предмет і несумісне з ним дзеркальне зображення. Вони являють собою два оптичних антипода і тому називаються також оптичними ізомерами.
Стереоізомери, які не є енантіомерами, називаються діастереоізомери або, коротше, діастереомер. Молекули діастереомерів можуть бути хіральними і ахіральнимі. Наприклад, діастереомери винної кислоти.
34. Кислоти і основи.
Кислотність і основність – поняття, що визначають багато фізико-хімічні властивості і реакційну здатність органічних сполук. Для оцінки кислотності і основності органічних сполук найбільше значення мають дві теорії – теорія Бренстеда і теорія Льюїса.
За теорією Бренстеда кислотність і основність сполук зв'язується з переносом протона Н +. Кислоти – речовини, здатні віддавати протон (донори протонів). Основи –речовини, здатні приєднувати протон (акцептори протона).
Кислота і основа утворюють сполучену кислотно-основну пару. Кислотні властивості проявляються в присутності основи, основні – в присутності кислоти. Між кислотою і основою існує взаємозв'язок: чим сильніше кислота, тим слабкіше основа, і навпаки. Наприклад, оцтова кислота слабкіше, ніж соляна, і, відповідно, ацетат-аніон – більш сильний ніж, аніон хлору.
Для позначення електронної конфігурації хімічного елементу використовують назви орбіталей: s, p, d, f, g. Перед назвою орбіталі стоїть основне квантове число, а верхній індекс після позначення орбіталі вказує на те, скільки електронів є на орбіталях. Наприклад, для неону електронна конфігурація записується 1s22s22p6. Запис означає, що неон має 2 електрони на внутрішній s-орбіталі, 2 електрони на зовнішній s-орбіталі й 6 електронів на зовнішній p-орбіталі.