Материал: магістерський іспит з хімії 1
Мезомерний ефект називають негативним (–М-ефект), якщо атоми або групи атомів приймають електронну густину від p-зв’язку (являються акцепторами електронів).
Позитивний мезомерний ефект властивий електродонорним групам, здатним до часткової або повної передачі пари електронів у загальну спряжену систему. Наприклад, при наявності в бензеновому ядрі замісників першого роду (–ОН, –NH2, –R тощо) внаслідок їх електронодонорного характеру електронна густина підвищується у самому ядрі, що призводить до полегшення перебігу реакцій заміщення. При наявності в бензеновому ядрі замісників другого роду (-NO2, -COOH, -SO3H) внаслідок їх електроноакцепторному характеру електронна густина в ядрі зменшується, що утруднює перебіг реакцій заміщення.
Існують правила, що визначають знак і відносну величину М-ефекту:
![]() 1. -М-Ефекттимсильніший,чимбільшаелектронегативністьгетероелементав
заміснику:
1. -М-Ефекттимсильніший,чимбільшаелектронегативністьгетероелементав
заміснику:
2![]() .
+М-Ефект замісника тим сильніший, чим
менша електронегативність
відповідногогетероелемента:
.
+М-Ефект замісника тим сильніший, чим
менша електронегативність
відповідногогетероелемента:
![]() Винятком
є галогени:
Винятком
є галогени:
Мезомерний ефект, як і індукційний, зумовлює поляризацію молекул і тому впливає на фізичні властивостісполук.
Теорія резонансу( мезомерії)— спосіб опису електронної будови часток (молекул, радикалів, іонів), яким притаманна суттєва делокалізація електронів. Електронна будова таких часток погано описується структурною формулою із певним розподілом ковалентних зв'язків і неподілених електронних пар. Теорія резонансу спирається на метод валентних зв'язків і фактично є способом візуалізації результатів його застосування. Разом із тим, вона дозволяє наближено передбачити або пояснити хімічні властивості, ґрунтуючись лише на поняттях валентності та електронегативності.
Індуктивний та мезомерний ефекти відрізняються тим, що індуктивний ефект може діяти як у насичених, так і в ненасичених системах, тоді як мезомерний ефект спостерігається тільки в ненасичених і особливо в кон'югованих системах. Індуктивний ефект пов'язаний з електронами s-зв'язків, а мезомерний — з p-електронами і неподіленими електронними парами. Індуктивний ефект передається тільки на відносно короткі відстані в насиченому ланцюгу, тоді як мезомерний — на значно більші відстані за наявності кон'югації.
Кореляційнийаналіз дає більш широке уявлення про ступінь зв'язку між атомами.
З цього випливає, що теоретично будь-яке з'єднання, до складу якого входить атом водню може його віддавати у вигляді протона і, проявляти властивості кислоти. Здатність віддавати протон можуть проявляти не тільки нейтральні молекули (HCl, ROH), але і заряджені частинки - катіони (NH4+) І аніони кислот (HSO4- та ін.).
Кислоти і основи проявляють свої властивості тільки в присутність один одного. Жодна речовина не віддаватиме протон, якщо в системі немає акцептора протона - сполуки, і навпаки. Таким чином, вони утворюють пов'язану кислотно - основну пару.
Речовина, що виступає у ролі кислоти, віддаючи протон перетворюється у сполучену основу. При цьому основа не обов'язково повинна містити гідроксильну групу, а представниками кислот й основ можуть бути не тільки нейтральні молекули, але й іони.Основа, приєднавши протон, перетворюється у сполучену кислоту
Чим більша електронегативність тим легше здійснюється гетеролітичний розрив в молекулі. У періодах зліва направо з ростом заряду ядра зростає електронегативність– здатність елементів утримувати негативний заряд. В результаті переміщення електронної густини – зв'язок між атомами поляризується. Чим більше електронів і чим більше радіус атома, тим далі електрони зовнішнього енергетичного рівня розташовані від ядра, тим вище здатність до поляризації і вище кислотність.
Органічні сполуки, до складу молекули яких входять атоми азоту, кисню, сірки, можуть виступати в ролі основаній, приєднуючи протон водню за рахунок неподіленої пари електронів на зовнішньому енергетичному рівні. Гетероатомом в молекулі органічної речовини, що приєднує протон, називається центром основності.
Сила основвизначається стабільністю утворюється катіона (сполученої кислоти). Чим стабільніший катіон, тим сильніша основа.
Для кількісної характеристики основності зазвичай використовують величину pK BH+ - Показник константи основності сполученої кислоти. Чим більше pK BH+, Тим сильніше основа.
Для слабких електролітів сила кислот і основ визначається величинами констант кислотності рКай основності рКb. Якщо ці константи характеризують протолітичну взаємодію води з кислотою або основою, то добуток цих констант для сполученої кислотно – основної пари завжди дорівнює іонному добутку води рКw.
Амбідентний аніон – аніон, що здатний реагувати двома різними центрами. Напр., NO2− (з AgNO2) при реакції з RX може давати нітрити RONO або нітроалкани RNO2.
46. Ароматичність
Всі ароматичні сполуки: Ненасичені; Мають плоску будову; Мають циклічну будову; Мають делокалізовану -електронну систему.
Існує 3 критерії ароматичності: Структурний; Енергетичний (мають аномально низький запас внутрішньої енергії); Магнітний.
Не всі циклічні ненасичені системи можуть мати делокалізовану -електронну систему. У 1931 році Е.Хюккель (Вища техн.школа у Штутгарді) довів, що «ароматичними слід вважати всі циклічні системи, які мають плоску будову і містять у замкнутій системі спряження 4n + 2 електрона». Це правило відомо в органічній хімії як правило Хюккеля, або як правило«4n + 2». (Де n – будь-яке ціле число і 0). Строго кажучи правило Хюккеля відноситься лише для моноциклічних карбоциклів, але його іноді застосовують і для поліциклічних сполук і для гетероциклічних сполук.
Ароматичні системи з 2 -електронами ( n = 0 )
Єдиною карбоциклічною ароматичною системою цього ряду повинен бути гіпотетичний циклопропенілій-катіон:
![]()
Ароматичні системи з 6 -електронами ( n = 1 )
Циклопентадієніл аніон. В продуктах піролізу нафтових фракцій і в бензольній фракції кам’яновугільної смоли міститься типова ненасичена речовина – циклопентадієн. При дії на нього металевого натрію відбувається реакція:
![]()
У аніона, що утворився, всі 5 атомів карбону знаходяться в другому валентному стані (sp2-гібридизація). Унаслідок циклічного спряження відбувається вирівнювання електронної густини в делокалізованій -електронній системі, яка включає до себе 6 електронів («ароматичний секстет
Однак, якщо на циклопентадієніл-аніон діяти FeCl2, то утворюється цікава ароматична система – дициклопентадієнілферум , або фероцен, що побудований, як показує рентгеноструктурний аналіз, сендвічеподібно (Посон, Вудворд, Уілкінсон):
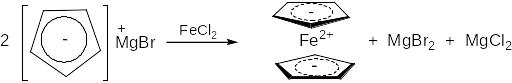
Фероцен є типовою ароматичною сполукою, вступає в реакції електрофільного заміщення, стійкий до окислення тощо.
Тропілій-катіон. У певній мірі антиподом циклопентадієніл-аніону є тропілій-катіон, який утворюється за такою схемою (Дьорінг):
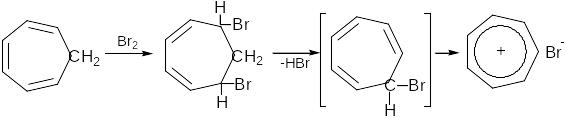 У
молекулі бензену всі 6 атомів Карбону
знаходяться в другому валентному стані
(sp2-гібридизація).
Оскільки гібридні орбіталі всіх атомів
Карбону лежать в одній площині (під
кутом 1200),
бензен являє собою плоску молекулу.
р-Електрони, що не брали участь в
гібридизації мають взаємнопаралельні
(копланарні) вісі симетрії, внаслідок
чого відбувається утворення делокалізованої
-електронної
системи.
Завдяки цьому відбувається утворення
міцних хім. зв’язків і стабілізація
молекули у цілому, що обумовлює появу
«ароматичних» властивостей.
У
молекулі бензену всі 6 атомів Карбону
знаходяться в другому валентному стані
(sp2-гібридизація).
Оскільки гібридні орбіталі всіх атомів
Карбону лежать в одній площині (під
кутом 1200),
бензен являє собою плоску молекулу.
р-Електрони, що не брали участь в
гібридизації мають взаємнопаралельні
(копланарні) вісі симетрії, внаслідок
чого відбувається утворення делокалізованої
-електронної
системи.
Завдяки цьому відбувається утворення
міцних хім. зв’язків і стабілізація
молекули у цілому, що обумовлює появу
«ароматичних» властивостей.
47. Гетероциклічні ароматичні системи.
Якщо до складу циклу поряд з атомами Карбону входять атоми інших елементів (гетероатоми), такі цикли називають гетероциклами. Найбільш поширеними гетероатомами є атоми Оксигену, Нітрогену, Сульфуру.
Розрізняють гетероцикли насичені і ненасичені. Серед останніх певна частина проявляє властивості ароматичних сполук. Ізоелектронними вважаються такі гетеро- і карбоцикли, в яких є одна й та ж кількість ланок (р-орбіталей, що належать атомам у другому валентному стані) і π-електронів.
П’ятичленні гетероцикли з одним гетероатомом – фуран (А.), пірол (Б.) і тіофен (В.), і є ізоелектронними циклопентадієніл-аніону, відносяться до ароматичних сполук:
А.![]() Б.
Б.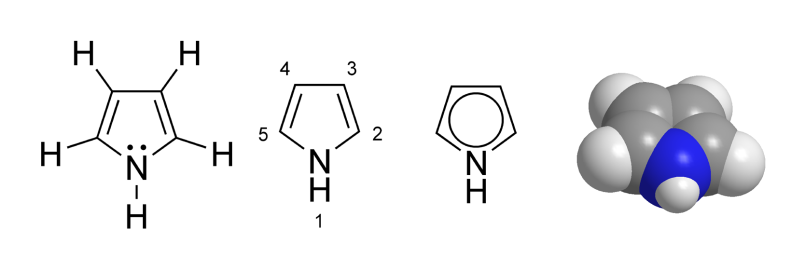 В.
В.![]()
Ці сполуки циклічні, плоскі, копланарні і мають у делокалізованій π-електронній системі шість електронів, що відповідає правилу Хюккеля.
Оскільки гетероатом має на своїй р-орбіталі вдвічі більше електронів, ніж атоми Карбону, він відіграє роль електронодонорного замісника – при утворенні делокалізованої π-електронної системи на атомах Карбону в циклі електронна густина зростає, та гетероатом набуває частково позитивного заряду, п’ятичленні гетероцикли з одним гетероатомом більш активні в реакціях електрофільного заміщення, ніж бензен.
З бензеном ізоелектронні такі шестичленні гетероцикли:
![]()
![]()
Піридин Піримідин
Усі ці сполуки проявляють ароматичні властивості, але в різній мірі. Енергія резонансу фурану, піролу і тіофену = відповідно 15, 21 і 28 ккал/моль. Це означає, що тіофен більш ароматичний, ніж фуран. Енергія резонансу піридину і піримідину найбільш близька до енергії резонансу бензену, що свідчить про високу ступінь ароматичності цих сполук.
Високоароматичною є структура порфіну, в делокалізованій π-електронній системі якого міститься 18 π-електронів. Ця сполука має плоску будову. Вона надзвичайно стійка до нагрівання, дії окислювачів. Для неї характерні кільцеві струми π-електронів.
Атом Нітрогену в молекулах піролу і піридину знаходиться у стані sp2-гібридизації, але р-орбіталі містять різну кількість електронів. У молекулах імідазолу і піразолу один із атомів Нітрогену такий, як в піролі, а другий – такий, як в піридині. У цілому всі ці гетероцикли мають «ароматичний секстет» π-електронів.
Таким чином, поняття ароматичності достатньо багатозначне. Концепція ароматичності постійно розвивається і сьогодні вже вийшла за межі тільки органічної хімії. У наш час вже відомі циклічні неорганічні сполуки, що мають всі ознаки ароматичних систем. Ця концепція виявилась плідною, наприклад, для тривимірних систем, пірамідальних структур тощо.
Якщо циклічні системи формально мають супряження -електронів, але не відповідають правилу Хюккеля, то при цьому зростає енергія дело-калізації -електронів і такі системи можуть бути неароматичними або антиароматичними
48. Основи теорії хімічних перетворень
В основі теорії перехідного стану використовуються наступні положення:
1) Зіткнення часток призводить до утворення зв'язку між ними.
Нестійкий стан, в якому існують зв'язки між усіма частинками, називається перехідним станом. Його також представляють як комплекс, тимчасово утворений взаємодіючими частинками, і називають активним комплексом.
утворення і розпад активного комплексу відбувається тільки в одному напрямку.
2) Порядок утворення і розпаду комплексу такий. Взаємодіючі частинки рухаються один до одного до тих пір, поки між ними не виникне додатковий зв'язок, утворення якої призводить до ослаблення зв'язку, вже існуючої в одній з взаємодіючих молекул. Потім частинки починають розходитися. Ослаблена раніше існуючий зв'язок зникає, а виникнувший при зближенні частинок новий зв'язок залишається.
Даний постулат забороняє розпад активного комплексу на вихідні частинки. Він може розпадатися тільки з утворенням продуктів реакції.
3) утворення активного комплексу не призводить до порушення розподілу часток за швидкостями і енергій Максвелла - Больцмана.
4) Передбачається, що зміщення електронних орбіталей в частинках при утворенні активного комплексу відбувається у багато разів швидше, ніж рух атомних ядер.
Енергія активації в теорії перехідного стану має чітке трактування як величина енергетичного бар'єра, що дорівнює різниці енергій в перехідному і вихідному станах.
У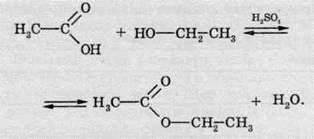 лабораторії
естери добувають, в основному, кип’ятінням
карбонових кислот зі спиртами в
присутності сульфатної кислоти. У цьому
разі сульфатна кислота відіграє роль
каталізатора й водовідіймальної
речовини, тобто вона зв’язує утворювану
воду й не дозволяє їй вступати у зворотну
реакцію гідролізу утворюваного
естеру(реакція
естерифікації)
лабораторії
естери добувають, в основному, кип’ятінням
карбонових кислот зі спиртами в
присутності сульфатної кислоти. У цьому
разі сульфатна кислота відіграє роль
каталізатора й водовідіймальної
речовини, тобто вона зв’язує утворювану
воду й не дозволяє їй вступати у зворотну
реакцію гідролізу утворюваного
естеру(реакція
естерифікації)
Реакція естерифікації є оборотною реакцією: поряд з реакцією утворення естеру відбувається зворотна реакція – реакція гідролізу.
Хімічні перетворення частіше супроводжуються гемолітичним розщепленням зв'язків С-Н з подальшим заміщенням атома Гідрогену на інші атоми або групи атомів, і для них характерні реакції заміщення, які відбуваються за радикальним механізмом (SR)
Атом галогену, сполучений з атомом Карбону, може легко витіснятися нуклеофілом у вигляді аніона, наприклад, гідроксид-іоном, який має електронну пару.
SN. Нуклеофільна реакція заміщення відбувається у два етапи. На 1-у етапі в результаті виходу негативно зарядженої частинки утворюється карбкатіон.2-й етап є іонною реакцією карбкатіона з багатим на електрони нуклеофілом.
SN1-механізм — це дворівневий процес: спочатку йде повільне утворення карбокатіону, потім цей іон швидко реагує з ОН-, утворюючи молекулу спирту.
SN2-механізм. При цьому нуклеофільному заміщенні процес проходить однорівнево. Нуклефіл ОН- атакує атом Карбону з боку, протилежного до атома Брому, що заміщується. В результаті атаки реалізується перехідний стан, в якому починає утворюватися зв’язок HO—С і одночасно починає розриватися зв’язок С—Вr. Нуклеофіл ОН-, що атакується атомом Карбону, і атом Брому лежать на одній прямій, три атоми Гідрогену й атом Карбону, що атакується, розташовані в площині, перпендикулярній до цієї прямої. Процес завершується утворенням нового зв’язку С—ОН і повним розривом зв’язку С—Вr.