Материал: магістерський іспит з хімії 1
49. Заміщення біля атому Карбону.
Хімічні перетворення частіше супроводжуються гемолітичним розщепленням зв'язків С-Н з подальшим заміщенням атома Гідрогену на інші атоми або групи атомів, і для них характерні реакції заміщення, які відбуваються за радикальним механізмом (SR)
Атом галогену, сполучений з атомом Карбону, може легко витіснятися нуклеофілом у вигляді аніона, наприклад, гідроксид-іоном, який має електронну пару.
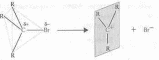 SN1-механізм.
Нуклеофільна реакція заміщення
відбувається у два етапи. На 1-у етапі в
результаті виходу негативно зарядженої
частинки утворюється карбкатіон.
SN1-механізм.
Нуклеофільна реакція заміщення
відбувається у два етапи. На 1-у етапі в
результаті виходу негативно зарядженої
частинки утворюється карбкатіон.
 2-й
етап є іонною реакцією карбкатіона з
багатим на електрони
2-й
етап є іонною реакцією карбкатіона з
багатим на електрони
нуклеофілом.
SN1-механізм — це дворівневий процес: спочатку йде повільне утворення карбокатіону, потім цей іон швидко реагує з гідроксид-іоном, утворюючи молекулу спирту.
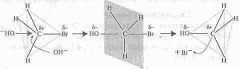 SN2-механізм.
При
цьому нуклеофільному заміщенні процес
проходить однорівнево. Нуклефіл
ОН- атакує
атом Карбону з боку, протилежного до
атома Брому, що заміщується. В результаті
атаки реалізується перехідний стан, в
якому починає утворюватися зв’язок HO—С
і одночасно починає розриватися зв’язок
С—Вr.
Нуклеофіл ОН-,
що атакується атомом Карбону, і атом
Брому лежать на одній прямій, три атоми
Гідрогену й атом Карбону, що атакується,
розташовані в площині, перпендикулярній
до цієї прямої. Процес завершується
утворенням нового зв’язку С—ОН і повним
розривом зв’язку С—Вr.
SN2-механізм.
При
цьому нуклеофільному заміщенні процес
проходить однорівнево. Нуклефіл
ОН- атакує
атом Карбону з боку, протилежного до
атома Брому, що заміщується. В результаті
атаки реалізується перехідний стан, в
якому починає утворюватися зв’язок HO—С
і одночасно починає розриватися зв’язок
С—Вr.
Нуклеофіл ОН-,
що атакується атомом Карбону, і атом
Брому лежать на одній прямій, три атоми
Гідрогену й атом Карбону, що атакується,
розташовані в площині, перпендикулярній
до цієї прямої. Процес завершується
утворенням нового зв’язку С—ОН і повним
розривом зв’язку С—Вr.
Механізм реакціїSNi або реакції внутрішньомолекулярного нуклеофільного заміщення протікає в кілька стадій за аналогією з механізмом SN1, однак частина заміщеної групи при цьому атакує субстрат, відщеплюючись від решти.
Загальна схема реакції:
1.Йонізація
субстрата:![]() 2.Нуклеофільная
атака:
2.Нуклеофільная
атака:![]()
На першому етапі субстрат дисоціює з утворенням контактної іонної пари. Компоненти такої пари знаходяться дуже близько один від одного, тому атака нуклеофіла вимушено відбувається з тієї ж сторони, де до цього перебувала відщеплена група.Реакції, що протікають за механізмом SNi, вкрай рідкісні. Одним із прикладів може служити взаємодія спирту з SOCl2
В реакції SNi конфигурація реакційного центра залишаєтьсянезмінною.
Відщеплення (,-елімінування) – це реакція протилежна реакції приєднання за подвійним зв’язком:
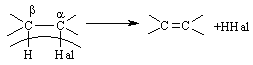
50. Електрофільне і нуклеофільне заміщення в ароматичному ряду.
Реакції нуклеофільного заміщення атома галогену, зв’язаного з ароматичним ядром
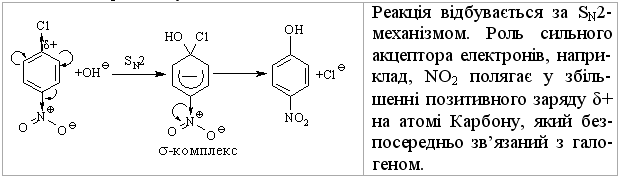
Х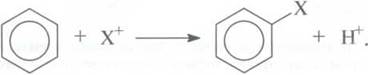 арактерною
реакцією бензену й інших ароматичних
сполук є електрофільне заміщення, при
якому ароматична система зберігається:
арактерною
реакцією бензену й інших ароматичних
сполук є електрофільне заміщення, при
якому ароматична система зберігається:
Електрофільне заміщення в ароматичних сполуках проходить у три етапи.
1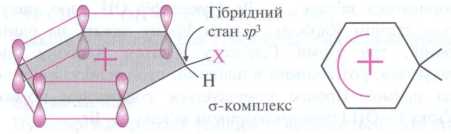 -й етап:
отримання активної електрофільної
частинки (Х+)
переважно за допомогою каталізатора.
-й етап:
отримання активної електрофільної
частинки (Х+)
переважно за допомогою каталізатора.
2-й етап: електрофільна частинка «атакує» негативно заряджену π-електронну хмару бензену, утворюючи π-комплекс. Із я-комплексу повільно формується перехідний стан позитивно зарядженого σ-комплексу.
3-й етап: утворюється продукт з відщеплюванням протона.
Реакції перегрупування (молекулярні перегрупування) — хімічні реакції, в результаті яких відбувається зміна взаємного розташування атомів у молекулі унаслідок переміщення мігруючої групи від одного атома до іншого із розривом та утворенням σ-зв'язків.
Реакція перегрупування супроводжується розривом σ-зв'язку. Залежно від типу частинки, що при цьому утворюється, перегрупування поділяються на:
Аніонотропні чи нуклеофільні — електронна пара зв'язку, що розривається відходить до мігруючої групи із утворенням карбаніона, який переміщується до електронодефіцитного центру (напр. перегрупування Гофмана, перегрупування Вольфа).
Радикальні — Електронна пара розривається із утворенням двох радикалів, мігрує група із одним неспареним електроном (радикала) (напр. ди-π-метанове перегрупування)
Катіонотропні чи нуклеофільні — електронна пара залишається на початковому місці міграції, утворюється мігруюча група із вакантноюмолекулярною орбіталлю(Карбокатіон), яка рухається до центру з надлишковою електронною густиною.
Прототропні — при перегрупуванні мігрує йон Гідрогену.
Під час внутрішньомолекулярного перегрупування мігруюча група весь час зберігає зв'язок із початковим та кінцевим місцем міграції. При цьому циклічний перехідний стан може бути як неароматичним, так і ароматичним за Гюккелем чи Мьобіусом.
51.Поняття хімічної номенклатури
Система офіційних назв хімічних речовин, хімічних реакцій, методів, апаратів і теоретичних концепцій має назву хімічної номенклатури.
Старі, досить образні, але безсистемні назви, які давалися речовинам на підставі джерела їх одержання, їх властивостей або за ім'ям вченого, який вперше їх одержав, наприклад такі, як нашатирний спирт (spiritsofhartshorn), cоляна кислота (muriaticacid), глауберова сіль (Glauber'ssalt), відносяться до так званої тривіальної (історичної) номенклатури і виходять з користування в якості офіційних назв цих речовин.
Відсутність єдиної хімічної номенклатури дуже ускладнювало обмін науковою інформацією і, в решті решт, гальмувало розвиток хімічної науки. Історії науки відомі факти, коли хіміки одержували одну й ту ж речовину, але давали їй різні назви.
Не змогла вирішити проблеми і так звана раціональна номенклатура, що була основана на деяких аспектах теорії будови органічних сполук. В рамках цієї номенклатури певні класи сполук розглядаються з точки зору поняття про гомологічні ряди. Гомологічним рядом називається сукупність сполук, що різняться між собою лише кількістю метиленових груп -СН2- в молекулі. Члени даного гомологічного ряду можна розглядати як похідні найпростішого члена цього ряду, одержані шляхом заміщення одного або декількох атомів Гідрогену на алкільні замісники. За основу береться назва першого члена гомологічного ряду, а всі інші члени цього ряду розглядаються як відповідні похідні
CH3-OH CH3-CH2-OH CH3-CH-OH
CH3
Карбінол Метилкарбінол Диметилкарбінол
Систематична номенклатура повинна давати однозначну назву будь якій органічній сполуці. Систематичною вона зветься тому, що назви сполук не придумуються а будуються на підставі системи розроблених правил. Вона повинна відповідати також вимогам зворотності, тобто можливості однозначного перекладу найменувань на мову класичних структурних формул.
Основи такої номенклатури були закладені у 1892 році на Женевському конгресі хіміків (женевські правила). Женевська номенклатура була задумана як номенклатура офіційна для словників, довідників, покажчиків, причому певній структурній формулі повинна відповідати одна і тільки одна офіційна назва.
Женевська номенклатура складається з 62 правил, які встановлюють порядок складання офіційних назв для вуглеводнів ациклічної будови та їх похідних з одним або декількома однаковими замісниками.
Замісники – нейтральні групи атомів, зв'язані тим чи іншим чином між собою. Наприклад: CH3-; -OH; -NO2; -COOH і інш. Вони заміщують один атом Гідрогену в органічних сполуках. Нейтральні групи атомів, що мають більше як одну вільну валентність, називають групою. Наприклад: >C=O – карбонільна група, >С=NH – іміногрупа і т.п. Терміну радикал, як фрагменту молекули, слід по можливості уникати, щоб не не плутати їх з частками, що мають вільний електрон.
Локант. Це слово означає цифру або літеру, що вказують на положення того чи іншого замісника в молекулі. Наприклад: 1,3-дихлорпропан, β-амінопропіонова кислота. Іноді локантом може бути слово: орто-динітробензен.
Числові префікси -

52. Номенклатура неорганічних сполук.
Для створення назв хімічних сполук існують єдині правила, які розроблені Комісією з номенклатури IUPAC.
Назви більшості елементів походять від латинських назв. Наприклад: Borum – Бор, Natrium – Натрій, Kalium – Калій, Magnium – Маґній, Chlorum – Хлор.
Елементи, що у вигляді простих речовин були відомі давно (залізо, срібло, золото, мідь, пізніше ртуть, азот, вуглець. Схвалили рішення Замість тривіальних термінів, таких як миш'як, кремній, сурма, вісмут, марганець, вживають міжнародні, латинські за походженням назви Арсен (As), Силіцій (Si), Стибій (Sb), Бісмут (Bi), Манґан (Mn). Паралельно можна використовувати і традиційні українські назви для таких елементів як Водень, Азот, Кисень, Сірка, Нікель тощо.
Назви простих речовин пишуть з малої літери.Якщо число структурних одиниць є невизначеним, то використовують префікси полi- та цикло-. Приклад: S8 – цикло-октосульфур, цикло-октосірка; Pn – цикло-полiфосфор.
Для твердих поліморфних модифікацій можна використовувати їх позначення грецькими літерами, а також використовувати назви за однією з ознак: кольором, кристалічним станом або кристалічною структурою.α-Fe – альфа-залізо; α-Sn – α-станум, α-олово, сірий станум; β-Sn – β-станум, β-олово, білий станум; γ-Sn – γ-станум, γ-олово, ромбічний (ромб) станум, крихкий станум; S8 – кристалічна сірка.
Номенклатура оксидів. Назви оксидів можна будувати за допомогою латинських та грецьких числових множників (множних префіксів):
Спочатку називають числовий множник атома металу чи неметалу, що утворює оксид, потім – систематичну назву цього атома в називному відмінку, далі називають числовий множник атома Оксисену і насамкінець додається слово "оксид".
Наприклад: N2O5 – динітроген пентаоксид; Al2O3 – діалюміній триоксид.
Якщо елемент утворює лише один оксид, то назва його може складатися лише з назви елемента та слова оксид: BaO – барій оксид; ZnO – цинк оксид.
Сполуки, що містять угрупування О22-, О2- та О3- називають відповідно: К2О2 – калій пероксид, КО2 – калій надпероксид, КО3 – калій озонід.
Сполуки оксигену з флуором (фтором): ОF2 –оксиген дифлуорид, О2F2 – диоксиген дифлуорид.
Номенклатура комплексних сполук будується за тими ж принципами, що й назви простих, але враховується їх хімічна природа:
– сполуки, що містять комплексні катіони - [Ag(NH3)2]Cl – діамінаргентум (І) хлорид, [Cu(NH3)4](OH)2 – тетраамінкупрум (ІІ) дигідроксид;
– сполуки, що містять комплексні аніони – Na[Al(OH)4] – натрій тетрагідроксоалюмінат, K3[Fe(CN)6] – калій гексаціаноферат (ІІІ), K4[Fe(CN)6] – калій гексаціаноферат (ІІ),
– нейтральні комплекси – [Ni(CO)4] – тетракарбонілнікол, [Cr(H2O)3F3] – трифлуоротриаквахром (ІІІ).
53. Номенклатура iupac органічних сполук.
Номенклатура органічних сполук ІЮПАК — система найменувань номенклатури органічних сполук: тривіальна, раціональна (радикальна), міжнародна (IUPAC).
Тривіальна номенклатура. Перші назви, які давали органічним сполукам, найчастіше відображали способи добування речовин (пірогалол — продукт піролізу галової кислоти), їх відмінні властивості або природне джерело, з якого сполуку вперше було виділено (мурашина кислота, лимонна кислота, тощо).
Раціональна (радикальна) номенклатура. Головний принцип цієї номенклатури полягає в тому, що будь який член будь якого ряду розглядається як похідне від родоначальника цього ряду. Наприклад, алкани розгалуженої будови розглядаються як похідні метану, в молекулі якого атоми Гідрогену заміщені на радикали. За основу назви вибирають центральний (метановий) атом Карбону, який має найбільше замісників. Найчастіше — це третинний або четвертинний атом Карбону; записують назви замісників (радикалів), сполучених з метановим Карбоном, починаючи з найменшого. Однакові радикали об'єднують префіксами (ди — 2, три — 3, тетра — 4); в кінці назви складного алкану додають слово метан. Для назв складних хімічних структур раціональна номенклатура не придатна.
56. Концентрація і розподіл як стадії пробопідготовки.
Підготовка проби до аналізу включає декілька стадій:
Висушування проби. 2. Розкладання проби. 3. Усунення впливу заважаючих компонентів: маскування, розділення.
Існують мокрий та сухий способи розкладання. Мокрий – це розчинення проби у воді, кислотах та їх сумішах, лугах, органічних розчинниках, при цьому розчинення відбувається за рахунок перебігу реакцій обміну, окиснення і комплексоутворення.
Методи маскування: Маскування- це спосіб усунення впливу заважаючих (сторонніх)
компонентів без їх відокремлення.
Способи маскування: 1. Зміна ступеню окиснення визначуваного або заважаючого компонента. 2. Зв’язування домішок у комплексну сполуку.
При неможливості замаскувати заважаючий компонент необхідно використовувати розділення. При визначенні дуже малих вмістів компонента не завжди можна підібрати методику, яка характеризується високою чутливістю. В такому випадку виникає необхідність сконцентрувати мікрокомпонент.
Операція, яка дозволяє розділити компоненти суміші, носить назву розділення. Концентрування - це операція, яка дозволяє підвищити концентрацію мікродомішок елемента, який необхідно визначати. При розділенні концентрації компонента, який визначають, і компонента, вплив якого не бажаний, можуть бути близькими і досить різними. Концентрування ж проводять в умовах різкої різниці концентрацій мікро- і макрокомпонентів.
При концентруванні речовину, яка має малу концентрацію, збирають у меншому об’ємі або масі - це є абсолютне концентрування. Абсолютне концентрування- це операція, яка дозволяє підвищитиконцентрації мікродомішок і макрокомпонента. Для цього проводять частковевипаровування або виморожування матриці (розчинника).
Відносне концентрування- підвищення співвідношення концентрацій мікрокомпонента і макрокомпонента. Здійснюють шляхом переведення мікрокомпонента і частини макрокомпонента в іншу фазу - осад, органічний розчинник, тощо.
Існує декілька класифікацій методів розділення. Найчастіше їх класифікують за фазовим станом системи. Раціонально навести класифікацію методів розділення та концентрування за фазовою ознакою, яка складає чотири групи:
I – нову фазу утворює речовина, яка відокремлюється: осадження, електроосадження, відгонка, кристалізація, сублімація та виморожування;
II – використання різниці у розподілі речовин між фазами: екстракція, співосадження, хроматографічні методи (іонний обмін, сорбція тощо);
III – використання різниці у масоперенесенні, яка спостерігається при переході з однієї фази в другу через третю (мембрану): діаліз, електродіаліз, ультрацентрифугування тощо.
IV – застосування механізму внутрішньофазового розділення за рахунок різниці у властивостях іонів, молекул, атомів в межах однієї гомогенної системи.
Більшість методів розділення ґрунтується на використанні двох фаз, які не змішуються: рідина-рідина, рідина-тверда фаза, рідина-газ.
Осадження використовують найчастіше для розділення неорганічних сполук.
Співосадження - це складний процес захвату мікрокомпонентів осадом макрокомпоненту за рахунок адсорбції, абсорбції, іонного обміну тощо.Екстракція ґрунтується на розподілі речовини між двома рідкими фазами, які не змішуються. Цей метод застосовується в аналізі для відокремлення із суміші одного чи декількох компонентів, а також для збагачення суміші цими компонентами. Тобто, екстракція - це метод і розділення, і концентрування.