Материал: Лебухов ФХ методы исслдния292-325

312 ЧАСТЬ I. ТЕОРИЯ: ФИЗИКО ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Тонкослойная хроматография находит применение при исследовании некоторых видов пищевых продуктов на безопасность, например для выявления токсинов (аф латоксинов, микотоксинов, патулина и др.) в арахисе, зер новых, овощах, фруктах, напитках; для определения пе стицидов (ДДТ и др.) в растительных и животных продук тах, гистамина как показателя порчи рыбы. Кроме того, ТСХ часто сочетают с газовой хроматографией, электро форезом и другими методами.
6.4. ХРОМАТОГРАФИЯ НА БУМАГЕ
По механизму разделения различают распределитель ную, адсорбционную, осадочную и другие виды бумаж ной хроматографии (БХ). В распределительной жидкость жидкостной хроматографии бумага, приготовленная из специальных сортов хлопка, исполняет роль носителя не подвижной жидкой фазы (НФ), в качестве которой часто выступает адсорбированная вода. В таком случае гидро фильная бумага используется для нормально фазовой хроматографии. Растворителями (ПФ) являются спирты (метанол, этанол, н пропанол, бутанол), простые эфиры (этиловый, метиловый), кетоны (ацетон, ацетилацетон), эфиры органических кислот (метилацетат, этилацетат), пиридин, хлороформ. Чаще используются смеси раство рителей. Так, для разделения неорганических неполяр ных веществ употребляют системы:
ацетон : HCl : H2O (в различных соотношениях);
H бутанол, насыщенный НCl (различной концентра ции);
H бутанол : 0,1М HNO3 : ацетилацетон.
Для разделения некоторых органических веществ ис пользуют метод обращенных фаз. В этом методе для при дания бумаге гидрофобного характера ее импрегнируют (пропитывают) нафталином, парафином, раствором кау чука, силиконом и др. Такая бумага служит носителем для неполярных растворителей в качестве НФ. В качестве ПФ применяют смеси кислот с низшими спиртами.

Глава 6. Методы хроматографического анализа |
313 |
Рис. 6.7
Виды бумажной хроматографии
Обращенно фазовая бумажная хроматография исполь зуется, например, для разделения и идентификации по линасыщенных жирных кислот при изучении состава липидов, выделенных из животных тканей. Бумагу про питывают 5% ным раствором силикона, в качестве ПФ используют 85% ный раствор уксусной кислоты.
Разделение веществ в распределительной БХ осуще ствляется благодаря различию в скоростях движения ком понентов при многократном повторении актов экстракции и сорбции. Скорость перемещения компонентов зависит от их коэффициентов распределения (как и в методе экст ракции).
По направлению движения элюента (ПФ) различают восходящую, нисходящую и радиальную (круговую) хро матографию (рис. 6.7). Если элюент движется по бумаге вверх, метод называют восходящей (а) бумажной хрома тографией; при его движении сверху вниз — нисходящей (б) бумажной хроматографией. Очень быстро можно осу ществить хроматографический анализ методом радиаль ной (в) бумажной хроматографии, в котором использует ся бумажный круг (г) с фитилем, опущенным в элюент.
Иногда при сложном составе пробы не удается разде лить ее компоненты с помощью одного растворителя. Тог да применяют двумерную хроматографию. В угол квадрат ного листа хроматографической бумаги наносят раствор

314 ЧАСТЬ I. ТЕОРИЯ: ФИЗИКО ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Рис. 6.8
Двумерная хроматография
пробы и хроматографируют сначала в одном элюенте, за тем, повернув хроматограмму на 90 , — в другом. Первый элюент производит предварительное разделение компо нентов пробы, второй — окончательное (рис. 6.8).
Для хроматографии на бумаге используют стеклянные герметизированные камеры. Внутри камеры в верхней (нисходящий вариант) или нижней ее части (восходящий вариант) помещают сосуд для подвижной фазы (лодочку).
Радиальную хроматографию можно осуществить в чаш ке Петри. Детекцию зон, идентификацию и количествен ное определение в БХ проводят так же, как и в методе тон кослойной хроматографии.
Методом распределительной жидкостной бумажной хроматографии успешно анализируют смеси катионов в неорганическом качественном анализе, смеси аминокис лот и других органических кислот, пептидов, пестицидов, фенолов, красителей, синтетических поверхностно актив ных веществ.
6.5.
ЭЛЕКТРОФОРЕЗ
Метод анализа, основанный на способности заряжен ных частиц к передвижению во внешнем электрическом поле, называют электрофорезом (греч. phoresis — пере несение). Электрофорез относится к методам разделения без превращения веществ, на основе заряда частиц. По тех нике выполнения метод аналогичен хроматографии.
Нередко под электрофорезом понимают перемещение коллоидных частиц или макромолекул (в отличие от ионо

Глава 6. Методы хроматографического анализа |
315 |
фореза — перемещения неорганических ионов малого размера).
Передвижение частиц при электрофорезе зависит от ряда факторов, основными из которых являются: напря женность электрического поля; величина электрическо го заряда; скорость и размер частицы; вязкость, рН и тем пература среды; продолжительность электрофореза.
Электрофорез можно проводить как в свободном ра створе (фронтальный электрофорез), так и на носителях (зональный электрофорез). Последний вариант более пред почтителен, так как носители способствуют стабилизации электрофоретических зон. В качестве носителей исполь зуют: фильтровальную бумагу, силикагель, крахмал, ок сид алюминия, поливинилхлорид, агаровый или полиак риламидный гель и др. Электрофоретическое разделение осуществляют на бумаге, в тонком слое сорбента, колонке или в блоке, который часто формируют из суспензии крах мала в подходящем электролите.
Аппаратура для электрофореза выполняется по еди ной схеме: источник тока, камера для электрофореза, два электрода, соединяющих камеру с источником тока, и приспособление для сбора и идентификации разделенных веществ (последний блок в некоторых случаях отсутству ет). Для электрофореза используются как готовые наборы аппаратуры (универсальный прибор для иммуноэлектро фореза и электрофореза белков на бумаге и крахмале, на бор для электрофореза в полиакриламидном геле венгерс кой фирмы «Реанал»), так и наборы, составляемые экспе риментатором из отдельных приборов.
На рисунке 6.9 представлена схема прибора для элек трофореза на бумаге. Электрофоретическая камера состо ит из двух кювет, в которые помещают графитовые элект роды и раствор проводящей жидкости (буферный раствор). Выше кювет располагается подставка для носителя бума ги. Смесь веществ, подлежащих разделению, наносят на бумагу, пропитанную проводящей жидкостью. Бумагу подсушивают, помещают на подставку, концы погружа ют в кюветы, затем камеру плотно закрывают крышкой. После пропитывания бумаги проводящей жидкостью под
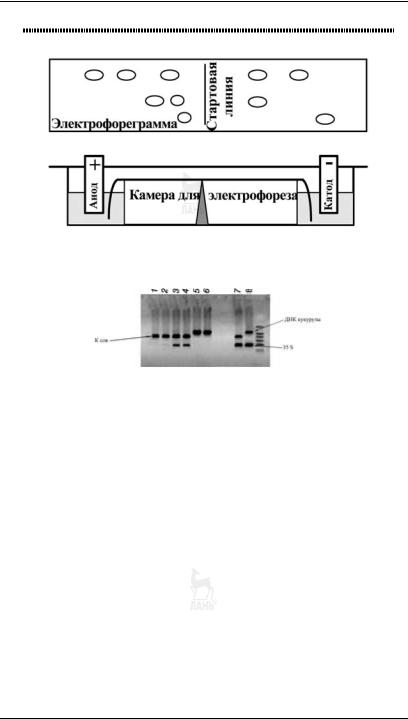
316 ЧАСТЬ I. ТЕОРИЯ: ФИЗИКО ХИМИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
Рис. 6.9
Схема прибора для электрофореза
Рис. 6.10
Электрофореграмма образцов на наличие генетически модифицированных ингридиентов
с помощью тест системы «АмплиСенс®ПЛАНТ,СКРИН»:
1, 2 — соевая мука, не содержащая ГМ сои; 3, 4 — соевая мука, содержащая ГМ сою; 5, 6 — кукурузная мука, не содержащая ГМ кукурузы; 7 — положительный контроль ПЦР ГМ сои 40 3 2; 8 — положительный контроль ПЦР ГМ кукурузы MON 810; ок — отрицательный контроль выделения ДНК; к — отрицательный контроль ПЦР.
ключают электрический ток. По окончании электрофоре за бумагу подсушивают. Качественную и количественную оценку осуществляют, применяя методы, используемые в бумажной хроматографии, например, проявление бел ков с помощью красителей, метод денситометрии.
Важной областью применения электрофореза являет ся анализ белков сыворотки крови, аминокислот, гидро лизатов белков, нуклеиновых кислот и т. п. В кислотном буферном растворе аминокислота находится в виде кати она NH3+...СООН, который перемещается к катоду, в то время как в щелочном буфере аминокислота превращает