Материал: Курс занятий. Липиды
Биосинтез холестерина
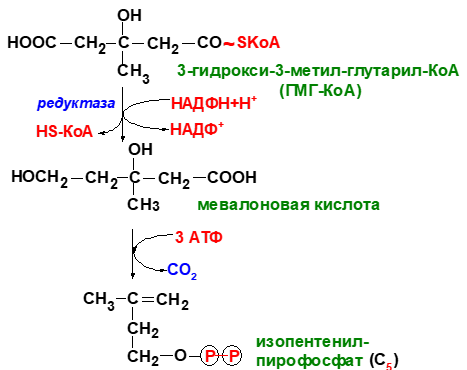
1 стадия – синтез мевалоновой кислоты
2 стадия – конденсация
3 стадия - циклизация
Регуляция ключевого фермента синтеза хо-лестерола (ГМГ-КоА-редуктазы) происходит разными способами.
Фосфорилирование/дефосфорилирование ГМГ-КоА-редуктазы
П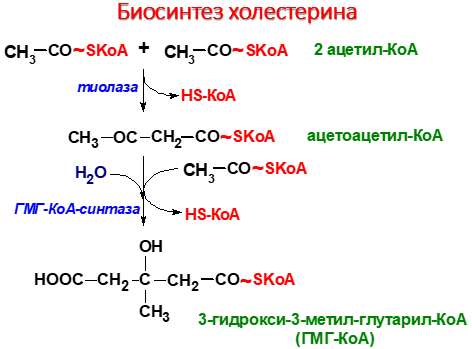
 ри
увеличении соотношения инсулин/глюкагон
этот фермент дефосфорилируется и
переходит в активное состояние. Действие
инсулина осуществляется через 2
фермента: фосфатазу
киназы ГМГ-КоА-редуктазы, которая
превращает киназу в неактивное
дефосфо-рилированное состояние; фосфатазу
ГМГ-КоА-редуктазыпутём
превращения её в дефосфорилированное
активное состояние. Результатом этих
реакций служит образование
дефосфорилированной активной формы
ГМГ-КоА-редуктазы. Следовательно, в
абсорбтивный период синтез холестерола
увеличивается. В этот период увеличивается
и доступность исходного субстрата для
синтеза холестерола - ацетил-КоА (в
результате приёма пищи, содержащей
углеводы, так как ацетил-КоА образуется
в основном при распаде глюкозы). В
постабсорбтивном состоянии глюкагон
через протеинкиназу А стимулирует
фосфо-рилирование ГМГ-КоА-редуктазы,
переводя её в неактивное состояние. Это
действие усиливается тем, что одновременно
глюкагон стимулирует фосфорилирование
и инактивацию фосфатазы ГМГ-КоА-редук-тазы
и фосфорилирование киназы ГМГ-КоА-редуктазы,
удерживая, таким образом, ГМГ-КоАредуктазу
в фосфорилированном неактивном состоянии.
В результате синтез холестерола в
постабсорбтивном периоде и при голодании
ингибируется. Ингибирование
синтеза ГМГ-КоА-редуктазы. Конечный
продукт метаболического пути (холестерол)
снижает скорость транскрипции гена
ГМГ-КоА-редуктазы, подавляя таким образом
собственный синтез. В печени активно
идёт синтез жёлчных кислот из холестерола,
поэтому и жёлчные кислоты (как конечные
продукты синтеза) подавляют активность
гена ГМГ-КоА-редуктазы. Так как молекула
ГМГ-КоА-редук-тазы существует около 3 ч
после синтеза, то ингибирование синтеза
этого фермента
ри
увеличении соотношения инсулин/глюкагон
этот фермент дефосфорилируется и
переходит в активное состояние. Действие
инсулина осуществляется через 2
фермента: фосфатазу
киназы ГМГ-КоА-редуктазы, которая
превращает киназу в неактивное
дефосфо-рилированное состояние; фосфатазу
ГМГ-КоА-редуктазыпутём
превращения её в дефосфорилированное
активное состояние. Результатом этих
реакций служит образование
дефосфорилированной активной формы
ГМГ-КоА-редуктазы. Следовательно, в
абсорбтивный период синтез холестерола
увеличивается. В этот период увеличивается
и доступность исходного субстрата для
синтеза холестерола - ацетил-КоА (в
результате приёма пищи, содержащей
углеводы, так как ацетил-КоА образуется
в основном при распаде глюкозы). В
постабсорбтивном состоянии глюкагон
через протеинкиназу А стимулирует
фосфо-рилирование ГМГ-КоА-редуктазы,
переводя её в неактивное состояние. Это
действие усиливается тем, что одновременно
глюкагон стимулирует фосфорилирование
и инактивацию фосфатазы ГМГ-КоА-редук-тазы
и фосфорилирование киназы ГМГ-КоА-редуктазы,
удерживая, таким образом, ГМГ-КоАредуктазу
в фосфорилированном неактивном состоянии.
В результате синтез холестерола в
постабсорбтивном периоде и при голодании
ингибируется. Ингибирование
синтеза ГМГ-КоА-редуктазы. Конечный
продукт метаболического пути (холестерол)
снижает скорость транскрипции гена
ГМГ-КоА-редуктазы, подавляя таким образом
собственный синтез. В печени активно
идёт синтез жёлчных кислот из холестерола,
поэтому и жёлчные кислоты (как конечные
продукты синтеза) подавляют активность
гена ГМГ-КоА-редуктазы. Так как молекула
ГМГ-КоА-редук-тазы существует около 3 ч
после синтеза, то ингибирование синтеза
этого фермента
В ыведение холестерина и жёлчных кислот из организма.
Выведение холестерола из организма. Структурная основа холестерола - кольца циклопентанпергидрофенантрена - не может быть расщеплена до СО2 и воды, как другие органические компоненты, поступающие с пищей или синтезированные в организме. Поэтому основное количество холестерола выводится в виде жёлчных кислот. Некоторое количество жёлчных кислот выделяется в неизменённом виде, а часть подвергается действию ферментов бактерий в кишечнике. Продукты их разрушения (в основном, вторичные жёлчные кислоты) выводятся из организма.
Ч асть
молекул холестерола в кишечнике под
действием ферментов бактерий
восстанавливается по двойной связи в
кольце В, в результате чего образуютря
2 типа молекул - холестанол и копростанол,
выводимые с фекалиями. В сутки из
организма выводится от 1,0 г до 1,3 г
холестерола, основная часть удаляется
с фекалиями,
асть
молекул холестерола в кишечнике под
действием ферментов бактерий
восстанавливается по двойной связи в
кольце В, в результате чего образуютря
2 типа молекул - холестанол и копростанол,
выводимые с фекалиями. В сутки из
организма выводится от 1,0 г до 1,3 г
холестерола, основная часть удаляется
с фекалиями,
Нормальный уровень холестерина в крови. Гиперхолестеринемия и ее причины.
Содержание холестерина в норме – 2,9-5,2 ммоль/л.
Диагностическое значение: В норме содержание общего холестерина составляет в среднем 2,9 - 6,5 ммоль/л в зависимости от пола, возраста, характера питания. Из этого количества 70% составляет этерифицированный и 30% - свободный холестерин.
Увеличение содержания холестерина в крови (гиперхолестеринемия) наблюдается при атеросклерозе, сахарном диабете, липоидном нефрозе, микседеме, при механической желтухе, наследственных нарушениях липидного обмена. Гипохолестеринемия характерна для анемии, туберкулеза, гипертиреоза, голодания, раковой кахексии, паренхиматозной желтухи.
К распространенным факторам, влияющим на развитие атеросклероза и повышение уровня холестерина, относятся неправильное питание, малоподвижный образ жизни, ожирение, возраст выше 50 лет, наследственность.
Гиперхолестеролемия обычно развивается вследствие избыточного поступления холестерола с пищей, а также углеводов и жиров. Гиперкалорийное питание - один из распространённых факторов развития гиперхолестеролемии, так как для синтеза холестерола необходимы только ацетил-КоА, АТФ и NADРН. Все эти субстраты образуются при окислении глюкозы и жирных кислот, поэтому избыточное поступление этих компонентов пищи способствует развитию ги-перхолестеролемии. В норме поступление холе-стерола с пищей снижает синтез собственного холестерола в печени, однако с возрастом эффективность регуляции у многих людей снижается.
Биохимия атеросклероза и жёлчнокаменной болезни, факторы риска.
Атеросклероз
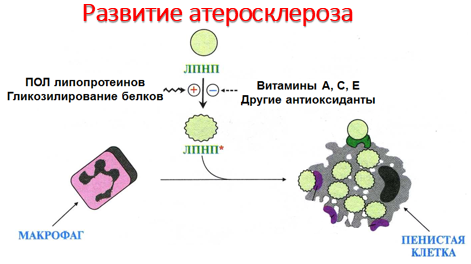
Процесс начинается с повреждения эндотелия сосудов, причём повреждение может иметь различные механизмы. Важнейший механизм - повреждение эндотелия за счёт изменённой структуры ЛПНП, например, в результате активации свободнорадикального ПОЛ в составе ЛПНП; повреждение провоцируется свободными радикалами, образующимися в процессе метаболизма или поступающими извне. В ходе ПОЛ в ЛПНП изменяется не только структура самих липидов, но и нарушается структура апопротеинов. Окисленные ЛПНП захватываются макрофагами через скевенджер-рецепто-ры. Этот процесс не регулируется количеством поглощённого холестерола, как в случае его поступления в клетки через специфические рецепторы, поэтому макрофаги перегружаются холестеролом и превращаются в «пенистые клетки», которые проникают в субэндотелиальное пространство. Это приводит к образованию жировых полосок в стенке кровеносных сосудов. На этой стадии эндотелий сосудов может сохранять свою структуру. При увеличении количества «пенистых клеток» происходит повреждение эндотелия сосудов.
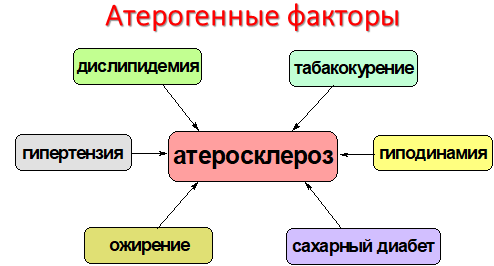
Факторы риска:
- наследственность,
- ожирение
- питание
- гиподинамия
- сахарный диабет
- курение,
- стресс,
- гендерный фактор,
- возраст.
Желчнокаменная болезнь.
- патологический процесс, при котором в жёлчном пузыре образуются камни, основу которых составляет холестерол.
У большинства больных желчнокаменной болезнью активность ГМГ-КоА-редуктазы повышена, следовательно, увеличен синтез холестерола, а активность 7-а-гидроксилазы, участвующей в синтезе жёлчных кислот, снижена. В результате синтез холестерола увеличен, а синтез жёлчных кислот из него замедлен, что приводит к диспропорции количества холестерола и жёлчных кислот, секретируемых в жёлчь.
Если эти пропорции нарушены, то холестерол начинает осаждаться в жёлчном пузыре, образуя вначале вязкий осадок, который постепенно становится более твёрдым. Иногда он пропитывается билирубином - продуктом распада гема, белками и солями кальция. Камни, образующиеся в жёлчном пузыре, могут состоять только из холестерола (холестериновые камни) или из смеси холестерола, билирубина, белков и кальция. Холестериновые камни обычно белого цвета, а смешанные камни - коричневого цвета разных оттенков. Причин, приводящих к изменению соотношения жёлчных кислот и холестерола, в жёлчи много: пища, богатая холестеролом, гиперкалорийное питание, застой жёлчи в жёлчном пузыре, нарушение энтерогепатической циркуляции, нарушение синтеза жёлчных кислот, инфекции жёлчного пузыря. Если камни начинают перемещаться из жёлчного пузыря в жёлчные протоки, то они вызывают спазм жёлчного пузыря и протоков, что больной ощущает как приступ сильной боли.
Причины желчно-каменной болезни
Избыток холестерина в пище
Гиперкалорийное питание
Повышенный синтез холестерина в печени
Снижение синтеза желчных кислот
Застой желчи
Нарушение гепатоэнтеральной циркуляции желчных кислот
Воспалительные заболевания желчного пузыря
Биохимические основы профилактики и лечения атеросклероза.
Диагностическое значение: Индекс атерогенности используется как тест вероятности развития атеросклероза. Эта величина в норме у взрослых составляет 2,0-3,5. При атеросклерозе и его осложнениях она всегда превышает 4,0, в тяжелых случаях патологии этот показатель дос-тигает величин 5,0 и даже 6,0.
Важным лечебным фактором, снижающим риск развития гиперхолестеролемии и атеросклероза, является гипокалорийная и гипохолес-териновая диета. Поступление холестерола с пищей не должно превышать 300 мг/сут.
Холестерол - стероид животного происхождения, поэтому он поступает в организм при употреблении животных жиров и жирного мяса. Растительная пища не содержит холестерола, поэтому у людей среднего и старшего возраста она должна составлять основу рациона.
К лечебным и профилактическим факторам относят обогащение пищи полиеновыми жирными кислотами семейства ω-3, уменьшающими риск тромбообразования. Ненасыщенные жирные кислоты способствуют более быстрому выведению холестерола из организма.
Витамины С, Е, А, обладающие антиоксидантными свойствами, ингибируют перекисное (свободнорадикальное) окисление липидов в ЛПНП и поддерживают нормальную структуру липидов ЛПНП и их метаболизм.
Лечение гиперхолестеролемии, как правило, комплексное.
Один из принципов лечения - «размыкание» цикла энтерогепатической циркуляции жёлчных кислот. Для этого используют лекарства типа холестирамина - полимера, который в кишечнике адсорбирует жёлчные кислоты, выделяется с фекалиями и таким образом уменьшает возврат жёлчных кислот в печень. В печени увеличивается захват холестерола из крови для синтеза новых жёлчных кислот. Препараты типа холестирамина называют секвестрантами жёлчных кислот.
Наиболее эффективные препараты, применяемые при лечении атеросклероза, - ингибиторы ГМГ-КоА-редуктазы. Эти препараты - антибиотики, например, мевакор, в печени трансформируются в активную форму и эффективно ингибируют регуляторный фермент биосинтеза холестерола.
Биосинтез фосфолипидов
Синтез фосфолипидов может происходить в различных тканях и по нескольким путям: в кишечнике с использованием пищевого холина или этаноламина (ресинтез фосфолипидов) и в печени (собственно биосинтез)
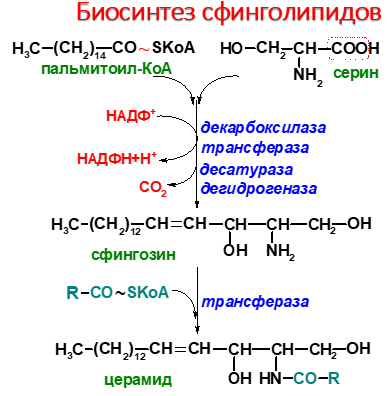
Биосинтез и катаболизм сфинголипидов
С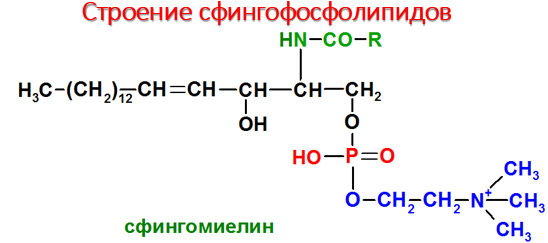 финголипиды
- производные церамида, образующегося
в результате соединения аминоспирта
сфингозина и жирной кислоты. В группу
сфинголипидов входят сфингомиелины и
гликосфинголипиды фингомиелины находятся
в мембранах клеток различных тканей,
но наибольшее их количество содержится
в нервной ткани. Сфингомиелины миелиновых
оболочек содержат в основном жирные
кислоты с длинной цепью: лигноцериновую
(24:0) и нервоновую (24:1) кислоты, а сфингомиелин
серого вещества мозга содержит
преимущественно стеариновую кислоту.
финголипиды
- производные церамида, образующегося
в результате соединения аминоспирта
сфингозина и жирной кислоты. В группу
сфинголипидов входят сфингомиелины и
гликосфинголипиды фингомиелины находятся
в мембранах клеток различных тканей,
но наибольшее их количество содержится
в нервной ткани. Сфингомиелины миелиновых
оболочек содержат в основном жирные
кислоты с длинной цепью: лигноцериновую
(24:0) и нервоновую (24:1) кислоты, а сфингомиелин
серого вещества мозга содержит
преимущественно стеариновую кислоту.
Гликосфинголипиды - гликолипиды, в состав которых входят церамид и один или несколько остатков углеводов, и сиаловая (N-ацетилнейраминовая) кислота узнавание клеток и их взаимодействие. Интересно, что углеводная часть структуры антигенов на поверхности эритроцитов (по системе АВО) может быть связана как с церамидом, так и с белками. В последнем случае структура антигена является не гликолипидом, а гликопротеином.
Некоторые ганглиозиды – рецепторы бактериальных токсинов. Например, GMl, находящийся на поверхности клеток кишечного эпителия, является местом прикрепления холерного токсина - белка, секретируемого возбудителями холеры.
Функции гликосфинголипидов
Взаимодействие между:
клетками;
клетками и межклеточным матриксом;
к
 летками
и микробами.
летками
и микробами.
Модуляция:
активности протеинкиназ;
активности рецептора фактора роста;
антипролиферативного действия (апоптоза, клеточного цикла).
Обеспечение:
структурной жёсткости мембран;
конформации белков мембран.
С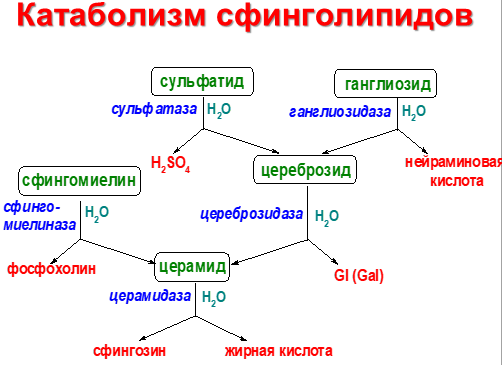 интез
церамида и его производных.
Синтез
сфинголипидов начинается с образования
церамида. Серии конденсируется с
пальмитоил-КоА. Продукт их взаимодействия
сначала восстанавливается коферментом
NADPH, затем к аминогруппе дигидросфингозина
амидной связью присоединяется жирная
кислота, содержащая, как правило, 24 атома
углерода. После окисления FAD-зависимой
дегидрогеназой образуется церамид.
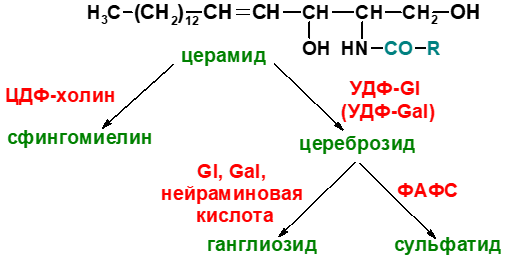
Церамид служит предшественником в
синтезе большой группы сфинголипидов:
сфингомиелинов, не содержащих углеводов,
и гликосфинголипидов. Последующие
реакции синтеза катализируются
специфическими трансферазами, набор
которых отличается в разных тканях.
Соединение фосфорилхолина с церамидом
сфингомиелин-синтазой приводит к
образованию сфингомие-лина. Присоединение
углеводных компонентов катализируется
специфическими гликозилтрансферазами.
Донорами углеводных компонентов служат
активированные сахара: УДФ-галактоза
и УДФ-глюкоза. Галактоцереброзид -
главный липид миелиновых оболочек;
глюкоцереброзид входит в состав мембран
многих клеток и служит предшественником
в синтезе более сложных гликолипидов
или продуктом на пути их катаболизма.
интез
церамида и его производных.
Синтез
сфинголипидов начинается с образования
церамида. Серии конденсируется с
пальмитоил-КоА. Продукт их взаимодействия
сначала восстанавливается коферментом
NADPH, затем к аминогруппе дигидросфингозина
амидной связью присоединяется жирная
кислота, содержащая, как правило, 24 атома
углерода. После окисления FAD-зависимой
дегидрогеназой образуется церамид.
Церамид служит предшественником в
синтезе большой группы сфинголипидов:
сфингомиелинов, не содержащих углеводов,
и гликосфинголипидов. Последующие
реакции синтеза катализируются
специфическими трансферазами, набор
которых отличается в разных тканях.
Соединение фосфорилхолина с церамидом
сфингомиелин-синтазой приводит к
образованию сфингомие-лина. Присоединение
углеводных компонентов катализируется
специфическими гликозилтрансферазами.
Донорами углеводных компонентов служат
активированные сахара: УДФ-галактоза
и УДФ-глюкоза. Галактоцереброзид -
главный липид миелиновых оболочек;
глюкоцереброзид входит в состав мембран
многих клеток и служит предшественником
в синтезе более сложных гликолипидов
или продуктом на пути их катаболизма.
Катаболизм сфингомиелина. В лизосомах находятся ферменты, способные гидролизовать любые компоненты клеток. Эти ферменты называют кислыми гидролазами, так как они активны в кислой среде. Значение рН=5, оптимальное для работы ферментов, создаётся протонным насосом, который, используя энергию АТФ, накачивает ионы водорода в лизосомы. Катаболизм сфингомиелинов и гликолипидов происходит в лизосомах. В распаде сфингомиелинов участвуют 2 фермента - сфингомиелиназа, отщепляющая фосфорилхолин, и церамидаза, продуктами действия которой являются сфингозин и жирная кислота