Материал: Курс занятий. Липиды
Какова же дальнейшая судьба глицерина и жирных кислот, полученных в результате расщепления жира ?
Глицерин включается в процесс глюконеогенеза (получение глюкозы из неуглеводных соединений ). Это т.н. «глюконеогенез из жира».
Жирные кислоты с током крови попадают в органы и ткани, где подвергаются окислению. Около 30% жирных кислот задерживается в печени уже при однократном прохождении через нее крови. Некоторое количество жирных кислот, не использованных для синтеза триглицеридов, окисляется в печени до кетоновых тел, которые, не подвергаясь дальнейшим превращениям в печени, попадают с током крови в другие органы и ткани (мышцы, сердце и др.), где окисляются до СО2 и Н2О. Т.о. жирные кислоты и кетоновые тела являются энергетическим субстратом. Небольшая часть мобилизованных жирных кислот используется в различных тканях для получения холестерина и других соединений.
Увеличение концентрации глюкозы в жировой ткани и повышение скорости гликолиза угнетают липолиз. Повышение концентрации глюкозы в крови стимулирует секрецию инсулина, что также приводит к угнетению липолиза. Т.о., когда в организм поступает достаточное количество углеводов и скорость их расщепления высока, мобилизация жирных кислот и их окисление идут с пониженной скоростью. Как только запасы углеводов истощаются, и снижается интенсивность гликолиза, происходит усиление липолиза, в результате чего ткани получают повышенные количества жирных кислот для окисления. Вместе с тем повышение содержания жирных кислот в крови вызывает понижение интенсивности утилизации и окисления глюкозы, например, в мышцах. Все это свидетельствует о том, что жировой и углеводный обмены, являющиеся главными энергообразующими процессами в организме, настолько тесно связаны друг с другом, что многие факторы, влияющие на один вид обмена, прямо или косвенно сказываются на другом. И опять в этих процессах явно просматривается руководящая роль инсулина. С Одной стороны инсулин способствует депонированию жиров, с другой стороны глюкагон (с помощью адреналина) способствует мобилизации депонированных жиров, включая их в процесс глюконеогенеза и кетогенеза.
Регуляция процессов мобилизации и резервирования нейтрального жира, , физиологическое значение процессов. Нарушение при ожирении.
Мобилизация депонированных жиров стимулируется глюкагоном и адреналином и, в меньшей степени, некоторыми другими гормонами (соматотропным, кортизолом). В постабсорбтивный период и при голодании глюкагон, действуя на адипоциты через аденилатциклазную систему, активирует протеинкиназу А, которая фосфорилирует и, таким образом, активирует гормончувствительную липазу, что инициирует липолиз и выделение жирных кислот и глицерина в кровь. При физической активности увеличивается секреция адреналина, который действует через β-адренергические рецепторы адипоцитов, активирующие аденилатциклазную систему
Р оль адреналина и глюкагона
Инсулин активирует депонирование нейтрального жира
Глюкагон и адреналин усиливают мобилизацию за счёт активации ТАГ-липазы (триацилглицеридлипазы)
В абсорбтивный период при увеличении соотношения инсулин/ глюкагон в печени активируется синтез жиров. В жировой ткани индуцируется синтез ЛП-липа-зы в адипоцитах и осуществляется её экспонирование на поверхность эндотелия; следовательно, в этот период увеличивается поступление жирных кислот в адипоциты. Одновременно инсулин активирует белки-переносчики глюкозы -ГЛЮТ-4.
Поступление глюкозы в адипоциты и гликолиз также активируются. В результате образуются все необходимые компоненты для синтеза жиров: глицерол-3-фосфат и активные формы жирных кислот. В печени инсулин, действуя через различные механизмы, активирует ферменты путём дефосфорилирования и индуцирует их синтез. В результате увеличиваются активность и синтез ферментов, участвующих в превращении части глюкозы, поступающей с пищей, в жиры. Это - регуляторные ферменты гликолиза, пируватдегидрогеназный комплекс и ферменты, участвующие в синтезе жирных кислот из ацетил-КоА. Результат действия инсулина на обмен углеводов и жиров в печени - увеличение синтеза жиров и секреция их в кровь в составе ЛПОНП. ЛПОНП доставляют жиры в капилляры жировой ткани, где действие ЛП-ли-пазы обеспечивает быстрое поступление жирных кислот в адипоциты, где они депонируются в составе триацилглицеринов.
Нарушения при ожирении.
Резистентность к инсулину.
Ожирение связано со снижением способности инсулина стимулировать элиминацию периферической глюкозы и подавлять выброс глюкозы печенью. С целью компенсации организм затем увеличивает секрецию глюкозы. Эта резистентность к инсулину и гиперинсулинемия могут быть вызваны поступлением свободных жирных кислот к печени из жировой ткани в брюшной полости. Возможно, поэтому абдоминальное ожирение связано с большим числом метаболических осложнений.
Нарушение обмена липидов.
Содержание триглицеридов в плазме часто повышено у людей, страдающих ожирением. Это приводит к снижению количества холестерина-ЛВП вследствие усиления катаболизма ЛВП. Концентрация холестерина-ЛИП также может быть повышена.
Изменения уровня половых гормонов.
Обследование мужчин с ожирением свидетельствует о снижении содержания тестостерона и фолликулостимулирующего гормона (ФСГ).
Липопротеины как транспортная форма липидов. Типы, состав и строение липопротеинов крови, взаимопревращения липопротеинов.
Все типы липопротеинов имеют сходное строение - гидрофобное ядро и гидрофильный слой на поверхности. Гидрофильный слой образован белками, которые называют апопротеинами, и амфифильными молекулами липидов - фосфолипидами и холестеролом. Гидрофильные группы этих молекул обращены к водной фазе, а гидрофобные части - к гидрофобному ядру липопротеина, в котором находятся транспортируемые липиды. Некоторые апопротеины интегральные и не могут быть отделены от липопротеина, а другие могут свободно переноситься от одного типа липопротеина к другому. Апопротеины выполняют несколько функций
• формируют структуру липопротеинов;
• взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов;
• служат ферментами или активаторами ферментов, действующих на липопротеины.
Ч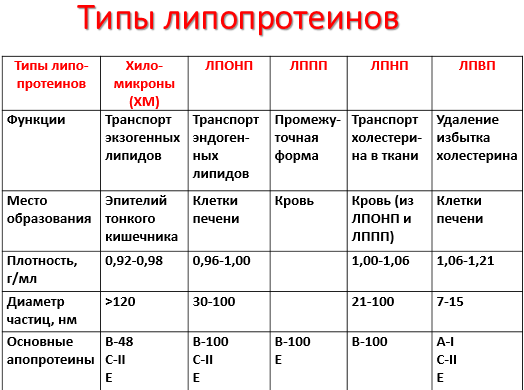 ем
ниже плотность липопротеинов, из-за
меньшей концентрации липопротеинов,
тем опасней для организма, т.к. они
способствуют образованию атеросклеротических
бляшке.
ем
ниже плотность липопротеинов, из-за
меньшей концентрации липопротеинов,
тем опасней для организма, т.к. они
способствуют образованию атеросклеротических
бляшке.
В результате действия ЛП-липазы на жиры ХМ образуются жирные кислоты и глицерол. Основная масса жирных кислот проникает в ткани. В жировой ткани в абсорбтивный период жирные кислоты депонируются в виде триацилглицеролов, в сердечной мышце и работающих скелетных мышцах используются как источник энергии. Другой продукт гидролиза жиров, глицерол, растворим в крови, транспортируется в печень, где в абсорбтивный период может быть использован для синтеза жиров.
В результате действия ЛП-липазы на ХМ количество жиров в них снижается на 90%, уменьшаются размеры частиц, апопротеин C-II переносится обратно на ЛПВП. Образовавшиеся частицы называются остаточными ХМ. Они содержат в себе фосфолипиды, холестерол, жирорастворимые витамины и апопротеины В-48 и Е. Остаточные ХМ захватываются гепатоцитами, которые имеют рецепторы, взаимодействующие с этими апопротеинами. Путём эндоцитоза остаточные ХМ попадают внутрь клеток, и ферментами лизосом белки и липиды гидролизуются, а затем утилизируются. Жирорастворимые витамины и экзогенный холестерол используются в печени или транспортируются в другие ткани.
Хиломикроны образуются в стенке кишечника, содержат до 80% ТАГ пищевого происхождения, которые транспортируются кровью в периферические ткани. В кровеносных капиллярах ТАГ подвергаются гидролизу липопротеинлипазой; образующиеся жирные кислоты поступают в ткани, а «остатки» хиломикронов поглощаются клетками печени.
ЛПОНП - образуются в печени, являются транспортной формой эндогенных ТАГ. Как и хиломикроны, являются субстратами липопротеинлипазы эндотелия капилляров. После гидролиза ТАГ, ЛПОНП превращаются в ЛПНП.
ЛПНП - образуются в крови из ЛПОНП под действием липопротеинлипазы. Богаты холестеролом, транспортируют его во внепечёночные ткани. В результате взаимодействия ЛПНП с рецепторами на поверхности мембран холестерол из ЛПНП проникает внутрь клеток, где участвует в образовании клеточных структур и реакциях биосинтеза веществ .
ЛПВП – образуются в печени, первоначально состоят преимущественно из белков и фосфолипидов и имеют форму дисков. При помощи фермента ЛХАТ липопротеины этого класса извлекают избыток холестерола из внепечёночных клеток и в форме эфиров доставляют его в печень.
Увеличение содержания в крови ЛПНП и ЛПОНП и уменьшение содержания ЛПВП способствует развитию атеросклероза. Следовательно, ЛПОНП и ЛПНП – атерогенные липопротеины, ЛПВП –антиатерогенные липопротеины.
Катаболизм липидов, биологическое значение.
Отложившиеся в жировых депо липиды по мере надобности могут вновь переходить в плазму крови(так называемая мобилизация жира), после чего они используются тканями в качестве энергетического или пластического (строительного) материала. Главным эндогенным источником липидов, используемых в качестве метаболического«топлива» служит резервный жир (в основном – триацилглицерины), содержащийся в цитоплазме клеток в форме капелек. Другой источник – фосфатиды мембран, подвергающиеся непрерывному обновлению.
Первым этапом использования жира в тканях в качестве энергетического материала является его расщепление с образованием глицерина и высших жирных кислот. Процесс этот катализируется тканевыми липазами. Различают несколько липаз, из которых триглицеридлипаза является гормонозависимой, т.е. активизируется гормонами с помощью аденилатциклазной системы (гормон ® аденилатциклаза ® цАМФ ® протеинкиназа ® фосфорилированная триглицеридлипаза). Фосфорилированная (активная) триглицеридлипаза расщепляет триглицерид на диглицерид и жирную кислоту. Затем под действием ди- и моноглицеридлипаз образуются конечные продукты липолиза - глицерин и жирные кислоты. В дальнейшем глицерин и жирные кислоты окисляются в тканях до СО2 и Н2О. Освобождающаяся при этом химическая энергия частью накапливается в ангидридных фосфатных связях АТФ, а частью переходит в теплоту.
Глицерин независимо от того поступит ли он на ресинтез жиров или будет претерпевать дальнейший распад, прежде всего фосфорилируется. Донором остатка фосфорной кислоты в этой реакции служит АТФ. Процесс ускоряется соответствующей фосфотрансферазой, получившей название глицерокиназы.
Фосфоглицерин (глицерофосфат) окисляется в тканях в фосфоглицериновый альдегид через фосфодиоксиацетон. Последний вступает в обменные реакции, рассмотренные ранее при изучении обмена углеводов: фосфоглицериновый альдегид – 1,3-дифосфоглицериновая кислота – 3-фосфоглицериновая кислота – 2-фосфоглицериновая кислота – фосфоенолпировиноградная кислота – пировиноградная кислота.
Пировиноградная кислота путем окислительного декарбоксилирования переходит в ацетил-КоА, который вовлекается в лимоннокислый цикл, сопряженный с цепью дыхательных ферментов, и окисляется до СО и Н О. Приокислении глицерина до СО2 и Н2О возникает вначале при окислении фосфоглицеринового альдегида три молекулы АТФ, одна молекула АТФ синтезируется при окислении 1,3-дифосфоглицериновой кислоты и одна молекула АТФ образуется при окислении 2-фосфоенолпировиноградной кислоты, наконец, 15 молекул АТФ образуется при окислении пировиноградной кислоты в лимоннокислом цикле. Таким образом, принимая во внимание, что одна молекула АТФ затрачивается на фосфорилирование глицерина, за счет окисления глицерина (при условии, что все атомы водорода, снятые дегидрогеназами, идут в дыхательную цепь ферментов, функционирующую сопряжено с окислительным фосфорилированием) образуется 19 молекул АТФ.
Β-ОКИСЛЕНИЕ ЖИРНЫХ КИСЛОТ. ХИМИЗМ, ФЕРМЕНТЫ, ЭНЕРГЕТИКА, БИОЛОГИЧЕСКАЯ РОЛЬ.
β-Окисление жирных кислот - специфический путь катаболизма жирных кислот, протекающий в матриксе митохондрий только в аэробных условиях и заканчивающийся образованием ацетил-КоА. Водород из реакций β-окисления поступает в ЦПЭ, а ацетил-КоА окисляется в цитратном цикле, также поставляющем водород для ЦПЭ. Поэтому β-окисление жирных кислот - важнейший метаболический путь, обеспечивающий синтез АТФ в дыхательной цепи.β-Окисление - специфический путь катаболизма жирных кислот, при котором от карбоксильного конца жирной кислоты последовательно отделяется по 2 атома углерода в виде ацетил-КоА. Метаболический путь - β-окисление - назван так потому, что реакции окисления жирной кислоты происходят у β-углеродного атома. Реакции β-окисления и последующего окисления ацетил-КоА в ЦТК служат одним из основных источников энергии для синтеза АТФ по механизму окислительного фосфорилирования. β-Окисление жирных кислот происходит только в аэробных условиях.
Активация жирных кислот. Перед тем, как вступить в различные реакции, жирные кислоты должны быть активированы, т.е. связаны макроэргической связью с коферментом А:
R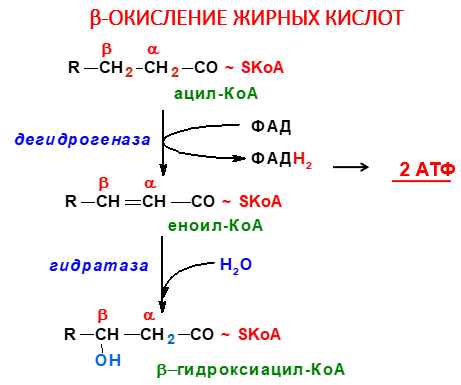 COOH
+ HSKoA + АТФ → RCO ~ КоА + АМФ + PPi.
COOH
+ HSKoA + АТФ → RCO ~ КоА + АМФ + PPi.
Р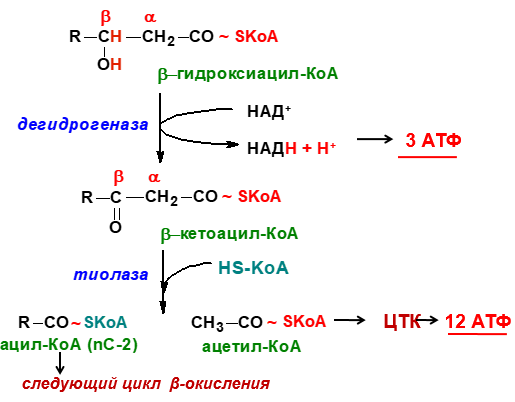 еакцию
катализирует фермент ацил-КоА син-тетаза.
Выделившийся в ходе реакции пирофосфат
гидролизуется ферментом пирофосфатазой:
Н4Р2О7 + Н2О → 2 Н3РО4. Выделение энергии
при гидролизе макроэргической связи
пирофосфата смещает равновесие реакции
вправо и обеспечивает полноту протекания
реакции активации. Ацил-КоА синтетазы
находятся как в цитозоле, так и в матриксе
митохондрий. Эти ферменты отличаются
по специфичности к жирным кислотам с
различной длиной углеводородной цепи.
Жирные кислоты с короткой и средней
длиной цепи (от 4 до 12 атомов углерода)
могут проникать в матрикс митохондрий
путём диффузии. Активация этих жирных
кислот происходит в матриксе митохондрий.
Жирные кислоты с длинной цепью, которые
преобладают в организме человека (от
12 до 20 атомов углерода), активируются
ацил-КоА синтетазами, расположенными
на внешней мембране митохондрий.
еакцию
катализирует фермент ацил-КоА син-тетаза.
Выделившийся в ходе реакции пирофосфат
гидролизуется ферментом пирофосфатазой:
Н4Р2О7 + Н2О → 2 Н3РО4. Выделение энергии
при гидролизе макроэргической связи
пирофосфата смещает равновесие реакции
вправо и обеспечивает полноту протекания
реакции активации. Ацил-КоА синтетазы
находятся как в цитозоле, так и в матриксе
митохондрий. Эти ферменты отличаются
по специфичности к жирным кислотам с
различной длиной углеводородной цепи.
Жирные кислоты с короткой и средней
длиной цепи (от 4 до 12 атомов углерода)
могут проникать в матрикс митохондрий
путём диффузии. Активация этих жирных
кислот происходит в матриксе митохондрий.
Жирные кислоты с длинной цепью, которые
преобладают в организме человека (от
12 до 20 атомов углерода), активируются
ацил-КоА синтетазами, расположенными
на внешней мембране митохондрий.
Т ранспорт
жирных кислот с длинной углеводородной
цепью в митохондриях. β-Окисление жирных
кислот, происходит в матриксе митохондрий,
поэтому после активации жирные кислоты
должны транспортироваться внутрь
митохондрий. Жирные кислоты с длинной
углеводородной цепью переносятся через
плотную внутреннюю мембрану митохондрий
с помощью карнитина. Карнитин поступает
с пищей или синтезируется из незаменимых
аминокислот лизина и метионина. В
реакциях синтеза карнитина участвует
витамин С (аскорбиновая кислота). В
наружной мембране митохондрий находится
фермент карнитинацилтрансфераза I
(карнитин-пальмитоилтрансфераза I),
катализирующий реакцию с образованием
ацилкарнитина. Образовавшийся ацилкарнитин
проходит через межмембранное пространство
к наружной стороне внутренней мембраны
и транспортируется с помощью
карнитинацилкарнитинтранс-локазы на
внутреннюю поверхность внутренней
мембраны митохондрий, где фермент
карнитинацилтрансфераза II катализирует
перенос ацила на внутримитохондриальный
КоА.
ранспорт
жирных кислот с длинной углеводородной
цепью в митохондриях. β-Окисление жирных
кислот, происходит в матриксе митохондрий,
поэтому после активации жирные кислоты
должны транспортироваться внутрь
митохондрий. Жирные кислоты с длинной
углеводородной цепью переносятся через
плотную внутреннюю мембрану митохондрий
с помощью карнитина. Карнитин поступает
с пищей или синтезируется из незаменимых
аминокислот лизина и метионина. В
реакциях синтеза карнитина участвует
витамин С (аскорбиновая кислота). В
наружной мембране митохондрий находится
фермент карнитинацилтрансфераза I
(карнитин-пальмитоилтрансфераза I),
катализирующий реакцию с образованием
ацилкарнитина. Образовавшийся ацилкарнитин
проходит через межмембранное пространство
к наружной стороне внутренней мембраны
и транспортируется с помощью
карнитинацилкарнитинтранс-локазы на
внутреннюю поверхность внутренней
мембраны митохондрий, где фермент
карнитинацилтрансфераза II катализирует
перенос ацила на внутримитохондриальный
КоА.