Материал: Курс занятий. Липиды
Биосинтез жирных кислот, химизм, ферменты.
Основные источники водорода для синтеза жирных кислот
В каждом цикле биосинтеза пальмитиновой кислоты проходят 2 реакции восстановления, донором водорода в которых служит кофермент NADPH. Восстановление NADP+ происходит в реакциях:
• дегидрирования в окислительных стадиях пентозофосфатного пути катаболизма глюкозы;
• дегидрирования малата малик-ферментом;
• дегидрирования изоцитрата цитозольной NADP-зависимой дегидрогеназой.
Синтез жирных кислот протекает в цитоплазме клетки. В митохондриях в основном происходит удлинение существующих цепей жирных кислот. Установлено, что в цитоплазме печеночных клеток синтезируется пальмитиновая кислота (16 углеродных атомов), а в митохондриях этих клеток из уже синтезированной в цитоплазме клетки пальмитиновой кислоты или из жирных кислот экзогенного происхождения, т.е. поступающих из кишечника, образуются жирные кислоты, содержащие 18, 20 и 22 углеродных атома.
Б иосинтез
жирных кислот протекает с участием
НАДФН, АТФ, Мn2+ и НСО3 – (в качестве
источника СО2); субстратом является
ацетил-КоА, конечным продуктом –
пальмитиновая кислота.
иосинтез
жирных кислот протекает с участием
НАДФН, АТФ, Мn2+ и НСО3 – (в качестве
источника СО2); субстратом является
ацетил-КоА, конечным продуктом –
пальмитиновая кислота.
Происходит образование малонил апю, а затем начинается "нанизывание" атомов углерода на цепь, пока не получится пальмитиновая, либо другая жирная кислота.
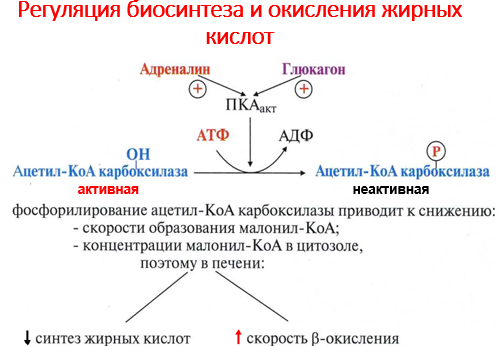
Регуляция биосинтеза и окисления жирных кислот
Глюкагон и адреналин:
увеличивают скорость β-окисления,
снижают скорость синтеза жирных кислот
Инсулин:
снижает скорость β-окисления,
увеличивает скорость синтеза жирных кислот
Биосинтез жирных кислот с длинной цепью углеродных атомов и непредельных.
В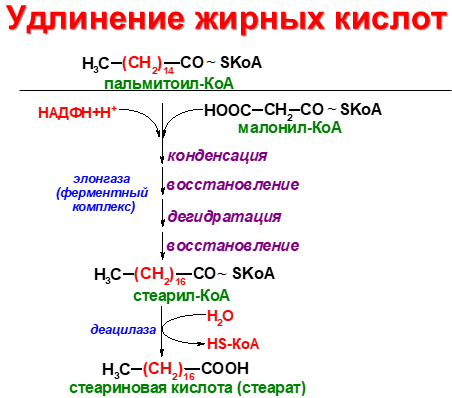 настоящее время показано, что в микросомах
клеток млекопитающих образование
двойных связей может происходить только
на участке цепи жирной кислоты от 9-го
до 1-го углеродных атомов, ибо в микросомах
отсутствуют десатуразы, которые могли
бы катализировать образование двойных
связей в цепи далее 9-го углеродного
атома. У животных двойные связи могут
образовываться в Δ4-, Δ5-, Δ6- и Δ9-положении,
но не далее Δ9-положения, в то время как
у растений – в Δ6-, Δ9-, Δ12 и Δ15-положении.
Поэтому в организме млекопитающих, в
том числе и человека, не могут
настоящее время показано, что в микросомах
клеток млекопитающих образование
двойных связей может происходить только
на участке цепи жирной кислоты от 9-го
до 1-го углеродных атомов, ибо в микросомах
отсутствуют десатуразы, которые могли
бы катализировать образование двойных
связей в цепи далее 9-го углеродного
атома. У животных двойные связи могут
образовываться в Δ4-, Δ5-, Δ6- и Δ9-положении,
но не далее Δ9-положения, в то время как
у растений – в Δ6-, Δ9-, Δ12 и Δ15-положении.
Поэтому в организме млекопитающих, в
том числе и человека, не могут
образовываться, например, из стеариновой кислоты (18:0) линолевая (18:2; 9,12) и линоленовая (18:3; 9,12,15) кислоты. Эти кислоты относятся к категории незаменимых жирных кислот. К незаменимым жирным кислотам обычно относят также арахидоновую кислоту (20:4; 5,8,11,14).
Полиненасыщенными жирными кислотами принято называть одноосновные жирные кислоты, в структуре которых присутствуют две и более двойных связей между атомами углерода.
К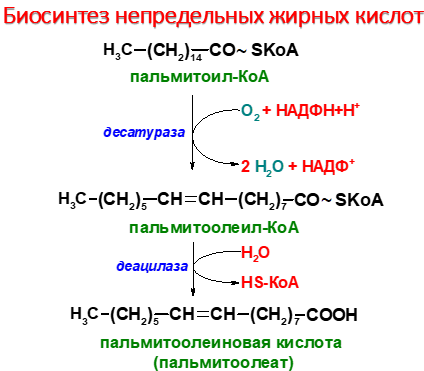 полиненасыщенным жирным кислотам
относятся в числе прочих и незаменимые
жирные кислоты или эссенциальные
жирные кислоты,
получившие название витамина F, такие
как линолевая (две
двойные связи, положение первой –
омега-6, то есть при шестом атоме углерода,
отсчитывая от метильного конца)
и линоленовая(три
двойные связи, положение первой –
омега-3, т. е. при третьем атоме
углерода),эйкозапентаеновая (шесть
двойных связей, положение первой –
omega-3) идокозагексаеновая (пять
двойных связей, положение первой –
омега-3) кислоты.
полиненасыщенным жирным кислотам
относятся в числе прочих и незаменимые
жирные кислоты или эссенциальные
жирные кислоты,
получившие название витамина F, такие
как линолевая (две
двойные связи, положение первой –
омега-6, то есть при шестом атоме углерода,
отсчитывая от метильного конца)
и линоленовая(три
двойные связи, положение первой –
омега-3, т. е. при третьем атоме
углерода),эйкозапентаеновая (шесть
двойных связей, положение первой –
omega-3) идокозагексаеновая (пять
двойных связей, положение первой –
омега-3) кислоты.
Кетоновые тела, биосинтез и использование, физиологическое значение процессов.
Б
 иологическая
роль кетоновых тел– являются
альтернативным глюкозе источником
энергии (особенно для мышечной ткани,
особенно при голодании и сахарном
диабете)
иологическая
роль кетоновых тел– являются
альтернативным глюкозе источником
энергии (особенно для мышечной ткани,
особенно при голодании и сахарном
диабете)
П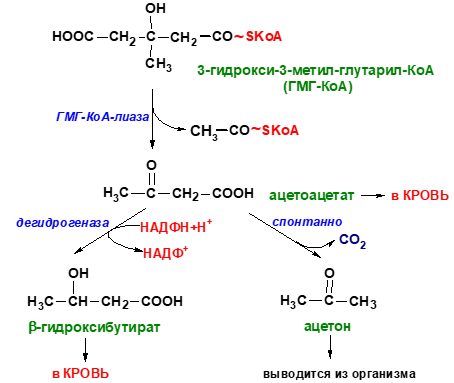 ри
голодании, длительной физической работе
и в случаях, когда клетки не получают
достаточного количества глюкозы, жирные
кислоты используются многими тканями
как основной источник энергии. В отличие
от других тканей мозг и другие отделы
нервной ткани практически не используют
жирные кислоты в качестве источника
энергии. В печени часть жирных кислот
превращается в кетоновые тела, которые
окисляются мозгом, нервной тканью,
мышцами, обеспечивая достаточное
количество энергии для синтеза АТФ и
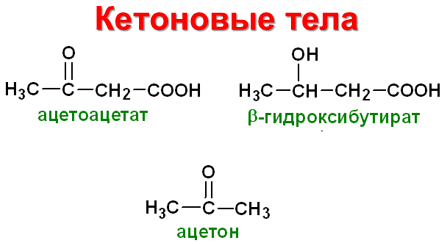
уменьшая потребление глюкозы. К кетоновым
телам
относят β-гидроксибутират,
ацетоацетат
и
ацетон.
Первые две молекулы могут окисляться
в тканях, обеспечивая синтез АТФ. Ацетон
образуется только при высоких концентрациях
кетоновых тел в крови и, выделяясь с
мочой, выдыхаемым воздухом и потом,
позволяет организму избавляться от
избытка кетоновых тел.
ри
голодании, длительной физической работе
и в случаях, когда клетки не получают
достаточного количества глюкозы, жирные
кислоты используются многими тканями
как основной источник энергии. В отличие
от других тканей мозг и другие отделы
нервной ткани практически не используют
жирные кислоты в качестве источника
энергии. В печени часть жирных кислот
превращается в кетоновые тела, которые
окисляются мозгом, нервной тканью,
мышцами, обеспечивая достаточное
количество энергии для синтеза АТФ и
уменьшая потребление глюкозы. К кетоновым
телам
относят β-гидроксибутират,
ацетоацетат
и
ацетон.
Первые две молекулы могут окисляться
в тканях, обеспечивая синтез АТФ. Ацетон
образуется только при высоких концентрациях
кетоновых тел в крови и, выделяясь с
мочой, выдыхаемым воздухом и потом,
позволяет организму избавляться от
избытка кетоновых тел.
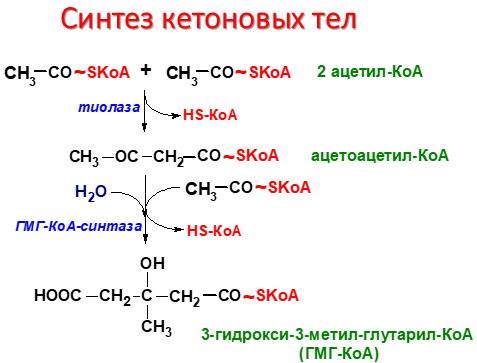
Синтез кетоновых тел в печени. При низком соотношении инсулин/глюкагон в крови в жировой ткани активируется распад жиров. Жирные кислоты поступают в печень в большем количестве, чем в норме, поэтому увеличивается скорость β-окисления. Скорость реакций ЦТК в этих условиях снижена, так как оксалоацетат используется для глюконеогенеза. В результате скорость образования ацетил-КоА превышает способность ЦТК окислять его. Ацетил-КоА накапливается в митохондриях печени и используется для синтеза кетоновых тел. Синтез кетоновых тел происходит только в митохондриях печени. Синтез кетоновых тел начинается с взаимодействия двух молекул ацетил-КоА, которые под действием фермента тиолазы образуют ацетоацетил-КоА. С ацетоацетил-КоА взаимодействует третья молекула ацетил-КоА, образуя 3-гидрокси-3-метилглутарил-КоА (ГМГ-КоА). Эту реакцию катализирует фермент ГМГ-КоА-синтаза. Далее ГМГ-КоА-лиаза катализирует расщепление ГМГ-КоА на свободный ацетоацетат и ацетил-КоА. Ацетоацетат может выделяться в кровь или превращаться в печени в другое кетоновое тело - β-гидроксибутират путём восстановления. В клетках печени при активном β-окислении создаётся высокая концентрация NADH. Это способствует превращению большей части ацетоацетата в β-гидроксибутират, поэтому основное кетоновое тело в крови - именно β-гидроксибутират. При голодании для многих тканей жирные кислоты и кетоновые тела становятся основными топливными молекулами. Глюкоза используется в первую очередь нервной тканью и эритроцитами. При высокой концентрации ацетоацетата часть его неферментативно декарбоксилируется, превращаясь в ацетон. Ацетон не утилизируется тканями, но выделяется с выдыхаемым воздухом и мочой. Таким путём организм удаляет избыточное количество кетоновых тел, которые не успевают окисляться, но, являясь водорастворимыми кислотами, вызывают ацидоз. При длительном голодании кетоновые тела становятся основным источником энергии для скелетных мышц, сердца и почек. Таким образом глюкоза сохраняется для окисления в мозге и эритроцитах. Через 2-3 дня после начала голодания концентрация кетоновых тел в крови достаточна для того, чтобы они проходили в клетки мозга и окислялись, снижая его потребности в глюкозе. β-Гидроксибутират, попадая в клетки, дегидрируется NAD-зависимой дегидрогеназой и превращается в ацетоацетат. Ацетоацетат активируется, взаимодействуя с сукцинил-КоА–донором КоА:
А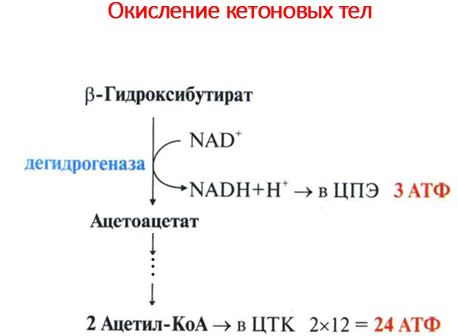 цетоацетат
+ Сукцинил-КоА → Ацетоацетил- КоА +
Сукцинат.
цетоацетат
+ Сукцинил-КоА → Ацетоацетил- КоА +
Сукцинат.
Реакцию катализирует сукцинил-КоА-ацето-ацетат-КоА-трансфераза. Этот фермент не синтезируется в печени, поэтому печень не использует кетоновые тела как источники энергии, а производит их "на экспорт". Кетоновые тела - хорошие топливные молекулы; окисление одной молекулы β-гидроксибутирата до СО2 и Н2О обеспечивает синтез 27 молекул АТФ. Эквивалент одной макроэргической связи АТФ (в молекуле сукцинил-КоА) используется на активацию ацетоацетата, поэтому суммарный выход АТФ при окислении одной молекулы β-гидроксибутирата - 26 молекул.
Диагностическое значение: Кетоновые тела (ацетон, β-гидрокси-маслянная и ацетоуксусная кислоты) являются нормальными метаболитами липидного обмена. Они образуются в печени и отправляются током крови в мышцы, где подвергаются дальнейшему окислению. Содержание их в крови в норме колеблется до 30 мг/л. При сахарном диабете, голодании содержание кетоновых тел резко возрастает (кетонемия), как следствие, они появляются в моче (кетонурия).
Сахарный диабет — заболевание, развивающееся вследствие абсолютной или относительной недостаточности инсулина, что приводит к нарушению утилизации углеводов, расстройствам липидного и белкового обменов, проявляется гипергликемией и поражением сосудов. Выделяют инсулинзависимый сахарный диабет (ИЗСД), диабет I типа, и инсулиннезависимый (ИНСД) или диабет II типа.
Биосинтез фосфолипидов в тканях, химизм, физиологическое значение.
Синтез фосфолипидов может происходить в различных тканях и по нескольким путям: в кишечнике с использованием пищевого холина или этаноламина (ресинтез фосфолипидов) и в печени (собственно биосинтез)
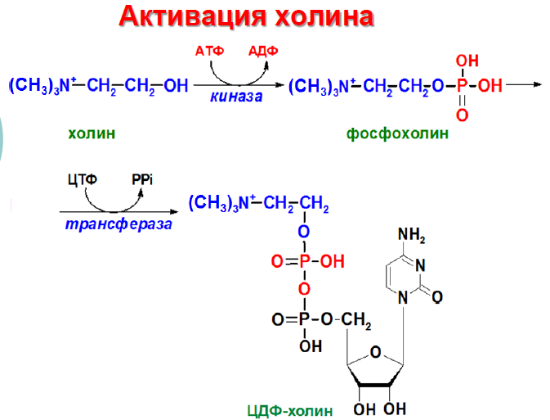
С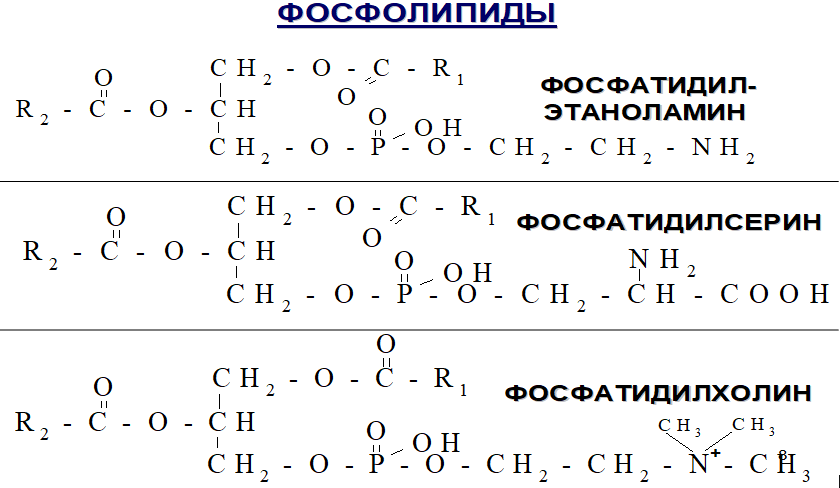 интез
фосфатидилхолинов, фосфатидилэтаноламинов
и фосфатидилсеринов.
Начальные
этапы синтеза глицерофосфолипидов и
жиров происходят одинаково до образования
фосфатидной кислоты. Фосфатидная кислота
может синтезироваться двумя разными
путями: через глицеральдегид-3-фосфат
и через дигидроксиацетонфосфат
интез
фосфатидилхолинов, фосфатидилэтаноламинов
и фосфатидилсеринов.
Начальные
этапы синтеза глицерофосфолипидов и
жиров происходят одинаково до образования
фосфатидной кислоты. Фосфатидная кислота
может синтезироваться двумя разными
путями: через глицеральдегид-3-фосфат
и через дигидроксиацетонфосфат
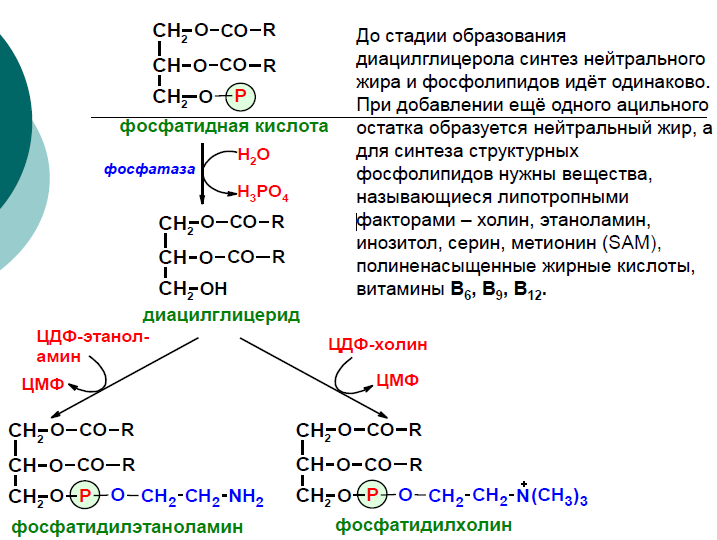
Н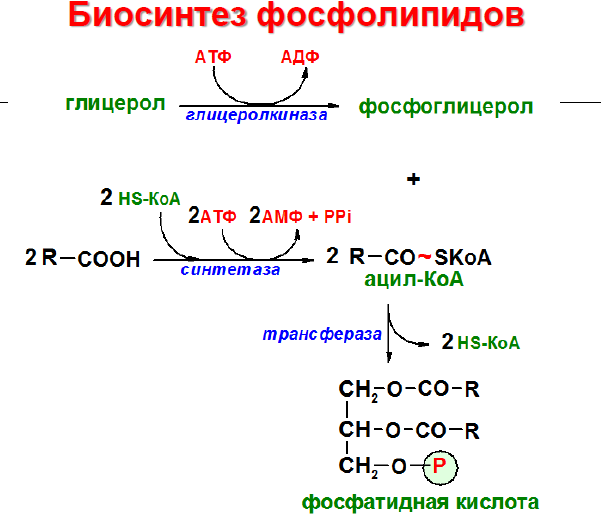 а
следующем этапе фосфатидаза отщепляет
от фосфатидной кислоты фосфатный
остаток, в результате чего образуется
диацилглицерол. Дальнейшие превращения
диацилглицерола также могут идти разными
путями. Один из вариантов - образование
активной формы "полярной головки"
фосфолипида: холин, серии или этаноламин
превращаются в ЦДФ-холин, ЦДФ-серин или
ЦДФ-этаноламин. Далее диацилглицерол
взаимодействует с ЦМФ-производными,
при этом выделяется ЦМФ, и образуется
соответствующий фосфолигид, например,
фосфатидилхолин. Между глицерофосфолипидами
возможны различные взаимопревращения.
Фосфатидилхолин может образовываться
и другим путём: из фосфатидилэтаноламина,
получая последовательно 3 метальные
группы от SAM. Фосфатидилсерин может
превращаться в фосфатидилэтаноламин
путём декарбоксилирования.
Фосфатидилэтаноламин может превращаться
в фосфатидилсерин путём обмена этаноламина
на серии.
а
следующем этапе фосфатидаза отщепляет
от фосфатидной кислоты фосфатный
остаток, в результате чего образуется
диацилглицерол. Дальнейшие превращения
диацилглицерола также могут идти разными
путями. Один из вариантов - образование
активной формы "полярной головки"
фосфолипида: холин, серии или этаноламин
превращаются в ЦДФ-холин, ЦДФ-серин или
ЦДФ-этаноламин. Далее диацилглицерол
взаимодействует с ЦМФ-производными,
при этом выделяется ЦМФ, и образуется
соответствующий фосфолигид, например,
фосфатидилхолин. Между глицерофосфолипидами
возможны различные взаимопревращения.
Фосфатидилхолин может образовываться
и другим путём: из фосфатидилэтаноламина,
получая последовательно 3 метальные
группы от SAM. Фосфатидилсерин может
превращаться в фосфатидилэтаноламин
путём декарбоксилирования.
Фосфатидилэтаноламин может превращаться
в фосфатидилсерин путём обмена этаноламина
на серии.
Б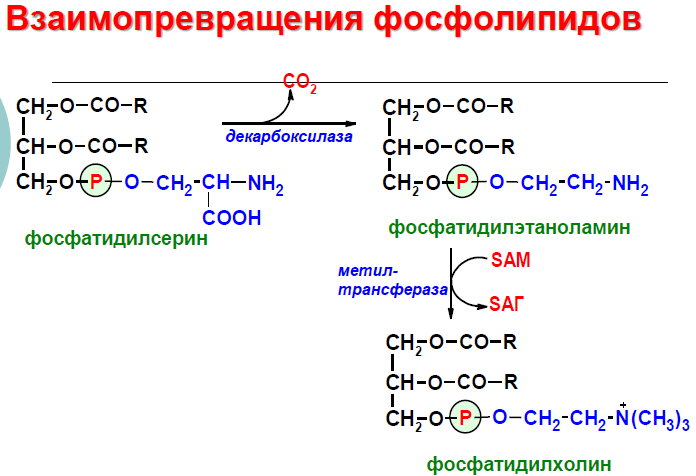 иологическая
роль.
иологическая
роль.
Входят в состав мембран, участвуя в их избирательной проницаемости.
Дипальмитоилфосфатидилхолин (до 80%), является компонентом сурфактанта, выстилающего альвеолы легких и препятствующей слипанию стенок альвеол во время вдоха.
Фосфатидилэтаноламин и фосфатидилхолин мембран взаимодействует с ферментами, образуя комплексы, которые активируют факторы свертывания крови. Фосфатидилсерин активирует процессы фибринолиза, связываясь с другими ферментами.
Обладают липотропным действием, препятствуя отложению нейтрального жира в печени.
Продукты их распада участвуют в патогенезе бронхиальной астмы, атеросклероза.
Фосфатидилсерин влияет на освобождение гистамина.
Холестерин, строение, биосинтез, судьба в организме.
Х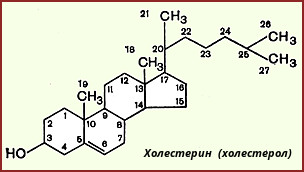
 олестерол
- стероид, характерный только для животных
организмов. Он синтезируется во многих
тканях человека, но основное место
синтеза - печень. В печени синтезируется
более 50% холестерола, в тонком кишечнике
- 15-20%, остальной холестерол синтезируется
в коже, коре надпочечников, половых
железах. В сутки в организме синтезируется
около 1 г холестерола; с пищей поступает
300-500 мг. Холестерол выполняет много
функций: входит в состав всех мембран
клеток и влияет на их свойства, служит
исходным субстратом в синтезе жёлчных
кислот и стероидных гормонов.
Предшественники в метаболическом пути
синтеза холестерола превращаются также
в убихинон - компонент дыхательной цепи
и долихол, участвующий в синтезе
гликопротеинов.
олестерол
- стероид, характерный только для животных
организмов. Он синтезируется во многих
тканях человека, но основное место
синтеза - печень. В печени синтезируется
более 50% холестерола, в тонком кишечнике
- 15-20%, остальной холестерол синтезируется
в коже, коре надпочечников, половых
железах. В сутки в организме синтезируется
около 1 г холестерола; с пищей поступает
300-500 мг. Холестерол выполняет много
функций: входит в состав всех мембран
клеток и влияет на их свойства, служит
исходным субстратом в синтезе жёлчных
кислот и стероидных гормонов.
Предшественники в метаболическом пути
синтеза холестерола превращаются также
в убихинон - компонент дыхательной цепи
и долихол, участвующий в синтезе
гликопротеинов.