Материал: Курс занятий. Ферменты

Аллостерический центр
6
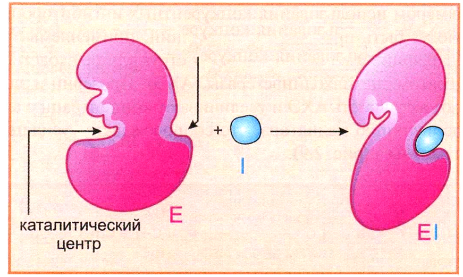 )Аллостерическое
ингибирование.
)Аллостерическое
ингибирование.
-ингибиторы связываются с отдельными участками фермента вне активного центра.
-конформационные изменения в молекуле фермента, которые приводят к уменьшению его активности
Регуляция ферментативной активности.
Возможность регулировать активность ферментов в соответствии с потребностями клетки и целостного организма относится к важнейшим свойствам этих веществ. Ферменты должны работать со строго определѐнной активностью и в строго определѐнных направлениях. В регуляции метаболизма принимают участие несколько факторов.
1. Количество фермента в клетке, которое определяется двумя факторами:
скоростью синтеза; скоростью распада.
(два типа ферментов)
конститутивные (ферменты жизнеобеспечения – энергетического обмена, синтеза нуклеиновых кислот, белков, липидов и т.д.)синтезируются с постоянной скоростью и с постоянной скоростью разрушаются;
индуцибельные (адаптивные) – ферменты, обеспечивающие выполнение специфических функций; синтез этих ферментов возрастает при наличии соответствующих стимулов (индукторов). Например, при беременности и после родов в молочной железе индуцируется синтез ф-та лактозосинтазы под действием лактотропного гормона
2. Доступность фермента и субстрата (например, при отсутствии инсулина глюкоза не может проникнуть в клетки, где находятся ферменты еѐ метаболизма).
3. Регуляция активности самого фермента: компонентами самой клетки (температурой, рН, количеством субстрата, компартментализацией ферментов, наличием транспортных систем, наличием эффекторов);
а
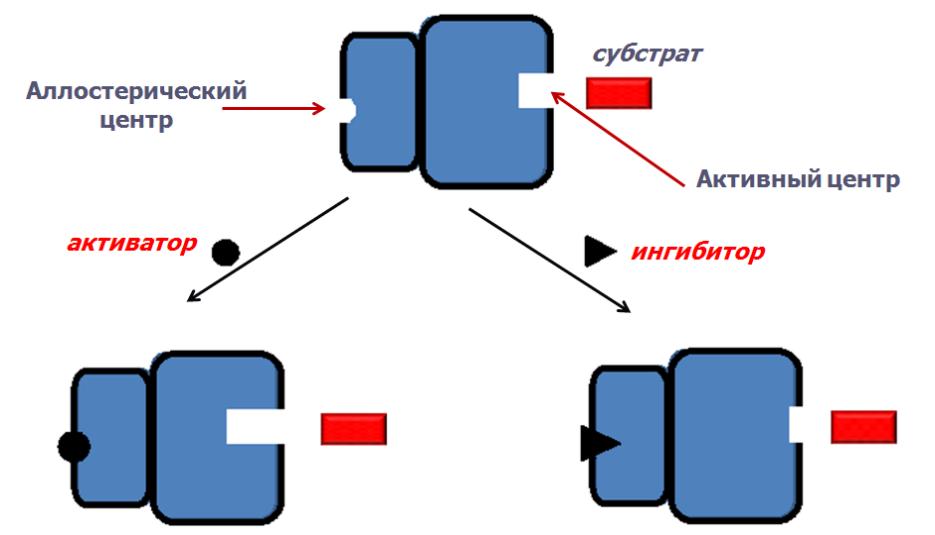 ллостерическая
регуляция;
ллостерическая
регуляция;
-К аллостерическому центру присоединяется не субстрат, а эффектор
-Аллостерические ферменты построены из двух и более субъединиц: одни субъединицы содержат каталитический центр, другие имеют аллостерический центр(регуляторные).
-Присоединение эффектора к аллостерическому центру регуляторной субъединицы изменяет конформацию белка и, соответственно, активность каталитической субъединицы
-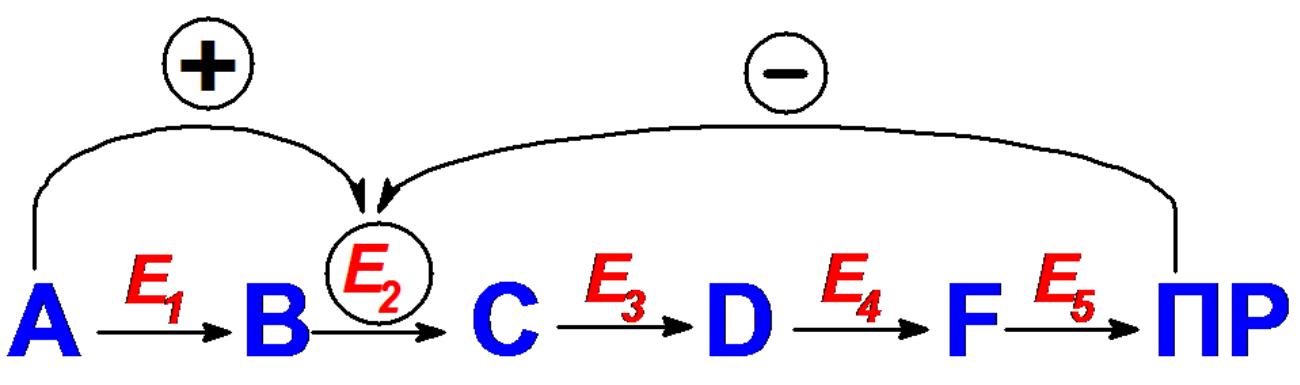 Регуляторы
– исходные вещества и конечные продукты,
а также вещества, участвующие в сопряжѐнных
реакциях, поэтому аллостерическую
регуляцию часто называют саморегуляцией,
Конечные продукты (иногда промежуточные
метаболиты) – ингибиторы, исходные
субстраты – активаторы.
Регуляторы
– исходные вещества и конечные продукты,
а также вещества, участвующие в сопряжѐнных
реакциях, поэтому аллостерическую
регуляцию часто называют саморегуляцией,
Конечные продукты (иногда промежуточные
метаболиты) – ингибиторы, исходные
субстраты – активаторы.
химическая модификация (ковалентная и нековалентная);
Ф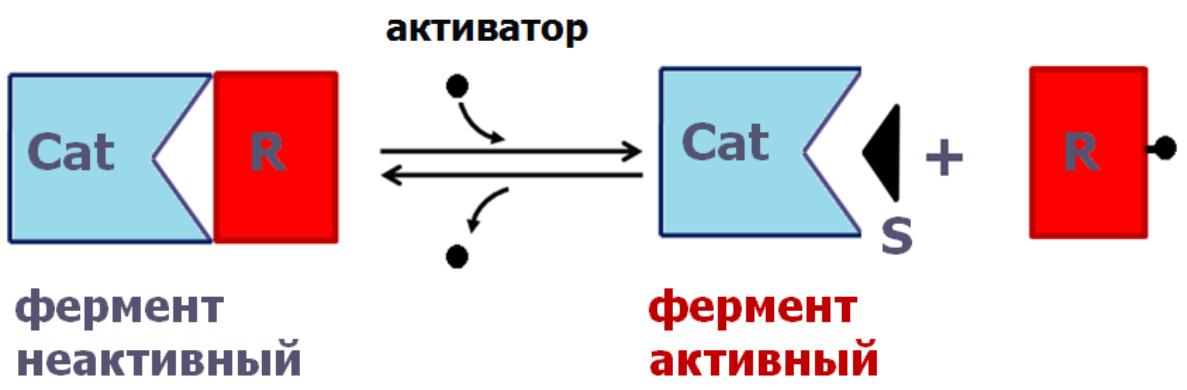
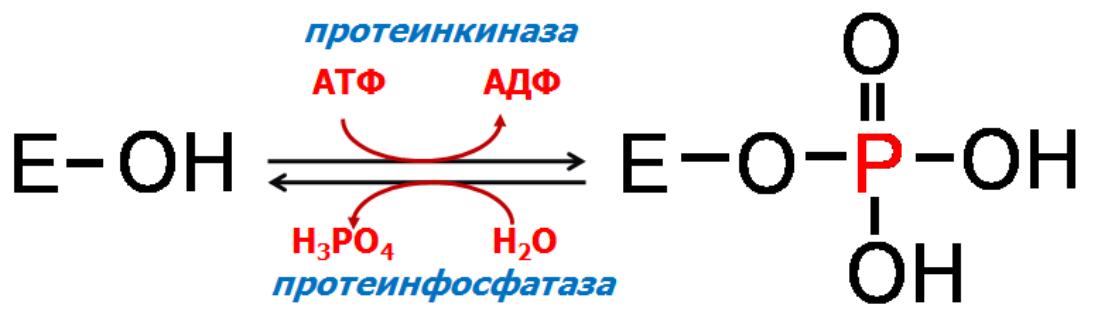 осфорилирование
и дефосфорилирование (ковалентная
модификация) – один из наиболее
распространѐнных способов регуляции
активности ферментов. Такая модификация
заключается в обратимом присоединении
или отщеплении фосфорной кислоты.
Фосфорилирование фермента происходит
по остаткам серина и тирозина. Присоединение
фосфорной кислоты к белку осуществляют
ферменты протеинкиназы,
отщепление – протеинфосфатазы.
осфорилирование
и дефосфорилирование (ковалентная
модификация) – один из наиболее
распространѐнных способов регуляции
активности ферментов. Такая модификация
заключается в обратимом присоединении
или отщеплении фосфорной кислоты.
Фосфорилирование фермента происходит
по остаткам серина и тирозина. Присоединение
фосфорной кислоты к белку осуществляют
ферменты протеинкиназы,
отщепление – протеинфосфатазы.
Ферменты могут быть активны как в фосфорилированном, так и в дефосфорилированном состоянии. Например, при фосфорилировании ферментов, участвующих в обмене гликогена, фермент распада гликогена (гликогенфос-форилаза) находится в активном состоянии, а фермент синтеза гликогена (гликогенсинтаза) – в неактивном. В дефосфорилированном состоянии, наоборот, гликогенфосфорилаза неактивна, а гликогенсинтаза активна. Таким образом противоположно направленные процессы никогда не идут одновременно. Процессы диссоциации-ассоциации и фосфорилирования-дефосфорилирования не происходят спонтанно, а начинаются только при поступлении гормонального сигнала.
частичный протеолиз- отщепление пептида от неактивного предшественника, в результате чего формируется правильная конформация белка-фермента, и он переходит в активное состояние
Кофакторы ферментов: ионы Ме
Алкогольдегидрогеназа, карбоангидраза |
Zn |
Аргиназа, аминопептидаза |
Mn |
Дипептидаза |
Co |
Фосфатаза, фосфокиназа |
Mg |
Тирозиназа |
Cu |
Сукцинатдегидрогеназа |
Fe |
Ксантиноксидаза |
Mo |
Содержание
-глюкозооксидаза используется - содержание глюкозы в крови
-уреаза –определение концентрации мочевины
липаза – липидов
Активность
–измерение скорости превращения субстрата в продукт, т.е. количество превращѐнного субстрата в единицу времени.
Типы единиц
1![]() )Международная
(стандартная) Единица активности – это
количество фермента, которое катализирует
превращение 1 мкмоля субстрата в минуту
в оптимальных условиях:
)Международная
(стандартная) Единица активности – это
количество фермента, которое катализирует
превращение 1 мкмоля субстрата в минуту
в оптимальных условиях:
2)Катал – количество фермента, которое катализирует превращение в оптимальных условиях 1 моля субстрата за одну секунду
![]()
![]()
3)Другие -активность протеиназ - «тирозиновые единицы»
-активность амилазы – в амилокластических
-активность аминотрансфераз – условных
Энзимология
-раздел биохимии, изучающий строение, механизм действия и молекулярную структуру ферментов, нарушение их функционирования, а также выделение, процессы биосинтеза ферментов и их практическое применение
в неѐ входят энзимодиагностика и энзи-мотерапия.
Э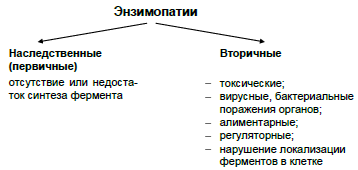 НЗИМОПАТИЯ
(энзимопатология)
– количественное или качественное
нарушение ферментов, сопровождающееся
болезнью. В большинстве случаев - приводят
к снижение количества или активности
ферментов→ нарушение метаболических
процессов.
НЗИМОПАТИЯ
(энзимопатология)
– количественное или качественное
нарушение ферментов, сопровождающееся
болезнью. В большинстве случаев - приводят
к снижение количества или активности
ферментов→ нарушение метаболических
процессов.
П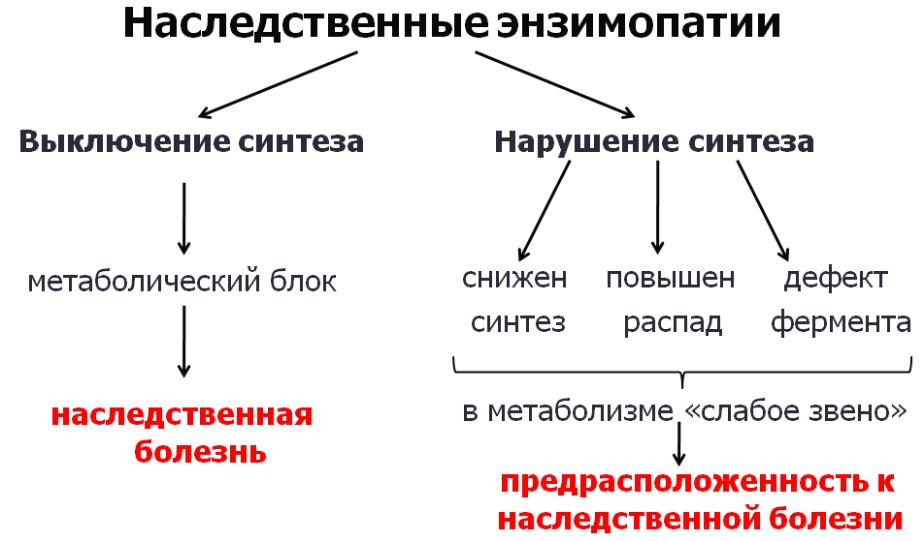 ервичные–
заболевания, связанные с дефектом
генетического аппарата и являющиеся
наследственными Вторичные(приобретенные)
-возникают как следствие заболеваний
органов, вирусных ин-фекций, токсических
воздействий и т.п., что приводит к
нарушению синтеза фермента или условий
его работы, например, гипераммониемия
при заболе-ваниях печени, при которых
ухудшается синтез мочевины и в крови
накапливается аммиак, а при панкреатитах
наблюдается уменьшение секреции
пище-варительных ферментов и ухудшение
пищеварения.
ервичные–
заболевания, связанные с дефектом
генетического аппарата и являющиеся
наследственными Вторичные(приобретенные)
-возникают как следствие заболеваний
органов, вирусных ин-фекций, токсических
воздействий и т.п., что приводит к
нарушению синтеза фермента или условий
его работы, например, гипераммониемия
при заболе-ваниях печени, при которых
ухудшается синтез мочевины и в крови
накапливается аммиак, а при панкреатитах
наблюдается уменьшение секреции
пище-варительных ферментов и ухудшение
пищеварения.
Пр:, ФКУ-фенилкетонурия – наследственная болезнь, связанная с отсут-ствием фенилаланинмонооксигеназы (фенилаланингидроксилазы), галактоземия – отсутствие ферментов метаболизма галактозы.
Вторичные энзимопатии:
-токсические: обусловлены конкурентным или неконкурентным ингибированием ферментов (например, ядами, фосфорорганическими соединениями, боевыми отравляющими веществами и т.д.). Они могут действовать как на стадии биосинтеза фермента, так и блокировать уже готовый фермент.
-алиментарные энзимопатии являются следствием нерационального питания: недостаток витаминов, микроэлементов – причина нехватки кофакторов, недостаток белка – причина нехватки аминокислот для синтеза апофермента.
-регуляторные энзимопатии связаны с нарушением функционирования эндокринной системы, а поскольку все процессы в организме регули-руются гормонами, то недостаток или избыток гормонов приведѐт к нарушению работы ферментов.
поскольку все ферментативные процессы «привязаны» к определѐн-ным клеточным структурам, то нарушение локализации ферментов (компартментализации) приведѐт и к нарушению их функций.
ферменты жизнеобеспечения (одинаковые во всех клетках и участвующих в синтезе белков, ДНК и РНК, в энергетическом обмене)
органспецифические ферменты (выполняющие специфические функции в определѐнных органах: в печени находятся ферменты синтеза мочевины, в щитовидной железе – йодпероксидаза, в надпо-чечниках – ферменты синтеза кортикостероидов).
Онтогенез
у новорожденных - отсутствуют ферменты поджелудочной железы, но к двум годам жизни они уже синтезируются в адекватном количестве) и при болезнях (наследственные и вторичные энзимопатии).
КЛИНИЧЕСКАЯ ЭНЗИМОЛОГИЯ, = энзимодиагностику + энзимотерапию.
ЭНЗИМОДИАГНОСТИКА – использование определения активности фермен-тов в диагностических целях. Практически любое заболевание сопровожда-ется изменением ферментного спектра, поэтому определение активности ферментов – один из важнейших критериев для постановки диагноза и разра-ботки тактики лечения. Как правило, для энзимодиагностики используют биологические жидкости – слюну, спинномозговую жидкость, и, чаще всего, кровь.
Ферменты крови по происхождению:
1)собственные ферменты крови (синтезируются печенью для обеспечения функционирования крови –ферменты свѐртывающей, противосвѐртывающей, фибринолитической систем). Эти ферменты часто на-зывают секреторными;
ферменты секретов и экскретов (попадающие в кровь из пищевари-тельных соков, жѐлчи и т.д.);
2)органспецифические (тканевые, индикаторные), синтезируемые клет-ками для собственных нужд, но в очень маленьком, строго постоян-ном количестве попадающие в кровь. Изменение их активности может свидетельствовать о нарушениях в тех или иных органах. Эти измене-ния могут носить различный характер:
• повышение активности может быть результатом ускорения процессов синтеза (щелочная фосфатаза при рахите, гепатите), некроза клеток, понижения выведения, повышении проницаемости клеточных мембран;
• снижение активности вызывается уменьшением числа клеток, секретирующих фермент (холинэстераза при циррозе печени), недостаточностью синтеза, увеличением выведения фермента, торможением активности (в результате действия протеиназ);
• исчезновение фермента может быть вызвано некрозом ткани (при некрозе поджелудочной железы сначала активность ферментов в крови увеличивается, а затем падает до нуля).
В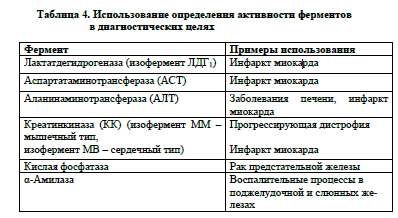 настоящее время для диагностики
используют так называемый «диаг-ностический
ферментный спектр» – комплекс ферментов,
изменения которых характерно для того
или иного заболевания. Например, острые
гепатиты ха-рактеризуются резким
увеличением активности аланин- и
аспартатами-нотрансфераз и альдолазы.
При механических желтухах характерным
являет-ся нарастание содержания щелочной
фосфатазы без большого увеличения
активности аминотрансфераз и альдолазы
настоящее время для диагностики
используют так называемый «диаг-ностический
ферментный спектр» – комплекс ферментов,
изменения которых характерно для того
или иного заболевания. Например, острые
гепатиты ха-рактеризуются резким
увеличением активности аланин- и
аспартатами-нотрансфераз и альдолазы.
При механических желтухах характерным
являет-ся нарастание содержания щелочной
фосфатазы без большого увеличения
активности аминотрансфераз и альдолазы
ЭНЗИМОТЕРАПИЯ – использование ферментов с лечебной целью. В связи с белковой природой ферментов их использование ограничено. Основными направлениями энзимотерапии являются:
ферментозаместительная терапия (при нарушении секреции пищева-рительных желѐз – пепсидил, панкреатин, мезим, фестал, креон и т.д.);
противовоспалительная терапия (трипсин, химотрипсин, коллагеназу применяют для ускорения отторжения некротизированных тканей, для очистки трофических язв, ожоговых поверхностей; рибонуклеаза и де-зоксирибонуклеаза входят в состав глазных капель для лечения ви-русных конъюнктивитов);
фибринолитическая терапия (стрептокиназу и урокиназу используют как активаторы фибринолиза при тромбозах);
литическая терапия (для рассасывания рубцов, спаек применяется ли-даза – лекарственная форма гиалуронидазы, гидролизующая компо-ненты межклеточного матрикса).
Для каждой ткани (органа) характерен определённый ферментный состав (маркерные ферменты). Для сердечной мышцы маркерными ферментами являются - аспартатаминотрансфераза (АсТ), креатинкиназа; для печени – аланинаминотрансфераза (АлТ); для предстательной железы – кислая фосфатаза ( КФ); для поджелудочной железы – α-амилаза и т.д.
При заболеваниях, сопровождающихся некрозом, маркерные (органоспецифичные) ферменты из повреждённых клеток в большом количестве поступают в кровь, и уровень их активности увеличивается, возникает гиперферментемия. Определение уровня активности маркерных ферментов в сыворотке крови имеет клиническое значение в диагностике и прогнозе ряда заболеваний.
Так, при инфаркте миокарда увеличивается уровень активности АсТ, креатиназы; вирусном гепатите – АлТ; раке предстательной железы – кислой фосфатазы; при заболеваниях поджелудочной железы – α-амилазы и т.д.
Некоторые ферменты применяют в качестве лечебных препаратов:
Пепсин – при нарушении синтеза и секреции пепсина в желудке;
Трипсин, химотрипсин используются для лечения гнойных ран;
Фибринолизин, стрептокиназа – для предотвращения тромбообразования при пересадке органов и других операциях;
Гиалуронидаза обеспечивает рассасывание рубцов;
Аспарагиназа применяется при лечении некоторых злокачественных образований и т.д.
При отсутствии или недостатке тех или иных ферментов, связанных с мутацией гена, ответственного за синтез белка – фермента, возникают наследственные энзимопатии.
При фенилпировиноградной олигофрении отсутствует фермент гидроксилаза, катализирующая превращение аминокислоты фенилаланина в тирозин. Это приводит к повышению уровня фенилаланина в крови и моче, кроме того, из фенилаланина образуется фенилпировиноградная кислота, что оказывает токсическое действие на центральную нервную систему, в результате чего развивается слабоумие.
При галактоземии отсутствует фермент галактозо-1-фосфат-уридилтрансфе-раза, катализирующий превращение галактоза-1-фосфат в глюкоза-1-фосфат. Это является причиной увеличения галактозы и галактоза-1-фосфат в крови, что сопровождается у детей грудного возраста рвотой, диареей, вздутием живота и т.д.