Материал: Курс занятий. Ферменты
Такое соответствие - не заранее "готовое", а формирующееся в ходе взаимодействия - американский ученый Кошленд положил в основу теории ИНДУЦИРОВАННОГО СООТВЕТСТВИЯ (или «НАВЕДЕННОГО» СООТВЕТСТВИЯ), которая преодолела ограниченность существовавшей ранее теории КЛЮЧА И ЗАМКА (жесткого соответствия структуры субстрата структуре адсорбционного центра).
Некоторые вещества, обладающие подходящими характеристиками (то есть похожие на субстрат), могут тоже связываться с адсорбционным центром фермента. Но если в их молекуле нет такой химической связи, на которую может воздействовать каталитический центр данного фермента, то химических превращений этого вещества не произойдет. Занимая активный центр фермента, такие молекулы блокируют его работу, то есть являются ОБРАТИМЫМИ ИНГИБИТОРАМИ данного фермента (обратимыми, потому что связаны с ферментом слабыми типами связей). Повышая концентрацию субстрата, их можно ВЫТЕСНИТЬ из адсорбционного центра. Поэтому такие ингибиторы называют КОНКУРЕНТНЫМИ. Они конкурируют с истинным субстратом данного фермента за обладание его адсорбционным центром.
АЛЛОСТЕРИЧЕСКИЙ ЦЕНТР - такие участки молекулы фермента вне его активного центра, которые способны связываться СЛАБЫМИ ТИПАМИ СВЯЗЕЙ (значит - обратимо) с тем или иным веществом (лигандом). Причем такое связывание приводит к такой конформационной перестройке молекулы фермента, которая распространяется и на активный центр, облегчая, либо затрудняя (замедляя) его работу. Соответственно такие вещества называются АЛЛОСТЕРИЧЕСКИМИ АКТИВАТОРАМИ или АЛЛОСТЕРИЧЕСКИМИ ИНГИБИТОРАМИ данного фермента.
Термин "аллостерический" (то есть "имеющий иную пространственную структуру") появился в связи с тем, что эти эффекторы по своей пространственной конфигурации совсем не похожи на молекулу субстрата данного фермента (и потому не могут связываться с активным центром фермента). Было сделано заключение, что и аллостерический центр не похож по своей структуре на активный центр фермента.
Аллостерические центры найдены не у всех ферментов. Они есть у тех ферментов, работа которых может изменяться под действием гормонов, медиаторов и других биологически активных веществ. Некоторые искусственно синтезированные лекарства обладают биологической активностью потому, что их молекулы комплементарны аллостерическому центру некоторых ферментов организма.
Принцип открытия основан или на исчезновении субстрата под действием фермента, или на появлении в реакционной смеси продуктов реакции. Биологическая жидкость, ткань или продукт, в которых в достаточном количестве присутствует фермент, называется источником фермента.
Номенклатура
1.Тривиальные названия ферментов (пепсин, трипсин, химотрипсин).
2. Рабочее: по типу катализируемой реакции (дегидрирование – дегидрогеназа, карбоксилирование – карбоксилаза).
3. Систематическое название (международная классификациия): 1972 г
Название субстрата + суффикс –аза
( Пр:,
лактат: НАД+- оксидоредуктаза, ацетил-КоА:
холин-О-ацетил-трансфераза; липиды –
липаза, сахароза – сахараза)
Пр:,
лактат: НАД+- оксидоредуктаза, ацетил-КоА:
холин-О-ацетил-трансфераза; липиды –
липаза, сахароза – сахараза)
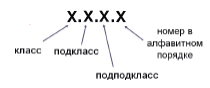
Класс 1 – оксидоредуктазы,
Подкласс 1 – окисляет гидроксильную группу,
Подподкласс 1 – акцептором водорода является НАД: алкогольдегидрогеназа
КФ 1.1.1.1. – это оксидоредуктаза, действует на ОН-группу донора с НАД в качестве акцептора с первым порядко-вым номером в своем подподклассе;
И зоэнзимы
отличаются сродством к субстрату,
максимальной скоростью катализируемой
реакции, чувствительностью к ингибиторам
и активаторам, условиями работы (оптимум
pH и температуры). Чаще всего -олигомерные
белки и «собраны» из разных типов
протомеров.
зоэнзимы
отличаются сродством к субстрату,
максимальной скоростью катализируемой
реакции, чувствительностью к ингибиторам
и активаторам, условиями работы (оптимум
pH и температуры). Чаще всего -олигомерные
белки и «собраны» из разных типов
протомеров.
Например, димерный фермент креатинкиназа (КК) 3 изоферментными формы, составленные из двух типов субъединиц: M (англ. muscle – мышца) и B (англ. brain – мозг).(КК1) локализуется в головном мозге, (КК2) – по одной М- и В в миокарде,(КК3) специфична для скелетной мышцы.
Классификация
классы(6): – по типу катализируемой реакции
подклассы – по природе атакуемой химической группы
подподклассы – по характеру атакуемой связи или по природе акцептора
1![]() .
ОКСИДОРЕДУКТАЗЫ–
окислительно-восстановительные
реакции(в основе
.
ОКСИДОРЕДУКТАЗЫ–
окислительно-восстановительные
реакции(в основе
биологического окисления). Систематическое название -«донор-акцептор-
оксидоредуктаза» (например, лактат:НАД+ оксидоредуктаза). -
- 22: дегидрогеназы, оксидазы, моно- и диоксигеназы, пероксидазы.
2![]() .
ТРАНСФЕРАЗЫ
(от
переносимой группы)–катализирующие
межмолекулярный
.
ТРАНСФЕРАЗЫ
(от
переносимой группы)–катализирующие
межмолекулярный
перенос атомов или функциональных групп (т.е. от донора к акцептору):
-9: аминотрансферазы, ацилтрансферазы, метилтрансферазы
3![]() .
ГИДРОЛАЗЫ(по
типу гидролизуемой связи)
–гидролиз
(расщепление
.
ГИДРОЛАЗЫ(по
типу гидролизуемой связи)
–гидролиз
(расщепление
химической связи с присоединением воды в ионной форме по месту разрыва):
-13:– пептидазы, фосфатазы, эстеразы (гидролизуют сложноэфирные связи),
гликозидазы
4![]() .
ЛИАЗЫ
–негидролитический
разрыв химических связей (С О, С С, C N и
других связей),
.
ЛИАЗЫ
–негидролитический
разрыв химических связей (С О, С С, C N и
других связей),
обратимые реакции отщепления различных групп от субстратов негидролитическим путем.
Эти реакции могут сопровождаться образованием двойной связи или присоединением групп
к месту двойной связи.
![]() -7подклассов
-7подклассов
5. ИЗОМЕРАЗЫ - реакции изомеризации, взаимопревращения оптических и
геометрических изомеров, а также внутримолекулярный перенос групп (в этом
случае они называются также «мутазы»).
-5 подклассов
6![]() .
ЛИГАЗЫ
(синтетазы) –присоединение
друг к другу 2 молекул с
.
ЛИГАЗЫ
(синтетазы) –присоединение
друг к другу 2 молекул с
использованием АТФ (или нуклеозидтрифосфатов):
ИЗОФЕРМЕНТЫ -ферменты, катализирующие одну и ту же реакцию, но отличающиеся -по первичной структуре
-локализованы в разных тканях
Л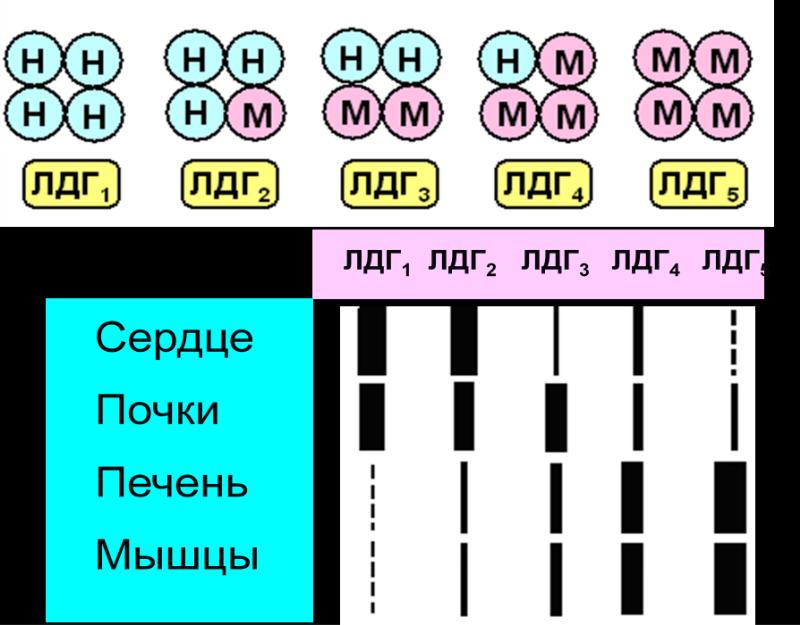 актатдегидрогеназа
(ЛДГ)
является тетрамером и состоит из
субъединиц типа M (англ. muscle – мышца) и
Н (англ. heart – сердце).
актатдегидрогеназа
(ЛДГ)
является тетрамером и состоит из
субъединиц типа M (англ. muscle – мышца) и
Н (англ. heart – сердце).
Существует пять типов ЛДГ с различным составом и локализацией.
ЛДГ 1 (Н4) и 2 (H3M1) присутствуют в тканях с аэробным обменом (миокард, мозг, корковый слой почек), обладают высоким сродством к молочной кислоте (лактату) и превращают его в пируват.
ЛДГ4 (H1M3) и ЛДГ5 (М4) находятся в тканях, склонных к анаэробному обмену (печень, скелетные мышцы, кожа, мозговой слой почек), обладают низким срод-ством к лактату и катализируют превращение пирувата в лактат.
ЛДГ3 (H2M2)-в тканях с промежуточным типом обмена (селезенка, поджелудочная железа, надпочеч-ники, лимфатические узлы). Активность разных изоферментов ЛДГ в сыворотке крови имеет клинико-диагностическое значение
ЛДГ катализирует реакцию:
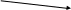 Глюкоза
ЛДГ 4,5
Глюкоза
ЛДГ 4,5


 ПВК
молочная кислота + 2 АТФ
ПВК
молочная кислота + 2 АТФ
СО2 + Н2О + 38 АТФ ЛДГ 1,2
ИММОБИЛИЗОВАННЫЕ ФЕРМЕНТЫ -ферменты,физически (адсорбционное) или химически (ковалентное) связанные с матрицей носителя, которая защищает фермент от инактивирующих воздействий, но в минимальной степени влияет на функционирование его активных центров
Осложнения при работе с ферментами:
–сложность и дороговизна получения достаточных количеств ферментов в чистом виде
--быстро теряют активность под действием различных факторов (изменение Рн, температуры, солевого состава)
--иммунологические
--невозможно создать высокую местную концентрацию фермента при локальных поражениях (не обладают способностью к
«направленному транспорту»)
Материалы носителя: неорганические пористые стекла, силикагели, а также природные или синтетические полимеры.
Виды иммобилизации:.
- реакции ацилирования, в которые могут вступать амино-окси- и некоторые другие группы белка, при этом чаще всего реакция протекает по аминогруппам лизиновых остатков.
- реакция образования азаметиновой связи (оснований Шиффа) м.у. альдегидными группами носителя и аминогруппами белка.
- терапевтические ферменты – иммобилизация на соединениях, характерных для самого организма или даже обладающих собственной биологической активностью, дополняющих или усиливающих действие связанного с ними фермента. Примером может служить фибринолизин, иммобилизованный на гепарине, урокиназа – на альбумине.
- растворимые препараты иммобилизованных ферментов медицинского назначения могут быть получены путем их межмолекулярного слияния. Например, слияние молекул галактозидазы обеспечивает стабилизацию фермента. Одновременно замедляется переваривание фермента и увеличивается время его нахождения в кровотоке.
Преимущества:
-обладают длительным сроком годности
-снижена аллергичность и иммуногенность за счет блокады антигенных участков белка макромолекулой носителя
-слабо восприимчивы к действию естественных ингибиторов
-проявляют терапевтическую активность в течение длительного времени
-более высокая стабильность ферментных препаратов,
-возможность их удаления из реакционной среды и его повторного использования
-возможность создания непрерывных процессов на ферментных колонках
-получение продукта реакции, не загрязнённого ферментом
-носитель обеспечивает устойчивость и направленную доставку фермента предпочтительно в зону поражения, т.е. в
определенный орган или ткань.
Область применения:
-могут быть компонентами аналитических систем для клинического биохимического анализа
-могут служить для модификации внутренних поверхностей, как различного рода протезов, так и медицинских аппаратов
-могут являться компонентами перевязочных и дренирующих материалов, обеспечивающих ускорение заживления и
очищения ран.
Если фермент служит для лечения местных поражений (опухолей, тромбов) и его присутствие в других органах нежелательно, то создаются биосовместимые и биоразлагаемые производные ферментов в виде микрочастиц, гранул, таблеток.
Некоторые иммобилизованные ферменты используются для наружного применения, при включении в состав различных мазей или кремов.
З ависимость скорости ферментативной реакции
от Температуры
Повышение температуры свыше 45-50˚С →тепловая денатурация→инактивпция (исключение – миокиназа мышц, папаин).
С повышением температуры ускоряется движение молекул→повышение вероятности взаимодействия реагирующих в-в.
-температура может повышать энергию реагирующих молекул, что также приводит к ускорению реакции
-скорость химической реакции, катализируемая ферментами, имеет свой температурный оптимум, превышение которого сопровождается понижением активности, возникающим из-за термической денатурации белковой мол-лы.
П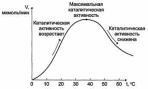 онижение
температуры
не разрушает, а приостанавливает
действие фермента
онижение
температуры
не разрушает, а приостанавливает
действие фермента
Холодовая инактивация ферментов обратима, термическая – нет, т.к. она связана с разрушением нативной структуры белка-фермента
Согласно правилу Вант-Гоффа при повышении температуры на каждые 10 градусов скорость химической реакции увеличивается приблизительно в 2-4 раза. Это правило выполняется и для ферментов, но только в пределах до 40-42ºС, затем скорость реакции начинает снижаться, что связано с денату-рацией белка.
Температурный оптимум (скорость реакции максимальна)= 37-38-40˚С(искл: термостабильные ферменты: Taq-полимераза, выделенная из микроорганизмов, живущих в горячих источниках, не инактивируется при повышении температуры до 95 °С. -используют в научно-практической
медицине для молекулярной диагностики заболеваний с использованием (ПЦР)
о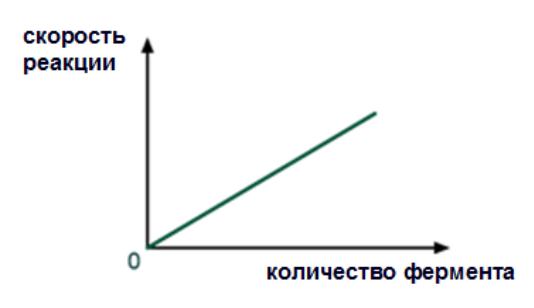 т
Концентрации фермента и субстрата
т
Концентрации фермента и субстрата
С Фермента
При увеличении - скорость реакции возрастает непрерывно и прямо пропорционально количеству фермента, т.к. большее количество молекул фермента производит большее число молекул продукта.
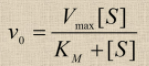
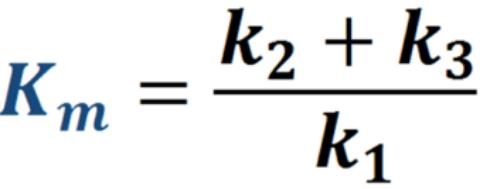
В целом скорость реакции зависит от скорости образования фермент-субстратного комплекса и скорости его разрушения или превращения в фермент-продуктный.
Каждая из этих реакций характеризуется своей константой скорости (k). Для упрощения уравнения была введена объединѐнная константа Михаэлиса, которая учитывает все три константы:
Зависимость скорости от концентрации субстрата описывается уравнением Михаэлиса-Метнен:
С Субстрата
При увеличении скорость реакции сначала возрастает (т.к. к катализу добавляемых молекул субстрата подключаются новые и новые молекулы фермента)→ скорость накопления продукта возрастает→ увеличение активности фермента. Затем→ скорость перестаѐт увеличиваться (плато на кривой), (все молекулы фермента заняты молекулами субстрата и непрерывно ведут катализ)-здесь скорость реакции максимальна, т.е. наступает насыщение фермента
1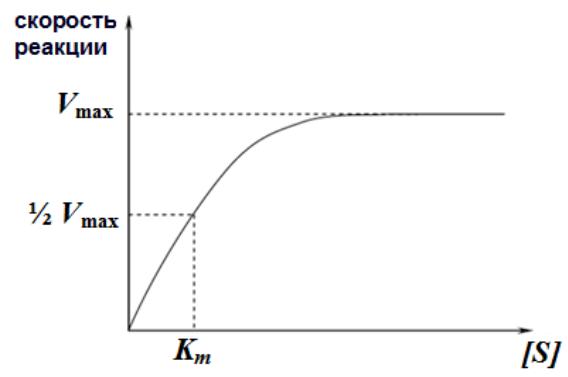 .
на начальных этапах концентрация
субстрата значительно меньше Km ([S]
<< Km). В этом случае знаменатель
уравнения мало изменяется при из-менении
[S], а величина скорости реакции V прямо
пропорциональна [S] (график линеен).
.
на начальных этапах концентрация
субстрата значительно меньше Km ([S]
<< Km). В этом случае знаменатель
уравнения мало изменяется при из-менении
[S], а величина скорости реакции V прямо
пропорциональна [S] (график линеен).
2. когда концентрация субстрата значительно больше Km ([S] >> Km), величиной Km можно пренебречь и при решении получим, что скорость реакции максимальна (плато на графике).