Материал: Курс занятий. Ферменты
Ферменты
Ферменты (латин. fermentum – «бродило», «закваска»)- энзимы (Е) (греч. en – в, внутри, zyme – дрожжи, т.е. «в дрожжах») – специфические белки, присутствующие во всех живых клетках и обеспечивающие биокатализ (изменение скорости химических реакций)
История
Ещѐ в начале XIX века было известно- мясо переваривается желудочным соком, а слюна превращает крахмал в сахар. Однако механизм этих явлений был неизвестен. История биохимии –в значительной степени история ферментов.
XVIIIв- Р. Реомюр (француз) - механизм переваривания пищи в желудке хищных птиц.
1814 г. - К.С. Киргофф - проросший ячмень способен превращать полисахарид крахмал в дисахарид мальтозу, а экстракт дрожжей расщепляет свекловичный сахар на моносахариды – глюкозу и фруктозу.
1836-Т. Шванн (немец) открыл в желудочном соке фермент пепсин (греч. pepto – «варю»)
1897-Э. Бухнеру - ферменты, полученные в виде экстракта из живых клеток, катализируют спиртовое брожение (основные метаболические процессы, связанные с производством энергии, могут функционировать вне клетки)
Дж. Самнер- первый фермент в чистом кристаллическом виде- уреаза (разрушающий мочевину)
1936- Д. Нортроп получил кристаллы пепсина, трипсина и химотрипсина
Свойства
Как белков
Высокая молекулярная масса
Образуют коллоидные растворы
Имеют сложную структурную организацию (первичную, вторичную, третичную и, нек, четвертичную)
Состоят из остатков аминокислот, соединѐнных пептидными связями
Не способны к диализу через полупроницаемые мембраны
Чувствительны к действию температуры
Термолабильны
Обладают высокой вязкостью, оптическими свойствами
Могут обратимо и необратимо осаждаться
Как катализаторов
Катализируют только термодинамически возможные реакции
Не потребляются в ходе реакции и не входят в состав конечных продуктов
В случае обратимости реакции ускоряют и прямую и обратную реакции
Ведут реакцию «в обход энергетического барьера»
Чувствительны к изменению параметров проведения реакции (температуре, рН, С катализатора и реагир. в-в)
Чувствительны к действию эффекторов – активаторов и ингибиторов
Собственные свойства
Высокая биологическая активность
Ферментная специфичность -действия
-субстратная
Наличие механизмов регуляции активности
-обладают высокой каталитической активностью по сравнению с минеральными катализаторами
Пример: реакцию разложения пероксида водорода платиновая чернь ускоряет в 2×104 раза, снижая энергию активации с 18 до 12 ккал/моль, а в присутствии каталазы - возрастает в 2×1011 раза с энергией активации 2 ккал/моль. Высокая биологическая активность определяется белковой природой и строением активного центра
Классификация
1. по химическому строению:
алифатические (липоевая кислота);
ароматические (коэнзим Q – убихинон);
гетероциклические (тиаминпирофосфат, биотин-кофермент, пи-ридоксальфосфат);
нуклеотидные (ФМН и ФАД, НАД и НАДФ, КоА, АТФ, ЦТФ, УТФ, УДФГК, ФАФС).
2. по функциям:
переносчики электронов и протонов (липоевая кислота, ФМН, ФАД, НАД, НАДФ, коэнзим Q);
переносчики групп (ТПФ, ПФ, ТГФК, КоА, биотин-кофермент);
коферменты синтеза и изомеризации (АТФ, биотин-кофермент, коферментные формы В12, КоА).
3. по механизму действия:
с высоким потенциалом переноса энергии (переносчики энергии – АТФ);
коферменты, участвующие в окислительно-восстановительных реакциях (липоевая кислота, коэнзим Q, ФМН, ФАД, НАД, НАДФ);
коферменты, формирующие активный центр фермента (все ви-таминсодержащие коферменты).
4. по скорости синтеза
Конститутивные (синтезиртся клетками с постоянной скоростью и постоянно присутствующие в клетках
Индуцируемые (адаптивные) (скорость биосинтеза и количество которых изменяется в зависимости от функционального состояния организма, характера питания, условий внешней среды)
Онтогенез: отмечается разнообразие возрастных изменений индукции ферментов. Разные периоды индукции определяют необходимость синтеза определенных ферментов. Фактор, меняющий метаболизм детского организма- изменение условий питания (характер пищи). Например, на рационе, содержащем много белка в пище, наблюдается увеличение активности ферментов, синтезирующих мочевину и превращение аминокислот.
Особенности ферментативного катализа
В основе каталитического действия - способность высокоизбирательно образовывать белково-лигандные комплексы с субстратами (веществами, на которые направлено их действие) и вызывать химические превращения субстратов.
Катализ (греч.κατάλσσις – «разрушение») – изменение скорости химической реакции в присутствии катализаторов
Теории катализа:
1)Гетерогенный катализ: реагирующие вещества и катализатор находятся в разных агрегатных состояниях, и химическая реакция ускоряется за счѐт повышения концентрации реагирующих соединений на поверхности раздела фаз
2)Гомогенный катализ: действие катализатора связано с тем, что он всту-пает во взаимодействие с реагирующими веществами с образованием промежуточных соединений, это приводит к снижению энергии акти-вации.
Теория ферментативного катализа включает в себя элементы гомогенного и гетерогенного катализов
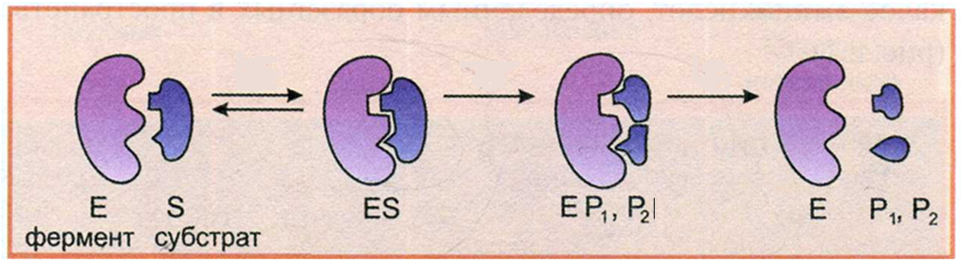
1)Фермент адсорбирует в активном центре субстрат и образует с ним нестойкое промежуточное соединение (фермент-субстратный комплекс)
2)В активном центре происходят химические превращения субстрата, и фермент-субстратный комплекс преобразуется в фермент-продуктный комплекс;
3)фермент-продуктный комплекс диссоциирует на свободный фермент и продукт реакции
![]()

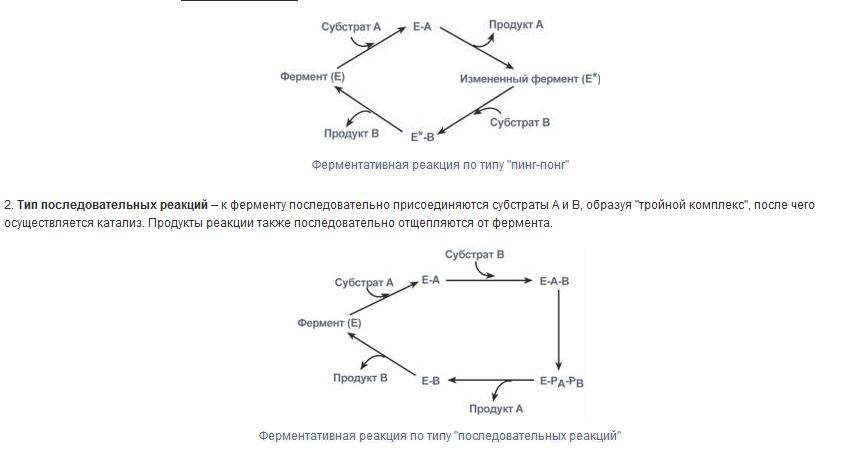
-
Ферментативная реакция
В организме каждая химическая реакция протекает на определенном энергетическом уровне, при определённой энергии активации.
- снижение
энергию активации путем увеличения
числа активированных молекул, которые
становятся реакционными на более низком
энергетическом уровне.
снижение
энергию активации путем увеличения
числа активированных молекул, которые
становятся реакционными на более низком
энергетическом уровне.
-субстрат (S) -вещество, химические превращения которого в продукт (Р) катализирует фермент (Е).
Стадии
I происходит сближение и ориентация, а также устанавливается индуцированное комплементарное соответствие между ферментом и субстратом, в результате образуется фермент-субстратный комплекс (ЕS).
II возникает напряжение и деформация субстрата, в результате чего происходит сдвиг электронной плотности, изменение степени поляризации, связи в молекуле субстрата деформируются и легко распадаются.
В процессе образования фермент-субстратного комплекса достигается переходное состояние, характеризующееся низкой энергией активации, в результате чего образуется новый продукт, а после его диссоциации фермент возвращается в исходное состояние.
Строение ферментов
П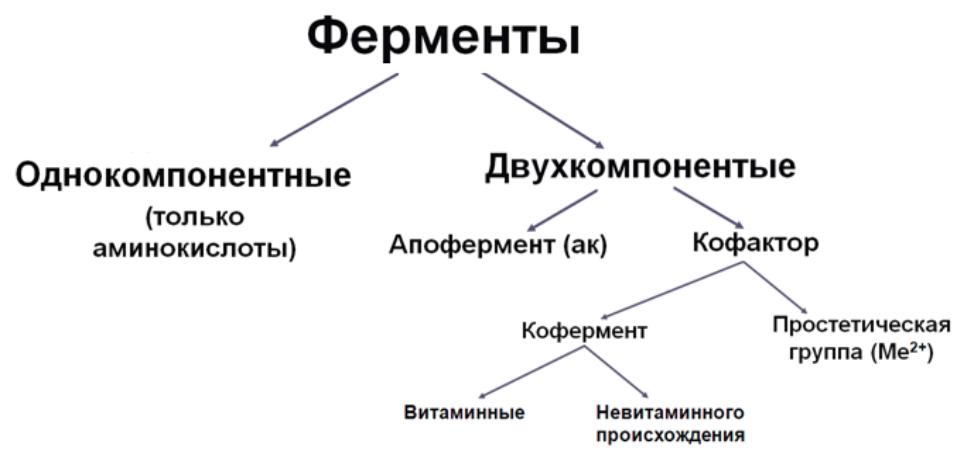 о
составу ферменты делятся на простые и
сложные
о
составу ферменты делятся на простые и
сложные
Простые -состоят из аминокислот (ферменты желудочно-кишечного тракта – α-амилаза, пепсин, трипсин, липаза и др. 3 класс – гидролаз)
Сложные -состоят из белковой части – апофермента и небелковой – кофактора (ионы металлов, так и органические соединения, многие из которых являются производными витаминов). Каталитически активный комплекс «фермент – кофактор» называется холоферментом.
Кофактор- небелковая часть ферментов:
-Простетическая группа-коферменты, которые прочно (часто ковалентно) связаны с апоферментом. Например, флавиновые дегидрогеназы состоят из белка и простетических групп ФАД, ФМН, производных витамина В2. Апофермент определяет направленность или специфичность действия фермента, прочно связана с белковой частью (ионы металлов, гем), еѐ невозможно отделить от апофермента, не разрушив при этом фермент;
-Кофермент- органические вещества, которые непрочно связаны с белковой частью (пр:НАД-зависимые дегидрогеназы состоят из белка и коферментов НАД, НАДФ, производных витамина РР, соединение белковой и небелковой частей происходит только на время биокатализа, и затем образованный ко мплекс легко разрушается
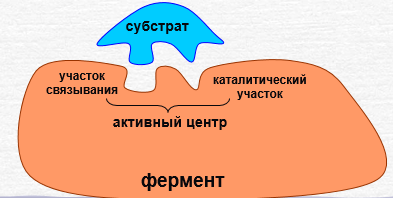
Активный центр
Активный(каталитический) центр- относительно небольшой участок молекулы фермента,
-отвечающий за распознавание, связывание и превращение субстрата,
-расположен в узком гидрофобном углублении (щели) поверхности молекулы фермента, участвующий в катализе
-точная пространственная организация больших ансамблей, построенных из аминокислотных остатков
-образуется на уровне третичной структуры белка-фермента
при образовании вторичной, третичной структур аминокислотные остатки сближаются, формируя активный центр.
Активный центр включает субстратсвязывающий участок, который отвечает за специфическое комплементарное связывание субстрата, и каталитический участок непосредственного химического взаимодействия
У однокомпонентных -представлен ФГ аминокислот(мб расположен не в соседних участках п-п цепи, но сближаются при формировании функционально активной конформации фермента)
У двухкомпонентных - гетероатомы кофакторов+ФГ аминокислот
В активном центре выделяют два участка:
-связывающий (контактный, якорный) – отвечает за связывание и ори-ентацию субстрата в активном центре
-каталитический –отвечает за осуществление реакции.
В активный центр сложных ферментов входит участок для связывания кофактора. Регуляторные (аллостерические) ферменты помимо активного центра имеют аллостерический центр. К аллостерическому центру могут присоединяться гормоны или продукты реакции→изменение структуры активного центра. Эти вещества называются аллостерическими эффекторами (модификаторами)-мб положительными (усиливают действие фермента) и отрицательными (блокируют действие фермента)
Теории конформации активного центра:
1. Теория Фишера (теория жѐсткой матрицы, «ключа и замка»): в фер-менте существует полностью сформированный активный центр, в ко-тором по принципу комплиментарности происходит взаимодействие фермента и субстрата
2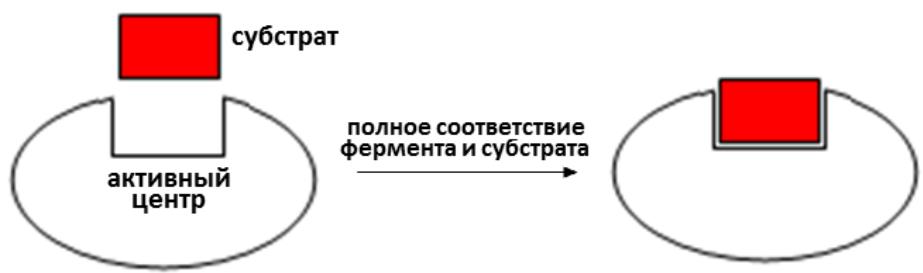
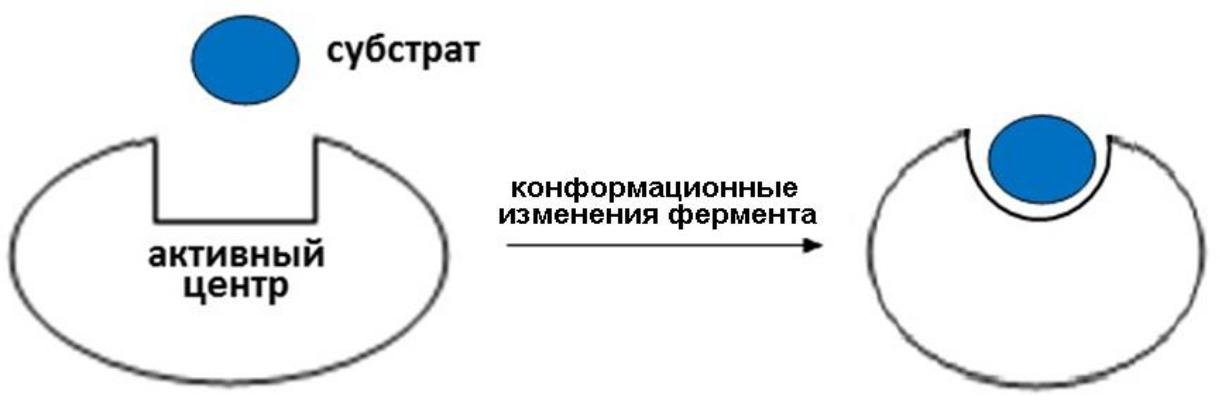 .
Теория Кошленда (теория индуцированного
соответствия, «руки и перчатки»): в
ферменте существует активный центр,
который полно-стью формируется только
при взаимодействии фермента и субстрата,
т.е. «подстраивается» под субстрат
.
Теория Кошленда (теория индуцированного
соответствия, «руки и перчатки»): в
ферменте существует активный центр,
который полно-стью формируется только
при взаимодействии фермента и субстрата,
т.е. «подстраивается» под субстрат
В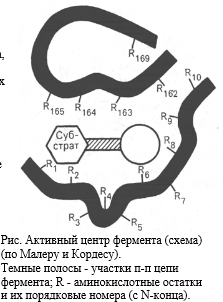 пределах активного центра различают
АДСОРБЦИОННЫЙ и КАТАЛИТИЧЕСКИЙ УЧАСТОК
(центр). Вне активного центра фермента
встречаются особые функциональные
участки; каждый из них обозначают
термином АЛЛОСТЕРИЧЕСКИЙ ЦЕНТР.
пределах активного центра различают
АДСОРБЦИОННЫЙ и КАТАЛИТИЧЕСКИЙ УЧАСТОК
(центр). Вне активного центра фермента
встречаются особые функциональные
участки; каждый из них обозначают
термином АЛЛОСТЕРИЧЕСКИЙ ЦЕНТР.
КАТАЛИТИЧЕСКИЙ ЦЕНТР - область (зона) активного центра фермента, которая непосредственно участвует в химических преобразованиях субстрата. Формируется он за счет радикалов двух, иногда трех аминокислот, расположенных в разных местах полипептидной цепи фермента, но пространственно сближенных между собой за счет изгибов этой цепи. Например, каталитический центр "серин-гистидиновых" ферментов формируется за счет радикалов аминокислот серина и гистидина. Если фермент является сложным белком, то в формировании каталитического центра нередко участвует простетическая группа молекулы фермента (кофермент). Коферментную функцию выполняют все водорастворимые витамины и жирорастворимый витамин K.
АДСОРБЦИОННЫЙ ЦЕНТР - это участок активного центра молекулы фермента, на котором происходит сорбция (связывание) молекулы субстрата. Он формируется одним, двумя, чаще тремя радикалами аминокислот, которые обычно расположены рядом с каталитическим центром. Главная его функция - связывание молекулы субстрата и передача этой молекулы каталитическому центру в наиболее удобном положении (для каталитического центра). Эта сорбция происходит только за счет слабых типов связей и потому является обратимой. По мере формирования этих связей происходит конформационная перестройка адсорбционного центра, которая приводит к более тесному сближению субстрата и активного центра фермента, более точному соответствию между их пространственными конфигурациями.