Материал: Курс занятий. Ферменты
3. если концентрация субстрата равна величине константы Михаэлиса ([S] = Km), по уравнению Михаэлиса-Ментен получаем, что скорость реакции V будет равна половине максимальной Vmax (V = ½ Vmax). Таким образом, Km соответствует концентрации субстрата, при которой скорость реакции равна половине максимальной.
от Реакции среды
О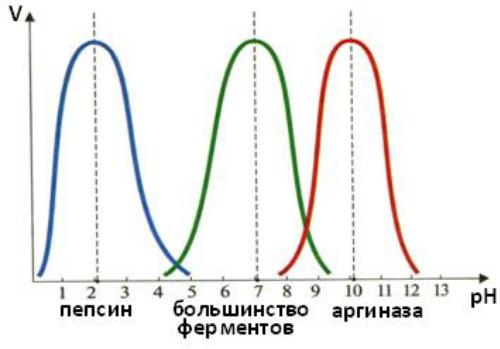 птимум
рН среды
-значение рН среды, при котором фермент
проявляет максимальную активность для
действия данного фермента.
птимум
рН среды
-значение рН среды, при котором фермент
проявляет максимальную активность для
действия данного фермента.
-лежит в пределах физиологических значений 6,0-8,0. (исключения: пепсин, (2,0); аргиназа – (10,0)
Зависимость скорости реакции от концентрации водородных ионов
определяется двумя факторами:
1.ионы Н+ и ОН− влияют на степень диссоциации ионогенных групп, т.е.
на конформацию белка;
2.ионы Н+ и ОН− влияют на сродство фермента и субстрата, т.к. могут вызывать и изменения конформации субстрата.
При небольшом сдвиге кислотности среды от оптимума скорость реак-ции уменьшается обратимо, при значительном – может насупить кислотная (или щелочная) денатурация, и фермент инактивируется необратимо.
Специфичность ферментов, ее виды
К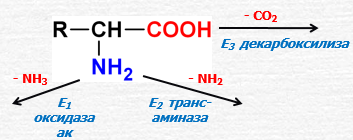 аталитическая
специфичность (специфичность действия)
– способность
фермента катализировать превращение
субстрата по одному из возможных путей
превращения.
аталитическая
специфичность (специфичность действия)
– способность
фермента катализировать превращение
субстрата по одному из возможных путей
превращения.
Так, один и тот же субстрат может вступать в различные химические реакции, каждая из которых катализируется собственным ферментом, например, для аминокислот характерны реакции декар-боксилирования (фермент декарбоксилаза), дезаминирования (фермент окси-даза аминокислот) и трансаминирования (фермент трансаминаза):
Субстратная специфичность − это способность фермента узнавать, связывать и катализировать превращение только определѐнных субстратов, может быть:
• абсолютная;
• относительная;
• стереоспецифичность.
А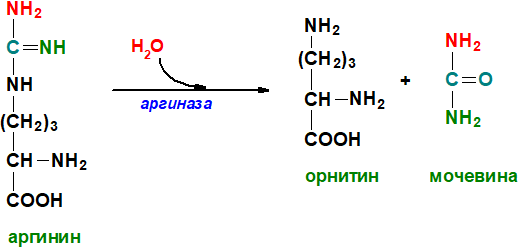 бсолютная
специфичность:
фермент может взаимодействовать только
с одним-единственным субстратом.
Например, уреаза расщепляет только
мочевину, а каталаза – только перекись
водорода:
бсолютная
специфичность:
фермент может взаимодействовать только
с одним-единственным субстратом.
Например, уреаза расщепляет только
мочевину, а каталаза – только перекись
водорода:
О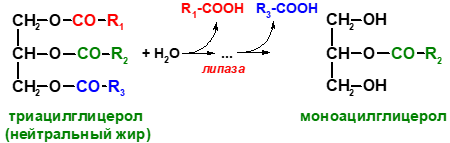 тносительная
(групповая) специфичность –
фермент может взаимодействовать с
группой сходных по строению субстратов.
Например, липаза расщепляет сложноэфирные
связи в любых жирах (триацилглицеролах),
а протеиназы – белки и пептиды, т.е.
действуют на пептидные связи.
тносительная
(групповая) специфичность –
фермент может взаимодействовать с
группой сходных по строению субстратов.
Например, липаза расщепляет сложноэфирные
связи в любых жирах (триацилглицеролах),
а протеиназы – белки и пептиды, т.е.
действуют на пептидные связи.
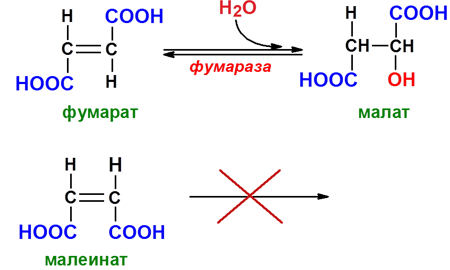
Стереоспецифичность - фермент действует только на один из возможных изомеров вещества (на D- илиL-стереоизмеры, цис- или транс-изомеры и т.д.). Так, фермент фумараза гидратирует транс-изомер бутен-1,4-диовой кислоты (фумаровую кислоту), но не оказывает влияния на цис-изомер – малеиновую
Эффекторы
(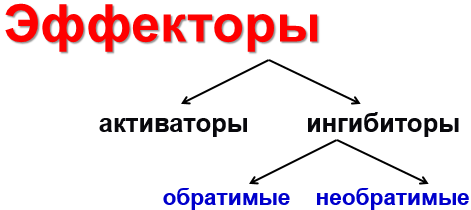 модификаторы)
-вещества, которые оказывают действие
непосредственно на фермент, изменяя
его активность.
модификаторы)
-вещества, которые оказывают действие
непосредственно на фермент, изменяя
его активность.
По направлению влияния -положительными (активаторы)
-отрицательными (ингибиторы).
АКТИВАТОРЫ (увеличивают скорость ферментативных реакций):
-неорганические вещества (ионы металлов; кислоты, например, Fe²+, Mg²+, Mn²+, Cu²+, Zn²+, АТФ, липоевая кислота, соляная – активатор пепсина; анионы, например, Сl – активатор амилазы);
-низкомолекулярные органические вещества (например, соли жѐлчных кислот, активирующие панкреатическую липазу);
-белки-ферменты
механизмы действия активаторов:
-служат «площадкой» для взаимодействия фермента и субстрата;
-повышают сродство фермента и субстрата;
-отщепляют ингибитор
Ферменты желудочно-кишечного тракта вырабатываются в виде неактивных форм – зимогенов. Под влиянием различных факторов происходит отщепление пептида с формированием активного центра и зимоген превращается в активную форму.
 П
П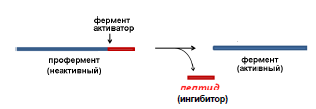 епсиноген
НСl
пепсин + пептид
епсиноген
НСl
пепсин + пептид
 Трипсиноген
энтерокиназа трипсин + пептид
Трипсиноген
энтерокиназа трипсин + пептид
предохраняет клетки ЖКТ от самопереваривания
- активация протекает по механизму частичного (ограниченного, локального) протеолиза: от неактивного предшественника (профермента) отщепляется пептид (рвѐтся одна или несколько пептидных связей), и фермент переходит в активную форму за счѐт формирования активного центра
ИНГИБИТОРЫ(снижают скорость реакции)
По прочности соединения ингибитора с ферментом
Обратимые ингибиторы –соединения, которые нековалентно взаимодействуют с ферментом и отщепляются от фермента.
Необратимые ингибиторы – соединения, которые образуют ковалентные, прочные связи с ферментом.
Специфическое--ингибиторы тормозят действие определенных ферментов, связывая отдельные функциональные группы активного центра. (Например, тиоловые яды ингибируют ферменты, в активный центр которых входят SН-группы; угарный газ (СО) ингибирует ферменты, имеющие в активном центре Fe²+)
Неспецифические--ингибиторы тормозят действие всех ферментов. К ним относятся все денатурирующие факторы (высокая температура, органические и минеральные кислоты, соли тяжелых металлов и др.).
По механизму действия:
конкурентным;
неконкурентным;
бесконкурентным;
субстратным;
аллостерическим.
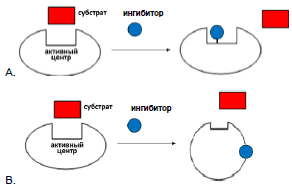
1 )Конкурентное ингибирование
-ингибитор имеет структурное сходство с субстратом и конкурирует с ним за место в активном центре фермента→уменьшение связывания субстрата с ферментом и нарушение катализа
-возможность усилить или ослабить ингибирование путѐм изменения концентраций субстрата и ингибитора
Клиника: многие лекарственные средства являются конкурентными ингибиторами ферментов.
сульфаниламиды – структурные аналоги ПАБК (фрагмента фолиевой кислоты, витамина В9) используют для лечения бактериальных инфекций;
ингибитор синтеза холестерина ловастатин, ингибирующий ГМГ-S-КоА-редуктазу; антикоагулянты, конкуренты витамина К – дикумарол и варфарин;
средство для лечения подагры аллопуринол, ингибирующий ксантиноксидазу.
Конкурентные ингибиторы используются также как антидоты при отравлениях, например, этиловый спирт может быть использован при отравлении метанолом, так как между этими спиртами происходит конкуренция за активный центр алкогольдегидрогеназы)
2)Неконкурентное ингибирование
- вызывается веществами, не имеющими структурного сходства с субстратом.
-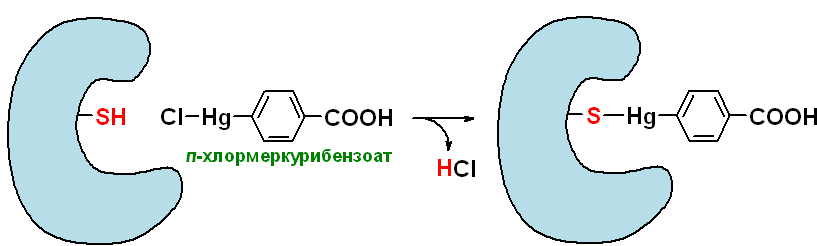 неконкурентные ингибиторы взаимодействуют
с функциональными группами белка-фермента
или в самом активном центре («выключая»
активный центр – А), или вне активного
центра (приводя к изменению конформации
активного центра – В).
неконкурентные ингибиторы взаимодействуют
с функциональными группами белка-фермента
или в самом активном центре («выключая»
активный центр – А), или вне активного
центра (приводя к изменению конформации
активного центра – В).
- образуются прочные ковалентные связи, что является причиной необратимости неконкурентного ингибирования.
степень ингибирования не зависит от концентрации субстрата;
ингибирование необратимо;
ингибирование наступает при малых количествах ингибитора
И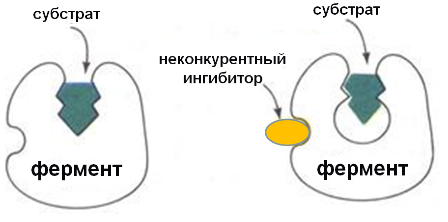 нгибиторы:
нгибиторы:
соли тяжѐлых металлов (вызывают денатурацию белка и разрушение АЦ – неспецифическое ингибирование)
яды (цианиды связываются с активным центром цитохром-оксидазы и нарушают образование АТФ)
ф
 осфорорганические
вещества, пестициды, инсектициды (ДФФ
– диизопропилфторфосфат прочно и
необратимо связывается с гидроксигруппой
серина в активном центре фермента
ацетилхолинэстеразы, гидролизующей
ацетилхолин в нервных синапсах);
осфорорганические
вещества, пестициды, инсектициды (ДФФ
– диизопропилфторфосфат прочно и
необратимо связывается с гидроксигруппой
серина в активном центре фермента
ацетилхолинэстеразы, гидролизующей
ацетилхолин в нервных синапсах);
боевые отравляющие вещества (зарин, зоман, табун – ингибиторы холинэстеразы).
Клиника: ацетилсалициловая кислота (аспирин) ингибирует циклооксигеназу – ключевой фермент синтеза простагландинов – веществ, вызывающих повышение температуры и болевой синдром при воспалениях. Эта кислота входит в состав средств, использующихся при воспалительных заболеваниях и лихорадочных состояниях. Пенициллин необратимо влияет на фермент транспептидазу, нарушая образование клеточной стенки бактерий.
3)Бесконкурентное ингибирование
-![]() торможение
ферментативной реакции, вызванное
присоединением ингибитора только к
комплексу фермент-субстрат с образованием
тупикового продукта ESI.
торможение
ферментативной реакции, вызванное
присоединением ингибитора только к
комплексу фермент-субстрат с образованием
тупикового продукта ESI.
-ингибитор вызывает такие конформационные измене-ния фермента, которые не дают возможности превращать субстрат в продукт реакции.
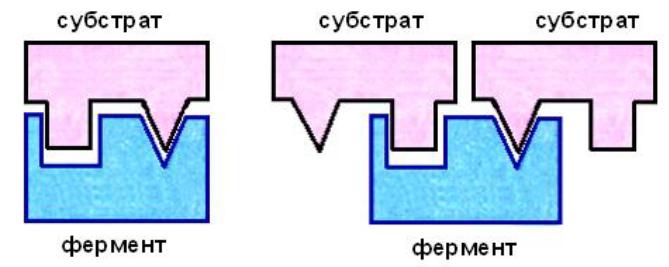
4)Субстратное ингибирование – ингибирование избытком субстрата.
-между молекулами субстрата происходит своеобразная конкуренция за место в активном центре, в результате чего скорость реакции снижается
-ингибирование обратимо