Материал: Курс занятий. Белки
3. нарушается синтез медиаторов, нарушается проведение нервных импульсов, страдает нервная система,
4. изменяется концентрация в крови катионов натрия и калия, нарушается электролитный баланс.
Поскольку аммиак очень токсичен, его необходимо повсеместно обезвреживать с образованием транспортных форм (глутамата, глутамина, амидированных карбоксильных групп белков плазмы крови), которые затем направляются в печень или в почки, где осуществляется окончательное обезвреживание аммиака с образованием менее токсичных форм его выведения – мочевины, аммонийных солей. При катаболизме сложных белков распад простетических групп приводит к образованию других азотсодержащих конечных продуктов (желчных пигментов, мочевой кислоты). Высокая степень разветвленности метаболических путей превращения аминокислот вовлекает в процесс множество высокоспецифичных ферментных систем, генетические дефекты которых обуславливают появление большого количества наследственных нарушений аминокислотного обмена, проявляющихся тяжелыми наследственными болезнями.
Трансаминирование, химизм. Трансаминазы, их специфичность. Роль витамина в6 в трансаминировании.
Трансаминирование – процесс переноса аминогруппы с α-аминокислоты на кетокислоту при участии ферментов трансаминаз (В6 – фосфопиридоксаль). Этому процессу подвергаются все аминокислоты, кроме лизина, треонина и пролина.
Реакцию трансаминирования катализируют высокоактивные аминотрансферазы: аланинаминотрансфераза (АЛТ) и аспартатаминотрансфераза (АСТ), которые обладают субстратной специфичностью.
АЛТ и АСТ – органоспецифические ферменты, в норме в крови их активнрсть равна 5-40 ЕД/л, т.е. активность трансаминаз сравнительно низкая. При заболеваниях, сопровождающихся деструкцией (некрозом) клеток, происходит выход ферментов в кровь и повышение их активности. Определение активности АЛТ и АСТ имеет большое диагностическое значение. Для дифференциальной диагностики заболеваний печени и сердца определяют соотношение активности АСТ/АЛТ в сыворотке крови – «коэффициент де Ритиса», который в норме составляет 1,33±0,42.
При гепатитах активность АЛТ увеличивается в 6-8 раз по сравнению с нормой, а АСТ – в2-4 раза. «Коэффициент де Ритиса» уменьшается примерно до 0,6. Особенно важное значение для диагностики имеет повышение активности АЛТ при безжелтушных формах вирусного гепатита. У детей при гепатитах активность АЛТ возрастает еще в дожелтушный период развития болезни. Однако, при церрозе печени «Коэффициент де Ритиса» приближается к 1,0, что свидетельствует о некрозе клеток, при котором в кровь выходят обе фракции (цитоплазматическая и митохондриальная).
При инфаркте миокарда активность АСТ увеличивается в 8-10 раз, а АЛТ – в 1,5 -2,0 раза. Значение «Коэффициента де Ритиса» резко возрастает. Инфекционные и токсические миокардиты характеризуются повышением АСТ, это же самое наблюдается при операциях на сердце.
При стенокардии, пороках сердца, инфаркте легкого активность аминотрансфераз в крови не возрастает.
ОСОБАЯ РОЛЬ ГЛУТАМАТА В РЕАКЦИЯХ ТРАНСАМИНИРОВАНИЯ.
Чаще всего в реакциях трансаминирования участвуют аминокислоты, содержание которых в тканях значительно выше остальных - глу-тамат, аланин, аспартат и соответствующие им кетокислоты - α-кетоглутарат, пируват и оксалоацетат. Основным донором аминогруппы служит глутамат.
Акцептором
аминогруппы любой аминокислоты,
подвергающейся трансаминированию
(аминокислота 1), служит α-кетоглутарат.
Принимая аминогруппу, он превращается
в глутамат, который способен передавать
эту группу любой α-кетокислоте с
образованием другой аминокислоты
(аминокислота 2).
Биологическая роль реакций трансаминирования
Путь синтеза заменимых аминокислот
Путь перераспределения азота без образования токсичного аммиака
Путь пополнения энергетического материала (образование субстратов окислительного декарбоксилирования ПВК и ЦТК)
Определение трансаминаз в сыворотке крови.
Аминотрансферазы – ферменты, катализирующие межмолекулярный перенос аминогруппы с аминокислоты на кетокислоту без образования свободного аммиака. Аминотрансферазы также называют трансаминазами, а реакцию — трансаминированием. Для аминотрансфераз донором аминогрупп являются аминокислоты, а акцептором — кетокислоты: AK1 + KK2 ↔ KK1 + AK2
Наибольшее значение имеет определение активности 2-х ферментов: аспартатаминотрансфе-разы (АсАТ) и аланинаминотрансферазы (АлАТ). Эти ферменты обладают высокой каталитической активностью, широко распространены в различных органах и тканях: сердечная мышца, печень, почки, скелетная мускулатура, т.п.
Определение активности АсАТ и АлАТ используется для диагностики болезней печени и заболеваний сердца. При болезни Боткина значительно возрастает активность АлАТ. Изменения активности, как правило, отражают тяжесть поражения печеночной паренхимы. Увеличивается активность АлАТ при обострении хронического гепатита, при токсическом поражении паренхимы печени. Изменение активности аспартатаминотрансферазы характеризует поражение сердечной мышцы. При инфаркте миокарда активность повышается уже через 4-6 часов и держится высокой в течение 3-7 дней. (Это особенно важно при инфарктах, не диагносцируемых на ЭКГ). Повышается активность АсАТ при гипертонических кризах.
Д езаминирование аминокислот
Дезаминирование – процесс потери аминокислотой аминогруппы, в результате чего образуется соответствующая α-кетокислота (безазотистый остаток) и выделяется молекула аммиака. В организме подвергается этому процессу только глутаминовая кислота, т.к. в организме активен фермент глутаматдегидрогеназа (ГДГ). Фермент ГДГ активен в митохондриях клеток всех органов, кроме мышечной ткани.
Окислительное дезаминирование химизм. Роль глутаматдегидрогеназы. Биологическая роль окислительного дезаминирования аминокислоты.
Наиболее активно в тканях происходит дезаминирование глутаминовой кислоты. Реакцию катализирует фермент глутаматдегидрогеназа, коферментом глутаматдегидрогеназы является NAD+. Реакция идёт в 2 этапа. Вначале происходит ферментативное дегидрирование глутамата и образование а-иминоглутарата, затем - неферментативное гидролитическое отщепление иминогруппы в виде аммиака, в результате чего образуется а-кетоглутарат. Окислительное дезаминирование глутамата - обратимая реакция и при повышении концентрации аммиака в клетке может протекать в обратном направлении, как восстановительное шинирование α-кетоглутарата. Глутаматдегидрогеназа очень активна в митохондриях клеток практически всех органов, кроме мышц. Этот фермент - олигомер, состоящий из 6 субъединиц (молекулярная масса 312 кД). Глутаматдегидрогеназа играет важную роль, так как является регуляторным ферментом аминокислотного обмена. Аллостерические ингибиторы глутаматдегидрогеназы (АТФ, ГТФ, NADH) вызывают диссоциацию фермента и потерю глутаматдегидрогеназной активности. Высокие концентрации АДф активируют фермент. Таким образом, низкий энергетический уровень в клетках стимулирует разрушение аминокислот и образованиеα-кетоглутарата, поступающего в ЦТК как энергетический субстрат. Глутаматдегидрогеназа может индуцироваться стероидными гормонами (кортизолом).
Оксидаза L-аминокислот. В печени и почках обнаружен фермент оксидаза L-аминокислот, способный дезаминировать некоторые L-аминокислоты. Коферментом в данной реакции выступает FMN. Однако вклад оксидазы L-аминокислот в дезаминирование, очевидно, незначителен, так как оптимум её действия лежит в щелочной среде (рН 10,0). В клетках, где рН среды близок к нейтральному, активность фермента очень низка.
Оксидаза D-аминокислот также обнаружена в почках и печени. Это FAD-зависимый фермент. Оптимум рН этой оксидазы лежит в нейтральной среде, поэтому фермент более активен, чем оксидаза L-аминокислот. Роль оксидазы D-аминокислот невелика, так как количество D-изомеров в организме крайне мало, потому что в белки пищи и белки тканей человека и животных входят только природные L-аминокислоты. Вероятно, оксидаза D-аминокислот способствует их превращению в соответствующие L-изомеры.
Непрямое дезаминирование аминокислот, понятие, стадии, биологическое значение.
Непрямое дезаминирование (трансдезаминирование) Большинство аминокислот не способно дезаминироваться в одну стадию, подобно Глу. Аминогруппы таких аминокислот в результате трансаминирования переносятся на α-кетоглутарат с образованием глутаминовой кислоты, которая затем подвергается прямому окислительному дезаминированию. Такой механизм дезаминирования аминокислот в 2 стадии получил название трансдезаминирования, или непрямого дезаминирования:
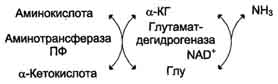
Непрямое дезаминирование аминокислот происходит при участии 2 ферментов: аминотрансферазы (кофермент ПФ) и глутаматдегидрогеназы (кофермент NAD+).
непрямое дезаминирование - основной способ дезаминирования большинства аминокислот. Обе стадии непрямого дезаминирования обратимы, что обеспечивает как катаболизм аминокислот, так и возможность образования практически любой аминокислоты из соответствующей α-кетокислоты.
В мышечной ткани активность глутаматдегидрогеназы низка, поэтому в этих клетках при интенсивной физической нагрузке функционирует ещё один путь непрямого дезаминирования с участием цикла ИМФ-АМФ. Вначале происходит перенос аминогруппы аминокислот на аспартат, затем на инозиновую кислоту (ИМФ) и в завершение - дезаминирование АМФ. Представленная схема отражает последовательность реакций непрямого неокислительного дезаминирования:
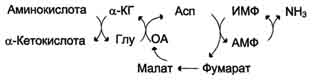
Можно выделить 4 стадии процесса:
трансаминирование с α-кетоглутаратом, образование глутамата;
трансаминирование глутамата с оксалоацета-том (фермент ACT), образование аспартата;
реакция переноса аминогруппы от аспартата на ИМФ (инозинмонофосфат), образование АМФ и фумарата;
гидролитическое дезаминирование АМФ.
Перенос аминогруппы от аспартата и синтез АМФ происходят следующим образом.
Реакция дезаминирования адениловой кислоты происходит под действием фермента АМФ дезаминазы Этот путь дезаминирования преобладает в мышцах при интенсивной работе, в результате которой накапливается молочная кислота. Выделяющийся аммиак предотвращает закисление среды в клетках, вызванное образованием лактата.
Биологическая роль непрямого дезаминирования. А - при катаболизме почти все природные аминокислоты сначала передают аминогруппу на а-кетоглутарат в реакции трансаминирования с образованием глутамата и соответствующей кетокислоты. Затем глутамат подвергается прямому окислительному дезаминированию под действием глутаматдегидрогена-зы, в результате чего получаются а-кетоглутарат и аммиак; Б - при необходимости синтеза аминокислот и наличии необходимых α-кетокислот обе стадии непрямого дезаминирования протекают в обратном направлении. В результате восстановительного аминирования а-кетоглутарата образуется глутамат, который вступает в трансаминирование с соответствующей α-кетокислотой, что приводит к синтезу новой аминокислоты
Декарбоксилирование аминокислот, химизм, ферменты, субстратная специфичность декарбоксилаз.
Декарбоксилирование – процесс отщепления группы СО2 при участии декарбоксилаз, небелковый компонент которых пиридоксальфосфат (ПФ), активная форма витамина В6. Реакции декарбоксилирования необратимы. Их продуктами являются СО2 и биогенные амины, которые выполняют функцию нейромедиаторов (серотонин, дофамин, ГАМК), гормонов (адреналин, норадреналин), регуляторных факторов местного действия (гистамин, карнозин и др.).

Биогенные амины, механизм образования, влияние на процессы метаболизма и физиологические функции. Окисление биогенных аминов.
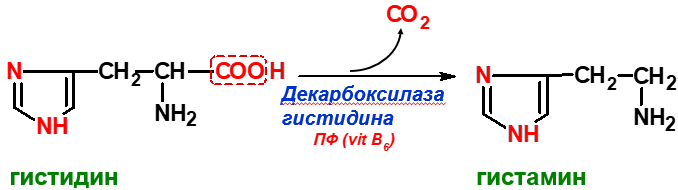
Гистамин – образуется путем декарбоксилирования гистидина в тучных клетках соединительной ткани. Секретируется в кровь при повреждении ткани (удар, ожог), развитии иммунных и аллергических реакций. Роль:
стимулирует секрецию желудочного сока, слюны;
п
 овышает
проницаемость капилляров, вызывает
отеки, снижает АД (но увеличивает
внутричерепное давление, вызывает
головную боль);
овышает
проницаемость капилляров, вызывает
отеки, снижает АД (но увеличивает
внутричерепное давление, вызывает
головную боль);сокращает гладкую мускулатуру легких, вызывает удушье;
участвует в формировании воспалительной реакции – вызывает расширение сосудов, покраснение кожи, отечность ткани;
выполняет роль нейромедиатора;
является медиатором боли.
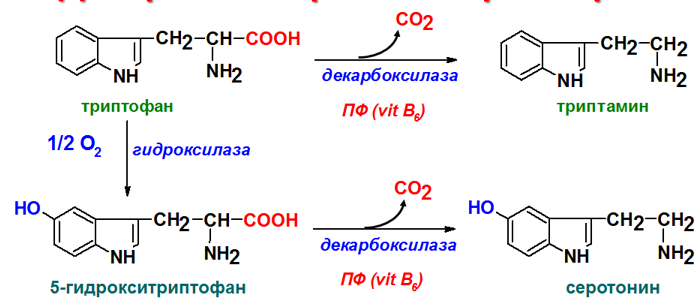
Серотонин – нейромедиатор проводящих путей. Образуется в надпочечниках и ЦНС из аминокислоты 5-окситриптофана. Он может превращаться в гормон мелатонин, регулирующий суточные и сезонные изменения метаболизма организма и участвующий в регуляции репродуктивной функции. Роль:
стимулирует сокращение гладкой мускулатуры;
оказывает сосудосуживающий эффект;
регулирует АД, температуру тела, дыхание;
обладает антидепрессантным действием;
принимает участие в аллергических реакциях.
Образование катехоламинов и гамк, функции аминов.
В мозговом веществе надпочечников и нервной ткани тирозин является предшественником катехоламинов (дофамина, норадреналина, адреналина).
При образовании катехоламинов и меланина (в меланоцитах) промежуточным продуктом служит диоксифенилаланин (ДОФА). Однако гидроксилирование тирозина в клетках различных типов катализируется различными ферментами:
- Тиразиназа ( Cu-зависимый фермент)
- Тирозингидроксилаза (1)
- ДОФА – декарбоксилаза (2)
- дофамингидроксилаза (3)
- фенилэтаноламин-N-метилтрансфераза (4)
дофамин и норадреналин служат медиаторами в синаптической передаче нервных импульсов, а адреналин – гормон широкого спектра действия, регулирующий энергетический обмен. Одна из функций катехоламинов – регуляция деятельности ССС.
γ-аминомаслянная кислота (ГАМК) – образуется путем декарбоксилирования глутаминовой кислоты. Основной тормозной медиатор высших отделов мозга. Роль:
1.увеличивает проницаемость постсинаптических мембран для ионов К+, что вызывает торможение нервного импульса;
2. повышает дыхательную активность нервной ткани;
3. улучшает кровоснабжение головного мозга.