Материал: Курс занятий. Белки
Пищевые белки как источник аминокислот. Качественный состав и биологическая ценность пищевых белков.
Критерии полноценности пищевого белка
Белок должен содержать все заменимые аминокислоты в соотношениях, близких к их соотношениям в человеческом организме
Белок должен перевариваться ферментами ЖКТ
Белок не должен содержать веществ, мешающих перевариванию и усваиванию
Для обмена белков характерно:
– неспособность организма собирать углеродные скелеты ряда аминокислот (незаменимые аминокислоты), они должны поступать с пищей в составе полноценных белков;
– сохранение постоянного баланса аминокислот в тканях при значительном колебании содержания их в пище;
– постоянное обновление белков, скорость которого определяется локализацией молекулы, функцией, строением, возрастом организма (динамическое состояние);
– чрезвычайная разветвленность метаболических путей превращения аминокислот в тканях.
Белки – незаменимый фактор питания, потребность, составляет 1,0-1,5 г/кг массы у взрослого человека и зависит от возраста, интенсивности метаболических процессов в тканях и качества пищевого белка (содержания в нем незаменимых аминокислот, способности гидролизоваться в желудочно-кишечном тракте). В переваривании белков участвует две группы протеолитических пищеварительных ферментов:
– эндопептидазы – ферменты, рвущие внутренние пептидные связи,
– экзопептидазы, отщепляющие N-концевые и С-концевые амино-кислотные остатки и завершающие протеолиз.
Динамическое состояние белков в организме. Нормы белка в питании. Азотистый баланс.
Фонд свободных аминокислот организма составляет примерно 35 г. Содержание свободных аминокислот в крови в среднем 35-65 мг/дл. Большая часть входит в состав белков, масса которых во взрослом организме 15 кг. В организме в сутки распадается на аминокислоты 400 грамм белка, столько же синтезируется. Для поддержания баланса необходимо 30-50 г в сутки, при физической нагрузки 100-120 г в сутки.
Азотистый баланс – соотношение поступившего в организм азота (в виде азота аминокислот) и выведенного азота (в виде конечных продуктов обмена – мочевины и солей аммония)
Виды азотистого баланса:
«положительный» – если азота выведено меньше, чем введено, т.е. азот задерживается в организме (в норме это имеет место у беременных, в растущем организме). При этом происходит накопление белков в тех или иных органах и тканях.
«нулевой» – азотистое равновесие.
«отрицательный» – если азота выведено больше, чем введено. Это значит, что в организме идет распад белков органов и тканей (сахарный диабет, ожоги, злокачественные новообразования и др.), который не компенсируется белками пищи. Он наблюдается при заболеваниях, связанных с усиленным распадом белков тканей, в старческом возрасте.
К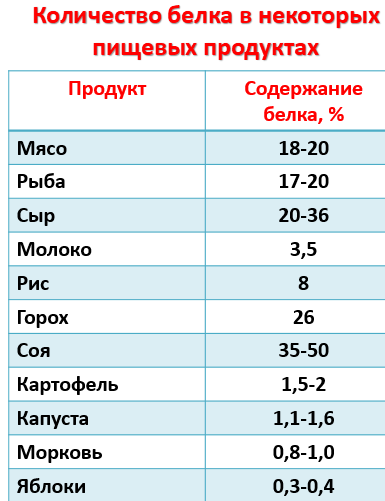 оэффициент
изнашивания – это результат ежесуточного
распада тканевого белка, который
равняется 23,2 г. Определен он был на
добровольцах, у которых на 8-10 день
безбелковой диеты начинает выделяться
постоянное количество азота (53 мг в
сутки на 1 кг массы тела).
оэффициент
изнашивания – это результат ежесуточного
распада тканевого белка, который
равняется 23,2 г. Определен он был на
добровольцах, у которых на 8-10 день
безбелковой диеты начинает выделяться
постоянное количество азота (53 мг в
сутки на 1 кг массы тела).
Потребность в пищевых белках
23,2 г/сут – коэффициент Рубнера – «коэффициент изнашивания» (азотистый баланс отрицательный).
30-45 г/сут – «физиологический минимум белка». Это минимальное количество белка, позволяющее поддерживать азотистое равновесие.
Физиологическая норма – 1-1,2 г белка на кг массы тела
П ереваривание белков
Переваривание белков начинается в желудке. Большую роль в этом процессе занимает соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов – гастринов, которые вызывают секрецию соляной кислоты (образуется в обкладочных клетках желудочных желез) и профермента пепсиногена. Под действием соляной кислоты происходит денатурация белков пищи, не подвергшихся термической обработке. НСl обладает бактерицидным действием и препятствует попаданию патогенных бактерий в кишечник. Она активирует пепсиноген и создает оптимум рН для действия пепсина.
Желудочное содержимое (химус) в процессе перевариваня поступает в двенадцатиперстную кишку. Низкое значение рН химуса вызывает в кишечнике выделение секретина, поступающего в кровь. Он стимулирует выделение из поджелудочной железы в тонкий кишечник панкреатического сока, содержащего НСО3- , что приводит к нейтрализации НСl желудочного сока и ингибированию пепсина (рН резко возрастает от 1,5-2,0 до 7,0).
Поступление пептидов в тонкий кишечник вызывает секрецию холецистокинина, который стимулирует выделение панкреатических ферментов с оптимумом рН 7,5 – 8,0. Под действием ферментов поджелудочной железы и клеток кишечника завершается переваривание белков.
Под влиянием протеолитических ферментов образуются аминокислоты, которые всасываются в кишечнике, либо диффузно, либо путем активного транспорта.
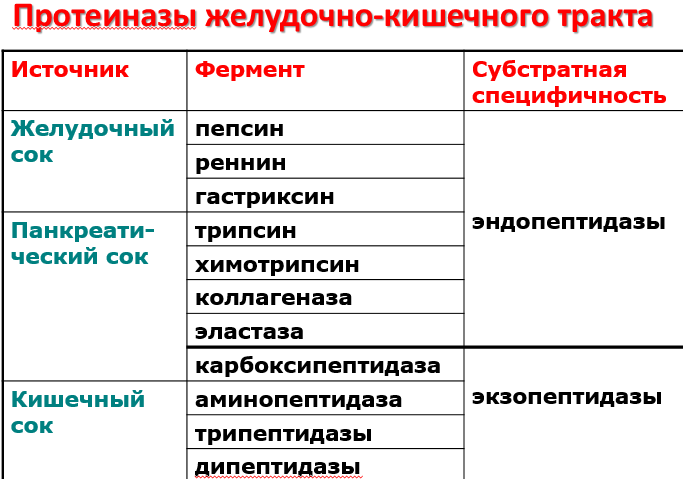
Протеиназы пищеварительного тракта (общая характеристика и классификация)
Ферменты, переваривающие белки (гидролизующие пептидные связи), называются протеиназы (пептидазы, протеазы, протеолитические ферменты)
Катепсины – лизосомальные протеиназы, обеспечивающие распад тканевых (собственных) белков, рН оптимум их лежит в кислой среде
Для протеолитических ферментов характерно:
– выделяются железами пищеварительной системы в неактивном состоянии (в форме проферментов),
– имеют единый механизм активации – частичный протеолиз – отщепление одного или нескольких пептидов от молекулы с образованием активного фермента,
– наличие субстратной специфичности,
– независимость действия.
П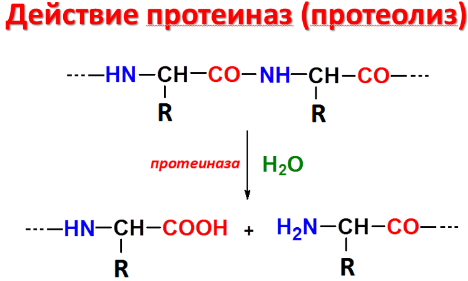
 ротеиназы
ЖКТ
ротеиназы
ЖКТ
Эндопептидазы
(синтезируются в неактивной форме)
Пепсин;
Реннин;
Гастриксин;
Трипсин;
Химотрипсин;
Эластаза.
Экзопептидазы
Карбоксипептидазы А и В;
Аминопептидазы;
Дипептидазы;
Трипептидазы.
Возрастная характеристика процессов переваривания и всасывания белков
1. Потребность в белке у детей выше, чем у взрослых, поскольку белок расходуется в этот период жизни в основном на пластические нужды, обусловленные интенсивным ростом и процессами самообновления тканей. Так, суточная потребность в зависимости от возраста: Новорожденный – 2,2 г/кг массы тела Грудной – 2,9 г/кг Дошкольник – 2,0 г/кг Школьник – 1,5-2,0 г/кг Взрослый – 1,0-1,5 г/кг
2. У ребенка выше потребность в незаменимых, особенно остроде-фицитных, аминокислотах (МЕТ, ЛЕЙ, ТРИ).
3. Дети более чувствительны к голоданию, особенно белковому. При недостатке белка в пище страдает синтез антител, появляется склонность к инфекционным заболеваниям.
4. В желудочном соке новорожденных детей имеется ранняя форма пепсина (ренин), фермент створаживает молоко, задерживает казеиноген в желудке, что улучшает его переваривание.
5. Основное переваривание белков идет в тонкой кишке, но, чем моложе ребенок, тем слабей этот процесс. Активность протеиназ у ребенка низкая, с возрастом она растет.
6. Вследствие высокой проницаемости мембраны энтероцита и низкой активности протеолитических ферментов возможно всасывание нерасщепленных белковых молекул, это вызывает сенсибилизацию организма, приводит к непереносимости пищевых продуктов.
7. Высокая степень всасываемости белков: Новорожденный – 84% Грудной – 78% Дошкольник – 73% Взрослый < 70%
Ж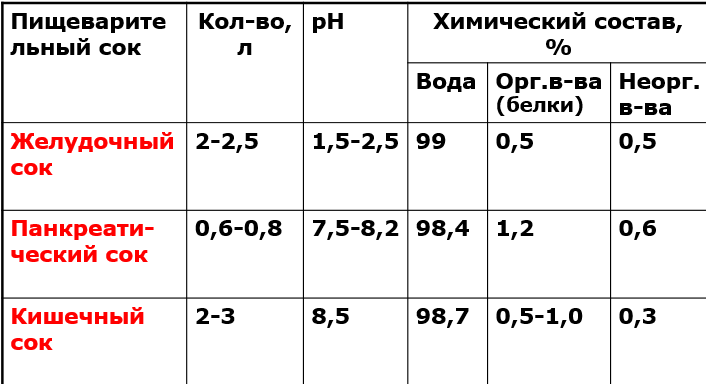 ЕЛУДОЧНЫЙ
СОК, СУТОЧНОЕ КОЛИЧЕСТВО, ХИМИЧЕСКИЙ
СОСТАВ, БИОЛОГИЧЕСКАЯ РОЛЬ.
Желудочный сок - продукт нескольких
типов клеток. Обкладочные клетки стенок
желудка образуют соляну кислоту, главные
клетки секретируют пепсиноген, добавочные
клетки муцинсодержающую слизь.
ЕЛУДОЧНЫЙ
СОК, СУТОЧНОЕ КОЛИЧЕСТВО, ХИМИЧЕСКИЙ
СОСТАВ, БИОЛОГИЧЕСКАЯ РОЛЬ.
Желудочный сок - продукт нескольких
типов клеток. Обкладочные клетки стенок
желудка образуют соляну кислоту, главные
клетки секретируют пепсиноген, добавочные
клетки муцинсодержающую слизь.
Выполняет несколько целей: - активирует пепсин из пепсиногена.
- обеспечивает химическую защиту от инородных тел. - "внутренним фактором" (фактором Касла). Этот белок связывает "внешний фактор" - витамин В12, предотвращает его разрушение и способствует всасыванию. - под действие соляной кислоты происходит денатурация белков. - содержит пепсин, расщепляющий белок.
Минеральный состав желудочного сока. Роль соляной кислоты в процессах пищеварения.
В желудочном соке в норме присутствует свободная соляная кислота
Функции соляной кислоты
активация пепсиногена
создание рН-оптимума для пепсина (1,5-2,5)
бактерицидное действие
денатурирует белки
регулирует работу привратника и стимулирует выработку секретина в кишечнике
активирует всасывание железа
обеспечивает всасывание витамина В12 (участвует в синтезе белкового фактора Кастла – антианемического)
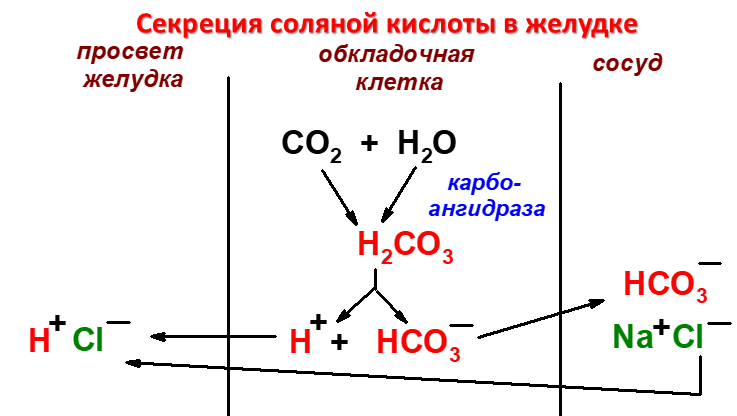
МЕХАНИЗМ СЕКРЕЦИИ СОЛЯНОЙ КИСЛОТЫ.
Основная пищеварительная функция желудка заключается в том, что в нём начинается переваривание белка. Существенную роль в этом процессе играет соляная кислота. Белки, поступающие в желудок, стимулируют выделение гистамина и группы белковых гормонов -гастринов которые, в свою очередь, вызывают секрецию НСI и профермента - пепсиногена. Источником Н+ является Н2СО3, которая образуется в обкладочных клетках желудка из СО2, диффундирующего из крови, и Н2О под действием фермента карбоангидразы (карбонатдегидра-тазы):
Н2О + СО2 → Н2СО3 → НСО3- + H+
Диссоциация Н2СО3 приводит к образованию бикарбоната, который с участием специальных белков выделяется в плазму в обмен на С1-, и ионов Н+, которые поступают в просвет желудка путём активного транспорта, катализируемого мембранной Н+/К+-АТФ-азой. При этом концентрация протонов в просвете желудка увеличивается в 106 раз. Ионы Сl- поступают в просвет желудка через хлоридный канал. Концентрация НСl в желудочном соке может достигать 0,16 М, за счёт чего значение рН снижается до 1,0-2,0. Приём белковой пищи часто сопровождается выделением щелочной мочи за счёт секреции большого количества бикарбоната в процессе образования НСl. Теперь их надо выделить в просвет желудка.
Водород - через мембранную Н/К-АТФ-азой. Хлор через ХЛОРИДНЫЙ канал.
Виды кислотности желудочного сока, определение и расчет всех видов кислотности по михаэлису.
Виды кислотности желудочного сока
Общая кислотность (НСl + прочие кислые вещества – кислые соли, органические кислоты) 40-60 ммоль/л
Соляная кислота:
Свободная 20-40 ммоль/л
Связанная (с ионогенными группами белков) – 10-12 ммоль/л
Часть соляной кислоты связывается с белками и продуктами их гидролиза, это свя-занная НСl, со свободной она образует общую НС1
В желудочном соке присутствуют органические кислоты и кислые фосфаты – это кислореагирующие продукты. Они вместе с общей соляной кислотой дают общую кислотность желудочного сока
Общая кислотность желудочного сока может как повышаться (гипера-цидное состояние), так и снижаться (гипоацидное), вплоть до исчезнове-ния (анацидное состояние). Гиперацидное состояние вызывается в основном избытком свободной соляной кислоты, т.е. возникает гиперхлоргид-рия. Снижение HCI в желудочном соке — это гипохлоргидрия, отсутствие – ахлоргидрия. Изменение кислотности желудочного сока имеет место при язвенной болезни, гастритах, при раке, злокачественном малокровии
Проферменты пищеварительных протеиназ, механизм превращения в ферменты. Субстратная специфичность протеиназ.
Биологический смысл синтеза проферментов – защита тканей пищеварительных желёз от самопереваривания (аутолиза)
Пепсиноген - белок, состоящий из одной полипептидной цепи с молекулярной массой 40 кД. Под действием НСl он превращается в активный пепсин (с оптимумом рН 1,0-2,5. В процессе активации в результате частичного протеолиза от N-конца молекулы пепсиногена отщепляются 42 аминокислотных остатка, которые содержат почти все положительно заряженные аминокислоты, имеющиеся в пепсиногене. Таким образом, в активном пепсине преобладающими оказываются отрицательно заряженные аминокислоты, которые участвуют в конформационных перестройках молекулы и формировании активного центра.
Образовавшиеся под действием НСl активные молекулы пепсина быстро активируют остальные молекулы пепсиногена (аутокатализ). Пепсин в первую очередь гидролизует пептидные связи в белках, образованные ароматическими аминокислотами (фенилаланин, триптофан, тирозин) и несколько медленнее - образованные лейцином и дикарбоновыми аминокислотами. Пепсин - эндопептидаза, поэтому в результате его действия в желудке образуются более короткие пептиды, но не свободные аминокислоты.
А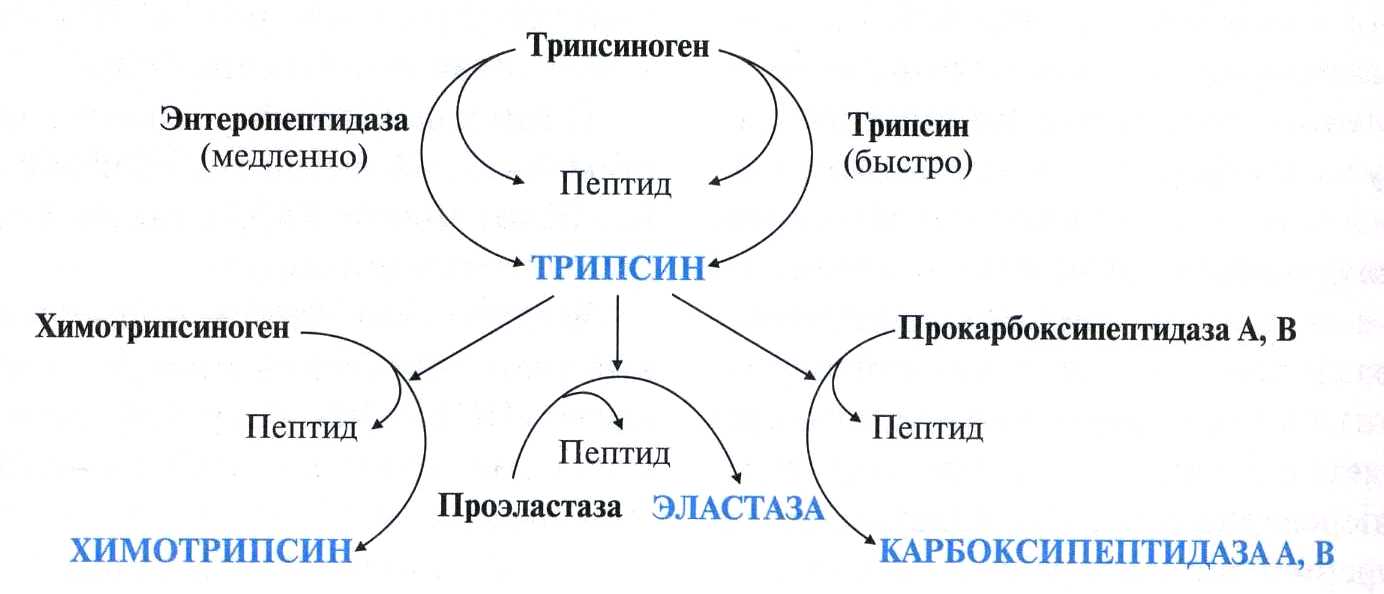 ктивация
панкреатических ферментов.
В поджелудочной железе синтезируются
проферменты ряда протеаз: трипсиноген,
химотрипсиноген, проэластаза,
прокарбоксипептидазы А и В. В кишечнике
они путём частичного протеолиза
превращаются в активные ферменты
трипсин, химотрипсин, эластазу и
карбоксипептидазы А и В.
ктивация
панкреатических ферментов.
В поджелудочной железе синтезируются
проферменты ряда протеаз: трипсиноген,
химотрипсиноген, проэластаза,
прокарбоксипептидазы А и В. В кишечнике
они путём частичного протеолиза
превращаются в активные ферменты
трипсин, химотрипсин, эластазу и
карбоксипептидазы А и В.
Активация трипсиногена происходит под действием фермента эпителия кишечника энтеропептидазы. Этот фермент отщепляет с N-конца молекулы трипсиногена гексапептид Вал-(Асп)4-Лиз. Изменение конформации оставшейся части полипептидной цепи приводит к формированию активного центра, и образуется активный трипсин. Последовательность Вал-(Асп)4-Лиз присуща большинству известных трипсиногенов разных организмов - от рыб до человека.
Специфичность действия протеаз. Трипсин преимущественно гидролизует пептидные связи, образованные карбоксильными группами аргинина и лизина. Химотрипсины наиболее активны в отношении пептидных связей, образованных карбоксильными группами ароматических аминокислот (Фен, Тир, Три). Карбоксипептидазы А и В - цинксодержащие ферменты, отщепляют С-концевые остатки аминокислот. Причём карбоксипептидаза А отщепляет преимущественно аминокислоты, содержащие ароматические или гидрофобные радикалы, а карбоксипептидаза В - остатки аргинина и лизина. Последний этап переваривания - гидролиз небольших пептидов, происходит под действием ферментов аминопептидаз и дипептидаз, которые синтезируются клетками тонкого кишечника в активной форме.
Аминопептидазы последовательно отщепляют N-концевые аминокислоты пептидной цепи. Наиболее известна лейцинаминопептидаза - Zn2+- или Мn2+-содержащий фермент, несмотря на название, обладающий широкой специфичностью по отношению к N-концевым аминокислотам.
Дипептидазы расщепляют дипептиды на аминокислоты, но не действуют на трипептиды.
В результате последовательного действия всех пищеварительных протеаз большинство пищевых белков расщепляется до свободных аминокислот.
Экзопептидазы (экзопротеиназы) — ферменты, гидролизующие белки, отщепляя аминокислоты от конца пептида: карбоксипептидазы — от C-конца, аминопептидазы — от N-конца, дипептидазы расщепляют дипептиды. Экзопептидазы синтезируются в клетках тонкого кишечника (аминопептидазы, дипептидазы) и в поджелудочной железе (карбоксипептидаза). Функционируют эти ферменты внутриклеточно в кишечном эпителии и, в небольшом количестве, в просвете кишечника.
Эндопептидазы (эндопротеиназы) — протеолитические ферменты (пепсин, трипсин, химотрипсин), расщепляющие пептидные связи внутри пептидной цепи. С наибольшей скоростью ими гидролизуются связи, образованные определёнными аминокислотами. Эндопептидазы синтезируются в виде проферментов, активируемых затем при помощи избирательного протеолиза. Таким образом клетки, секретирующие эти ферменты, защищают собственные белки от разрушения. От действия ферментов клеточную мембрану клеток животных защищает также поверхностный слой олигосахаридов —гликокаликс, а в кишечнике и желудке — слой слизи.