Материал: Курс занятий. Белки
Желудочные протеиназы: пепсин, гастриксин, их роль в переваривании белков.
Их роль в том, чтобы разделить один БОЛЬШОЙ белок на более короткие полипетиды и олигопептиды
Методы количественного определения пепсина.
Метод определения по Пятницкому
Пепсин, протеолитический фермент, способен гидролизировать белки при рН 1,5-2,5, а при рН 5,0 – створаживать казеиноген молока за счет превращения его в казеин (в основе превращения лежит также гидролиз пептидных связей). За единицу активности фермента принимают такое его количество, которое створаживает 5 мл молочно-ацетатной смеси рН 5,0 (смесь равных объемов молока и 1н. ацетатного буфера рН 5,0) при 25°С за 60 секунд. 100 единиц Пятницкого соответствует 1 мг фермента. В норме желудочный сок содержит 20-40 ед/мл (0,2-0,4 мг/мл, или 0,2-0,4 г/л) пепсина.
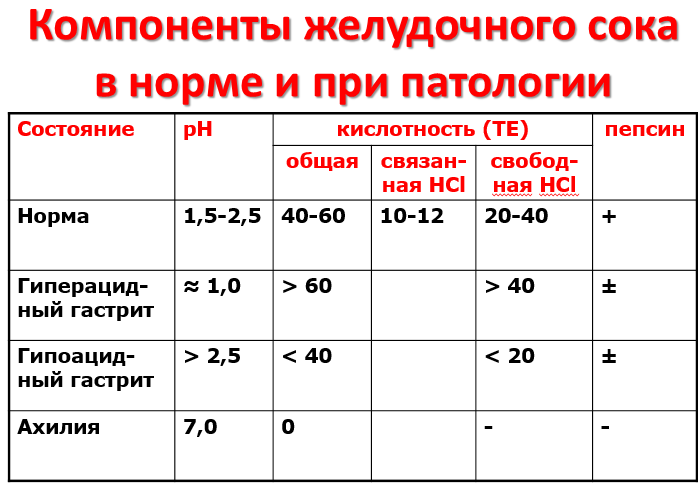
ПАТОЛОГИЧЕСКИЕ СОСТАВНЫЕ ЧАСТИ ЖЕЛУДОЧНОГО СОКА. ДИАГНОСТИЧЕСКОЕ ЗНАЧЕНИЕ
НАРУШЕНИЕ ПЕРЕВАРИВАНИЯ И ВСАСЫВАНИЯ БЕЛКОВ.
При различных заболеваниях ЖКТ в желудке нарушается выделение НСl и пепсиногена, при этом заметно снижается переваривание белков. Наиболее часто встречаются патологические изменения кислотности желудочного сока.
Повышенная кислотность (норма 40-60ТЕ) желудочного сока сопровождается изжогой, диареей и может быть симптомом язвы желудка и двенадцатиперстной кишки, гиперацидного гастрита.
Пониженная кислотность бывает при некоторых видах гастритов. Полное отсутствие НСl и пепсина (ахилия) наблюдается при атрофических гастритах.
Анацидность (рН >6) часто вызывает рак желудка.
У некоторых людей возникает иммунная реакция на прием белка, что связано со способностью к всасыванию негидролизованных коротких пептидов. Аминокислоты лишены антигенных свойств и иммунных реакций не вызывают.
У новорожденных проницаемость слизистой оболочки кишечника выше, чем у взрослых, поэтому в кровь могут поступать антитела молозива. Это усугубляется наличием в молозиве белка-ингибитора трипсина. Протеолитические ферменты в пищеварительных секретах новорожденных обладают низкой активностью. Это способствует всасыванию в кишечнике небольшого количества нативных белков, достаточного для обеспечения иммунной реакции. Подобное усиление всасывающей способности кишечника является причиной непереносимости белков пищи (молока, яиц) у взрослых людей.
При заболевании целиакии (нетропической спру) происходит нарушение клеток слизистой оболочки кишечника, где всасываются небольшие негидролизованные пептиды. Целиакия характеризуется повышенной чувствительностью к глютену (белок клейковины зерен злаков), который оказывает токсическое действие на слизистую тонкой кишки, что приводит к ее патологическим изменениям и нарушению всасывания.
Диагностическое значение: Общая кислотность желудочного сока может как повышаться (гипера-цидное состояние), так и снижаться (гипоацидное), вплоть до исчезнове-ния (анацидное состояние). Гиперацидное состояние вызывается в основ-ном избытком свободной соляной кислоты, т.е. возникает гиперхлоргид-рия. Снижение HCI в желудочном соке — это гипохлоргидрия, отсутствие – ахлоргидрия. Изменение кислотности желудочного сока имеет место при язвенной болезни, гастритах, при раке, злокачественном малокровии.
Составная часть |
Единицы СИ |
Азот: |
|
небелковый |
14,3—34,3 ммоль/л |
мочевины и аммиака |
4,99—9,99 ммоль/л |
аминокислот |
1,43—5,7 ммоль/л |
Хлориды |
155,1 ммоль/л |
Свободная хлористоводородная кислота |
20 ммоль/л |
Мочевая кислота |
47,6—118,9 мкмоль/л |
Калий |
5,6—35,3 мэкв/л (ммоль/л) |
Натрий |
31,3—189,3 мэкв/л (ммоль/л) |
Общая кислотность |
40-60 ммоль/л |
Свободная соляная кислота |
20-40 ммоль/л |
Связанная соляная кислота |
10 – 12 ммоль/л |
Пепсин |
0,2 – 0,4 мг/мл |
 ИОХИМИЧЕСКИЙ
АНАЛИЗ ЖЕЛУДОЧНОГО СОКА.
ИОХИМИЧЕСКИЙ
АНАЛИЗ ЖЕЛУДОЧНОГО СОКА.
Химический состав панкреатического и кишечного соков. Роль панкреатических и кишечных протеиназ в переваривании белков.
Дуоденальный сок - пищеварительный сок двенадцатиперстной кишки, состоящий из секрета поджелудочной железы, желчи, сока кишечных крипт и дуоденальных желез
Панкреатический сок имеет высокую концентрацию бикарбонатов, которые обусловливают его щелочную реакцию. Его рН колеблется от 7,5 до 8,8. В соке содержатся хлориды натрия, калия и кальция, сульфаты и фосфаты. Вода и электролиты выделяются в основном центроацинарными и эпителиальными клетками выводах протоков. В состав сока входит и слизь, которая вырабатывается бокаловидными клетками главного протока поджелудочной железы. Панкреатический сок богат ферментами, осуществляющими гидролиз белков, жиров и углеводов. Они вырабатываются ацинарными панкреацитами.
Протеолитические ферменты (трипсин, химотрипсин, эластаза, карбок-сипептидазы А и В) выделяются панкреацитами в неактивном состоянии, что предотвращает самопереваривание клеток.
Трипсин. Трипсиноген и трипсин получены в кристаллическом виде, полностью расшифрована их первичная структура и известен молекулярный механизм превращения профермента в активный фермент. В опытах in vitro превращение трипсиногена в трипсинкатализируют не только энтеропептидаза и сам трипсин, но и другие протеиназы и ионы Са2+.
Активирование трипсиногена химически выражается в отщеплении с N-конца полипептидной цепи 6 аминокислотных остатков (Вал–Асп– Асп–Асп–Асп–Лиз) и соответственно в укорочении полипептидной цепи.
Следует подчеркнуть, что в этом небольшом, казалось бы, химическом процессе – отщепление гексапептида от предшественника – заключено важное биологическое значение, поскольку при этом происходят формирование активного центра и образование трехмерной структуры трипсина, а известно, что и белки биологически активны только в своей нативной трехмерной конформации. В том, что трипсин, как и другие протеиназы, вырабатывается в поджелудочной железе в неактивной форме, также имеется определенный физиологический смысл, поскольку в противном случае трипсин мог бы оказывать разрушающее протеолитическое действие не только на клетки самой железы, но и на другие ферменты, синтезируемые в ней (амилаза, липаза и др.). В то же время поджелудочная железа защищает себя еще одним механизмом – синтезом специфического белка ингибитора панкреатическоготрипсина. Этот ингибитор оказался низкомолекулярным пептидом (мол. масса 6000), который прочно связывается с активными центрами трипсина и химотрипсина, вызывая обратимое их ингибирование. В поджелудочной железе синтезируется также α1-антипротеиназа (мол. масса 50000), которая преимущественно инги-бирует эластазу.
При остром панкреатите, когда трипсин и другие ферменты из пораженной поджелудочной железы «вымываются» в кровь, уровень их вкрови соответствует размерам некротического участка. В этом случае определение активности трипсина в сыворотке крови является надежным ферментным тестом при диагностике острого панкреатита. Следует отметить, что субстратная специфичность трипсинаограничена разрывом только тех пептидных связей, в образовании которых участвуют карбоксильные группы лизина и аргинина.
Химотрипсин. В поджелудочной железе синтезируется ряд химотрип-синов (α-, β- и π-химотрипсины) из двух предшественников – химотрипсиногена А и химотрипсиногена В. Активируются проферменты в кишечнике под действием активного трипсина ихимотрипсина. Полностью раскрыта последовательность аминокислот химотрипсиногена А, во многом сходная с последовательностьюаминокислот трипсина. Молекулярная масса его составляет примерно 25000. Он состоит из одной полипептидной цепи, содержащей 246 аминокислотных остатков. Активация профермента не сопряжена с отщеплением большого участка молекулы. Получены доказательства, что разрыв одной пептидной связи между аргинином и изолейцином в молекуле химотрипсиногена А под действием трипсина приводит к формированию π-химотрипсина, обладающего наибольшей ферментативной активностью. Последующее отщепление дипеп-тида Сер–Арг приводит к образованию δ-химотрипсина. Аутокаталити-ческий процесс активирования, вызванный химотрипсином, сначала способствует формированию неактивного промежуточного неохимотрипсина, который под действием активного трипсина превращается в α-химотрип-син; этот же продукт образуется из δ-химотрипсина, но под действием активного химотрипсина. Таким образом, благодаря совместному перекрестному воздействию химотрипсина и трипсина из химотрипсиногена образуются разные химо-трипсины, различающиеся как ферментативной активностью, так и некоторыми физико-химическими свойствами, в частности электрофорети-ческой подвижностью. Следует отметить, что химотрипсин обладает более широкой субстратной специфичностью, чем трипсин. Он катализирует гидролиз не только пептидов, но и эфиров, гидроксаматов, амидов и других ацилпроизводных, хотя наибольшую активность химотрипсин проявляет по отношению к пептидным связям, в образовании которых принимают участие карбоксильные группы ароматических аминокислот:фенилаланина, тирозина и триптофана.
Эластаза. В поджелудочной железе синтезируется еще одна эндопеп-тидаза – эластаза – в виде проэластазы. Превращениепрофермента в эластазу в тонкой кишке катализируется трипсином. Название фермент получил от субстрата эластина, который он гидролизует. Эластин содержится в соединительной ткани и характеризуется наличием большого числа остатков глицина и серина. Эластаза обладает широкой субстратной специфичностью, но предпочтительнее гидролизует пептидные связи, образованныеаминокислотами с небольшими гидрофобными радикалами, в частности глицином, аланином и серином. Интересно, что ни трипсин, нихимотрипсин не гидролизуют пептидные связи молекулы эластина, хотя все три фермента, включая эластазу, содержат сходные участкиаминокислотных последовательностей и одинаковые места положения дисульфидных мостиков, а также имеют в активном центре один и тот же ключевой остаток серина, что подтверждают опыты с ингибированием всех трех ферментовдиизопропилфторфосфатом, химически связывающим ОН-группу серина. Высказано предположение, что все три эндопептидазы поджелудочной железы: трипсин, химотрипсин и эластаза,– возможно, имеют один и тот же общий предшественник и чтоспецифичность активного фермента в основном определяется конформационными изменениями профермента в процессе активирования.
Экзопептидазы. В переваривании белков в тонкой кишке активное участие принимает семейство экзопептидаз. Одни из них – карбоксипеп-тидазы – синтезируются в поджелудочной железе в виде прокарбоксипеп-тидазы и активируются трипсином в кишечнике; другие – аминопептидазы – секретируются в клетках слизистой оболочки кишечника и также активируются трипсином.
Карбоксипептидазы. Подробно изучены две карбоксипептидазы – А и В, относящиеся к металлопротеинам и катализирующие отщепление от полипептида С-концевых аминокислот. Карбоксипептидаза А разрывает преимущественно пептидные связи, образованные концевыми ароматическими аминокислотами, а карбоксипептидаза В – связи, в образовании которых участвуют С-концевые лизин и аргинин. Очищенный препарат карбокси-пептидазы А обладает бифункциональной активностью – пептидазной и эстеразной и содержит ион Zn2+(один атом на 1 моль фермента). При замене ионов Zn2+на ионы Са2+ полностью утрачивается пепти-дазная активность, но усиливается исходная эстеразная активность, хотя
при этом существенных изменений в третичной структуре фермента не отмечается.
Аминопептидазы. В кишечном соке открыты два фермента – аланин-аминопептидаза, катализирующая преимущественно гидролизпептидной связи, в образовании которой участвует N-концевой аланин, и лейцин-аминопептидаза, не обладающая строгой субстратнойспецифичностью и гидролизующая пептидные связи, образованные любой N-концевой аминокислотой. Оба фермента осуществляют ступенчатое отщепление аминокислот от N-конца полипептидной цепи.
Дипептидазы. Процесс переваривания пептидов, их расщепление до свободных аминокислот в тонкой кишке завершают дипептидазы. Среди дипептидаз кишечного сока хорошо изучена глицилглицин-дипептидаза, гидролизующая соответствующий дипептид до двухмолекул глицина. Известны также две другие дипептидазы: пролил-дипептидаза (пролиназа), катализирующая гидролиз пептидной связи, в образовании которой участвует СООН-группа пролина, и пролин-дипептидаза (пролидаза), гидроли-зующая дипептиды, в которых азот пролина связан кислотно-амидной связью.
Б иохимические механизмы регуляции пищеварения, гормоны желудочно-кишечного тракта. Всасывание аминокислот.
Конечными продуктами гидролитического расщепления белков являются свободные аминокислоты, подвергающиеся активному транспорту через мембрану энтероцита в кровь.
Аминокислоты, образовавшиеся при переваривании белков, быстро всасываются в кишечнике. Транспорт их осуществляется двумя путями: через воротную систему печени, ведущую прямо в печень, и по лимфатическим сосудам, сообщающимся с кровью через грудной лимфатический проток. Максимальная концентрация аминокислот в крови достигается через 30- 50 мин после приёма белковой пищи (углеводы и жиры замедляют всасывание аминокислот). Всасывание L-аминокислот (но не D-изомеров) - активный процесс, требующий затраты энергии. Аминокислоты переносятся через кишечную стенку от слизистой её поверхности в кровь. Перенос через щёточную кайму осуществляется целым рядом переносчиков, многие из которых действуют при участии Na+-зависимых механизмов симпорта, подобно переносу глюкозы.
В настоящее время известно по крайней мере пять специфических транспортных систем, каждая из которых функционирует для переноса определённой группы близких по строению аминокислот:
• нейтральных, с короткой боковой цепью (аланин, серин, треонин);
• нейтральных, с длинной или разветвлённой боковой цепью (валин, лейцин, изолей-цин);
• с катионными радикалами (лизин, аргинин);
• с анионными радикалами (глутаминовая и аспарагиновая кислоты);
• иминокислот (пролин, оксипролин). Причём к числу Na+-зависимых относятся
переносчики аминокислот, входящих в первую и пятую группы, а также переносчик метионина. Независимые от Na+ переносчики специфичны для некоторых нейтральных аминокислот (фенилаланин, лейцин) и аминокислот с катионными радикалами (лизин).
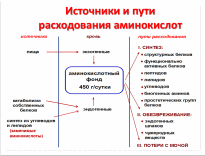
Общая схема источников и путей расходования аминокислот в тканях. Экзогенный и эндогенный пул аминокислот
Катаболизм аминокислот – внутриклеточный процесс, в котором выделяют два варианта:
1. Общие пути катаболизма, в результате которых все аминокислоты могут первично терять α-аминогруппу (дезаминирование, трансами-нирование) или α-карбоксильную группу (декарбоксилирование).
 2.
Индивидуальные пути катаболизма, при
которых имеют место пе-ричные превращения
аминокислоты по радикалу (трансметилирова-ние,
де- и транссульфирование, гидроксилирование
и др.).
2.
Индивидуальные пути катаболизма, при
которых имеют место пе-ричные превращения
аминокислоты по радикалу (трансметилирова-ние,
де- и транссульфирование, гидроксилирование
и др.).
Пути использования аминокислот после всасывания:
Синтез специфических белков тканей, плазмы крови, ферментов, гормонов.
Синтез углеводов (глюконеогенез).
Синтез липидов.
Синтез гистамина, серотонина, креатина, порфиринов, холина, адреналина, пуриновых, пиримидиновых нуклеотидов.
Синтез мочевины.
Оставшиеся неиспользованные аминокислоты подвергаются распаду с выделением энергии (10-15%).
Общие пути распада аминокислот:
Декарбоксилирование;
Трансаминирование;
Дезаминирование;
Конечными продуктами катаболизма аминокислот являются аммиак, вода и углекислый газ.
А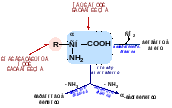 ммиак
– токсичное
соединение, особенно для центральной
нервной системы. Это судорожный яд,
требующий постоянного обезвреживания.
Механизм токсического действия аммиака
сводится к следующему:
ммиак
– токсичное
соединение, особенно для центральной
нервной системы. Это судорожный яд,
требующий постоянного обезвреживания.
Механизм токсического действия аммиака
сводится к следующему:
1. на обезвреживание аммиака расходуется α-кетоглутаровая кислота, это приводит к выключению ее из цикла трикарбоновых кислот, блокаде ЦТК и развитию гипоэнергетического состояния,
2. повышенная концентрация аммиака в крови (гипераммониемия) приводит к нарушению кислотно-основного состояния, развивается алкалоз,