Материал: Контроль содержания металлов электрохимическими методами в сточных водах гальванических цехов машиностроительных предприятий
Контроль содержания металлов электрохимическими методами в сточных водах гальванических цехов машиностроительных предприятий
ВВЕДЕНИЕ
металл токсикологический сточный гальванический
В Республике Беларусь гальваническое производство функционирует более чем на 140 предприятиях. Наибольшее распространение получили цинковые, никелевые, фосфатные, хромовые, медные и другие покрытия. В общем объеме производства гальванических покрытий более 80 % занимает цинкование как наиболее дешевый и надежный способ защиты от коррозионного разрушения металлических конструкций.
Гальванические (электрохимические) покрытия являются одним из самых распространенных методов защиты изделий от коррозии, придания им необходимых эксплуатационных характеристик и декоративных свойств. Гальванические технологии широко применяются в машиностроении, приборостроении, авиационной, электронной и радиотехнической промышленности, в других областях. Выбор способа нанесения гальванопокрытия определяется его видом и толщиной, требованиями к свойствам, размерами и формой обрабатываемых деталей, а также применяемыми подготовительными и заключительными операциями обработки.
В процессах обработки поверхности с
цельюпридания ей антикоррозионных и декоративныхсвойств используются
разнообразные реагенты,содержащие тяжелые металлы. Они входят в состав побочных
продуктов этого производства -твердых и жидких отходов, сточных вод, выбросов в
атмосферу. Также все гальванотехнические процессы сопряжены с большим
водопотреблением, а следовательно, и с большим количеством образующихся сточных
вод. В результате предприятия, в составе которых функционируют гальванические
цехи (участки), являются основными источниками поступления токсичных тяжелых
металлов в водные объекты. При этому становленные нормативы допустимых
концентраций по ионам тяжелых металлов для сточных вод, отводимых в
канализационные сети, часто не выполняются, что затрудняет работу городских
очистных сооружений. При очистке сточных вод гальванических производств на
локальных очистных сооружениях образуются осадки,которые относятся к отходам
3-4 классов опасности. В процессе применения технологических растворов
образуются шламы, которые практически не используются и хранятся на площадках
предприятий. Поэтому контроль содержания металлов в сточных водах
гальванических цехов является актуальным на сегодняшний день.
1. МЕТАЛЛЫ В СТОЧНЫХ ВОДАХ ГАЛЬВАНИЧЕСКИХ ЦЕХОВ
МАШИНОСТРОИТЕЛЬНЫХ ПРЕДПРИЯТИЙ
При производстве машиностроительной продукции многие предприятия для повышения коррозионной стойкости и улучшения внешнего вида металлических деталей наносят на них гальванические покрытия из водных растворов или расплавов солей металлов.
Крупнейшие предприятия Республики Беларусь, где функционирует гальваническое производство: РУП «Белорусский металлургический завод» (Жлобин), РУП«Гомельский завод литья и нормалей», ОАО «Минский подшипниковый завод», РУП «Гомсельмаш», РУП «БелАЗ» (Жодино), ПРУП «Минский автомобильный завод», РУП «Минский тракторный завод», ЗАО «Атлант»(Минск), РУПП «Витязь» (Витебск) и др. Наибольшее распространение получили цинковые, хромовые, никелевые, медные и кадмиевые покрытия.
Воздействие на окружающую среду гальванического производства в значительной степени зависит от организации водного хозяйства, эффективности работы очистных сооружений и использования образующихся в процессепроизводства осадков и шламов.В гальваническом производстве неизбежно образуются токсичные сточные воды, которые необходимо обезвреживать.
Сточные воды гальванических производств содержат такие металлы, как хром, никель, свинец, медь, кадмий, цинк, олово и др. Длительное их поступление в организм с водой или пищей даже в незначительных дозах приводит в результате накопления в органах и тканях к нарушению функционирования центральной нервной системы, внутренних органов, эндокринной системы и других жизненно важных систем организма.
По данным Государственного водного кадастра в
водные объекты Беларуси в 2013 г. отведено 974 млн м3 сточных вод, среди
которых, как и ранее, количественно преобладали нормативно-очищенные воды.
Вторую позицию занимали сточные воды, сбрасываемые без очистки(табл.1), объем
которых из года в год увеличивался. Однако в 2013 г. их количество по сравнению
с предыдущим годом уменьшилось на 28 млн м3 (рис. 1).
Таблица 1 - Отведение различных категорий сточных вод в водные объекты в областях Беларуси и г.Минске в 2013 г., млн м3
|
Область, |
Всего |
|
из них |
|
|
|
|
недостаточно |
не требующих |
нормативно- |
|
|
|
очищенных |
очистки |
очищенных |
|
1 |
2 |
3 |
4 |
5 |
|
Всего |
974 |
2,92 |
317 |
654 |
|
Брестская |
176 |
0,09 |
104 |
72 |
|
Витебская |
128 |
0,08 |
40 |
88 |
|
Гомельская |
124 |
0,09 |
27 |
98 |
|
Гродненская |
89 |
0,05 |
7 |
82 |
|
Минская |
183 |
2,11 |
118 |
62 |
|
Могилевская |
99 |
9,49 |
12 |
87 |
|
г.Минск |
174 |
0,00 |
9 |
165 |
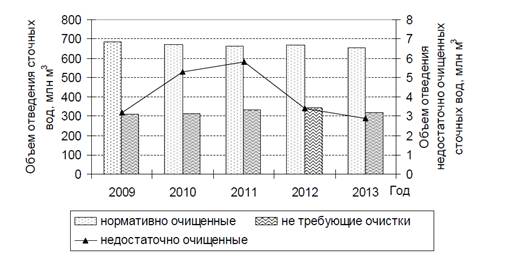 Рисунок 1 -
Динамика отведения сточных вод в водные объекты
Рисунок 1 -
Динамика отведения сточных вод в водные объекты
В 2013 г. в целом для страны количество сточных вод,содержащих загрязняющие вещества, составило 890 млн м3 и уменьшилось по сравнению с 2012 г. на 59 млн м3.
Количество загрязняющих веществ, сброшенных в составе сточных вод в водные объекты, представлено в таблице 2. Следует отметить, что в последние годы отмечается тенденция к уменьшению объемов сброса соединений азота.Так, по сравнению с 2012 г. их суммарное поступление в водные объекты страны сократилось на 0,5 тыс.т.
Общее количество сброшенных в водные объекты в2013 г. металлов оказалось наименьшим за пятилетний период,а по сравнению с 2012 г. сократилось на 128 т. При этом основное количество (381,7 т) приходится на железо, цинк составляет 24,75 т, никель - 5,66 и хром - 3,32 т.
Свинец содержится в сточных водах Гомеля (0,35 т), Минска (0,82), Могилева (0,22), Минской (0,1) и Витебской (0,1 т) областей.
При этом по сравнению с2012 г. его сброс со
сточными водами Минска увеличился в2,6 раза, Могилева и Гомеля напротив
уменьшился на 0,18 и 0,05 т соответственно, в Минской и Витебской области
остался на прежнем уровне.
Таблица 2 - Сброс загрязняющих веществ в составе сточных вод в Беларуси в 2009-2013 гг.
|
Показатель |
Раз- |
|
|
Год |
|
|
|
|
мерность |
2009 |
2010 |
2011 |
2012 |
2013 |
|
Органические |
|
8 |
8 |
8 |
9 |
8 |
|
вещества (БПК5) |
тыс.т |
|
|
|
|
|
|
Нефть и нефтепро- |
|
|
|
|
|
|
|
дукты в растворен- |
тыс.т |
0,13 |
0,12 |
0,11 |
0,12 |
0,10 |
|
ном и эмульгирован- |
|
|
|
|
|
|
|
ном состоянии |
|
|
|
|
|
|
|
Взвешенные |
тыс.т |
13 |
13 |
13 |
12 |
14 |
|
Сульфаты |
тыс.т |
63 |
56 |
60 |
61 |
58 |
|
Хлориды |
тыс.т |
73 |
65 |
71 |
75 |
72 |
|
Аммонийный азот |
тыс.т |
5,40 |
5,50 |
5,90 |
5,70 |
5,30 |
|
Нитритний азот |
тыс.т |
0,19 |
0,16 |
0,20 |
0,18 |
0,15 |
|
Нитратный азот |
тыс.т |
3,70 |
3,50 |
3,40 |
3,16 |
|
|
Медь |
т |
6,70 |
5,00 |
6,20 |
7,00 |
5,80 |
|
Другие металлы (же- |
|
|
|
|
|
|
|
лезо общее, цинк, |
т |
421 |
494 |
516 |
543 |
415 |
|
никель, хром общий) |
|
|
|
|
|
|
Кобальт (0,17 т) поступал в реки со сточными
водами Гомеля, молибден (3,76) - Витебской области, фториды (10,47)
сбрасывались со сточными водами Гомеля, фенолы - со сточными водами Гомельской
области (1,62), а также городов Гродно (0,26) и Могилева (0,06 т). Среди указанных
загрязняющих веществ, следует обратить внимание на рост в 2013 г в сравнении с
прошлым годом сброса фторидов на 2,21 т[1]
. ХИМИЧЕСКАЯ И ТОКСИКОЛОГИЧЕСКАЯ ХАРАКТЕРИСТИКА
МЕДИ, НИКЕЛЯ, КОБАЛЬТА, ЦИНКА
.1 Химическая и токсикологическая характеристика
кобальта
В соединениях кобальт проявляет переменную валентность. В простых соединениях наиболее устойчив Со(П), в комплексных - Со(Ш). Для Со(I) и Co(IV) получены только немногочисленные комплексные соединения. При обыкновенной температуре компактный кобальт стоек против действия воды и воздуха. Мелко раздробленный кобальт, полученный восстановлением его оксида водородом при 250 °С ,на воздухе самовоспламеняется, превращаясь в СоО. Компактный кобальт начинает окисляться на воздухе выше 300 °С; при красном калении он разлагает водяной пар. С галогенами кобальт легко соединяется при нагревании, образуя галогениды СоХ2. При нагревании кобальт взаимодействует с S, Se, P, As, Sb, С, Si, В, причем состав получающихся соединений иногда не удовлетворяет указанным выше валентным состояниям (например, Со2Р, Co2As, CoSb2, Со3С, CoSi3). В разбавленных соляной и серной кислотах кобальт медленно растворяется с выделением водорода и образованием соответственно хлорида СоCо2 и сульфата CoSO4. Разбавленная азотная кислота растворяет кобальт с выделением оксидов азота и образованием нитрата Co(NO3)2. Едкие щелочи осаждают из растворов солей Со2+ синий гидроксид Со(ОН)2, которая постепенно буреет вследствие окисления кислородом воздуха до Со(ОН)3.
Из простых соединений Со(IП) известны лишь немногие. При действии фтора на порошок Со или СоCl2 при 300-400 °С образуется коричневый фторид CoF3. Комплексные соединения Со(Ш) весьма устойчивы и получаются легко. Например, KNO2 осаждает из растворов солей Со (П), содержащих СН3СООН, желтый труднорастворимый гексанитрокобальтат (III) калия K3[Co(NO2)6]. [11]
В природные воды соединения кобальта попадают в результате процессов выщелачивания их из медноколчедановых и других руд, из почв при разложении организмов и растений, а также со сточными водами металлургических, металлообрабатывающих и химических заводов. Некоторые количества кобальта поступают из почв в результате разложения растительных и животных организмов.
Соединения кобальта в природных водах находятся в растворенном и взвешенном состоянии, количественное соотношение между которыми определяется химическим составом воды, температурой и значениями рН. Растворенные формы представлены в основном комплексными соединениями, в т.ч. с органическими веществами природных вод. Соединения двухвалентного кобальта наиболее характерны для поверхностных вод. В присутствии окислителей возможно существование в заметных концентрациях трехвалентного кобальта.
Кобальт относится к числу биологически активных элементов и всегда содержится в организме животных и в растениях. С недостаточным содержанием его в почвах связано недостаточное содержание кобальта в растениях, что способствует развитию малокровия у животных (таежно-лесная нечерноземная зона). Входя в состав витамина В12, кобальт весьма активно влияет на поступление азотистых веществ, увеличение содержания хлорофилла и аскорбиновой кислоты, активизирует биосинтез и повышает содержание белкового азота в растениях. Вместе с тем повышенные концентрации соединений кобальта являются токсичными.
В речных незагрязненных и слабозагрязненных водах его содержание колеблется от десятых до тысячных долей миллиграмма в 1 дм3, среднее содержание в морской воде 0.5 мкг/дм3.
ПДКв составляет 0.1 мг/дм3, ПДКвр 0.01 мг/дм3 .
[10]
2.2 Химическая и токсикологическая характеристика
меди
Образуя химические соединения, атом меди может отдавать один, два или три электрона, проявляя степень окисления соответственно +1, +2 и +3. При этом наиболее устойчивыми являются соединения меди (II), а наименее устойчивыми - соединения меди (III).
Медь относится к малоактивным металлам. Стандартный электродныйпотенциал меди равен +0,34 В, что определяет ее место в ряду стандартных электродных потенциалов: оно находится правее водорода. При обычных условиях она не взаимодействует с водой, растворами щелочей, соляной и разбавленной серной кислотой.
Однако в кислотах-сильных окислителях (например, азотной и концентрированной серной)-медь растворяется.
Как малоактивный металл медь обладает достаточно высокой стойкостью к коррозии, влажной атмосфере, содержащей углекислый газ, медь покрывается зеленоватым налетом карбоната меди.В большинстве известных соединений медь проявляет степень окисления + 2.
Соединения меди (II) - оксид СuО и гидроксид Сu(ОН)2-довольно устойчивы. Этот гидроксид амфотерен,хорошо растворяется в кислотахи в концентрированных щелочах.
Гидроксид меди (II) - труднорасворимое в воде вещество голубого цвета. Принагреванииразлагается,образуя оксид меди (II) черного цвета.
Темный цвет окисленных медных изделий обусловлен наличием на их поверхности этого оксида. Для ионов меди (II) Сu2+ характерно образование комплексных соединений, например K2[Cu(CN)4]-тетрацианокупрат (II) калия.
Из других комплексных соединений меди (II) отметим соединение с аммиаком. Если к раствору хлорида меди (II) прилить небольшое количество раствора аммиака, то выпадет осадок гидроксида меди (II).
Если добавить избыток аммиака, то гидроксид растворится с образованием комплексного соединения темно-синей окраски, характерной для аммиачного комплекса меди. Эта реакция является качественной на ион меди (II).
Соединения меди (III), например Cu203 или KCu02, встречаются редко, они малоустойчивы. Устойчивость соединений меди (I) выше, однако и они в водных растворах легко подвергаются диспропорционированию (реакции самоокисления-самовосстановления). [12]