Материал: КФ №2
где
![]() –
порядковый номер элемента в таблице
Менделеева, для водорода
–
порядковый номер элемента в таблице
Менделеева, для водорода
![]() =1;
=1;
е – заряд
электрона;
![]() – электрическая постоянная.
– электрическая постоянная.
Уравнение движения электрона в классической механике в этом случае имеет вид:
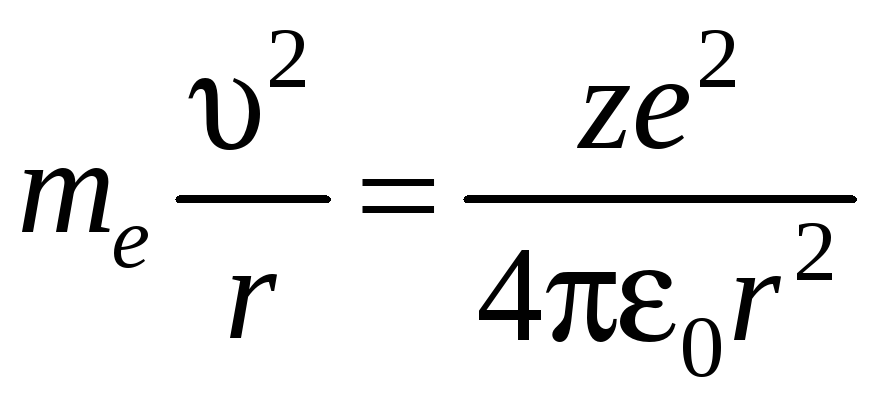 .
(4)
.
(4)
Исключив
![]() из уравнений (3) и (4), получим выражение
для радиусов допустимых орбит (боровских
орбит):
из уравнений (3) и (4), получим выражение
для радиусов допустимых орбит (боровских
орбит):
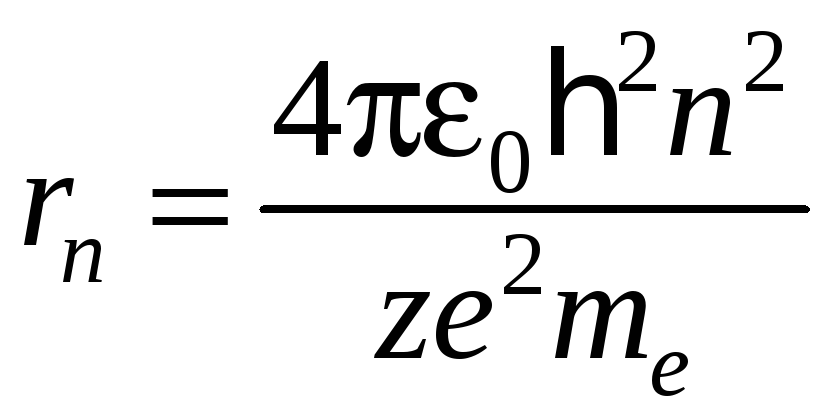 .
(5)
.
(5)
Радиус первой орбиты водородного атома называется боровским радиусом. Его значение равно:
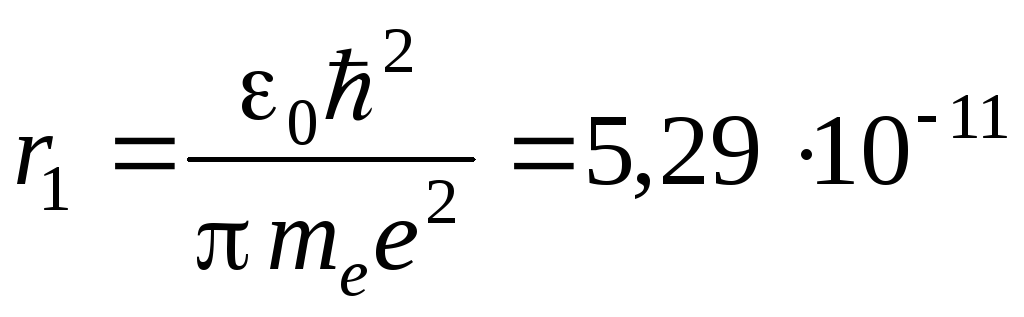 ,
м. (6)
,
м. (6)
Внутренняя энергия атома слагается из кинетической энергии электрона (ядро неподвижно) и энергии взаимодействия электрона с ядром
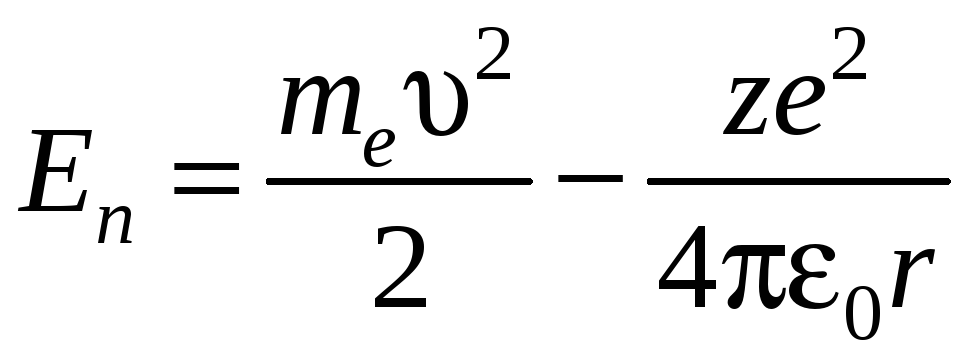 .
(7)
.
(7)
Из формулы (4) следует, что
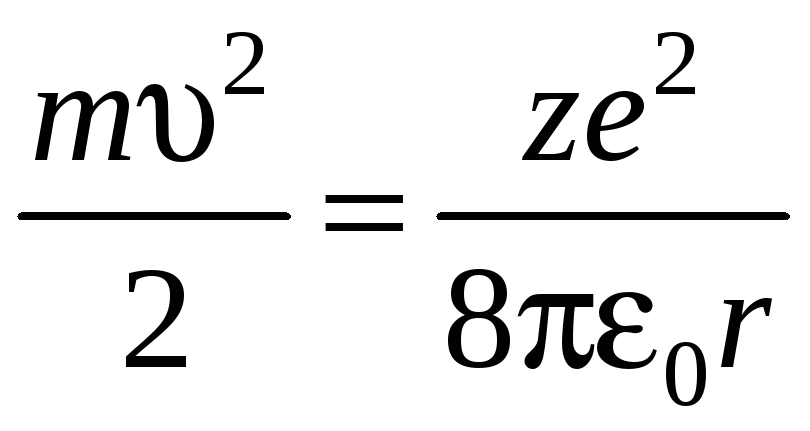 .
.
Следовательно,
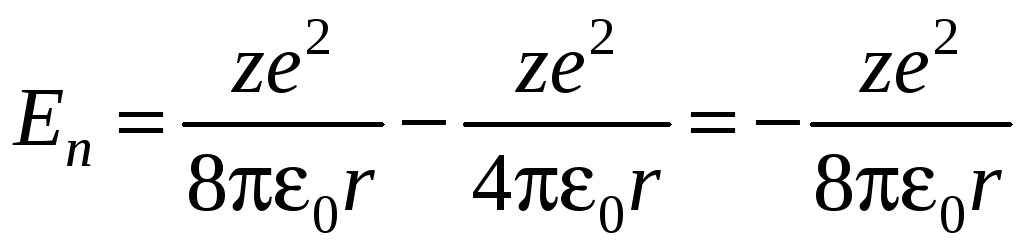 .
(8)
.
(8)
Подставив в
(8) значение
![]() из формулы (5), найдем дозволенные значения
внутренней энергии атома:
из формулы (5), найдем дозволенные значения
внутренней энергии атома:
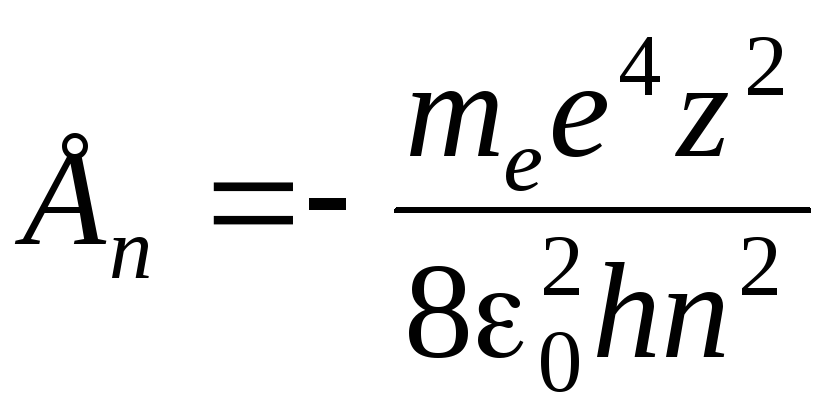 (n = 1, 2, 3 …).
(9)
(n = 1, 2, 3 …).
(9)
Схема энергетических уровней приведена на рис. 1.
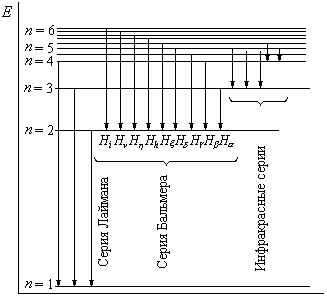
Рис.1
При переходе атома
водорода (![]() =1)
из состояния
=1)
из состояния
![]() в состояние
в состояние
![]() излучается, согласно формулам (1) и (9),
фотон энергии:
излучается, согласно формулам (1) и (9),
фотон энергии:
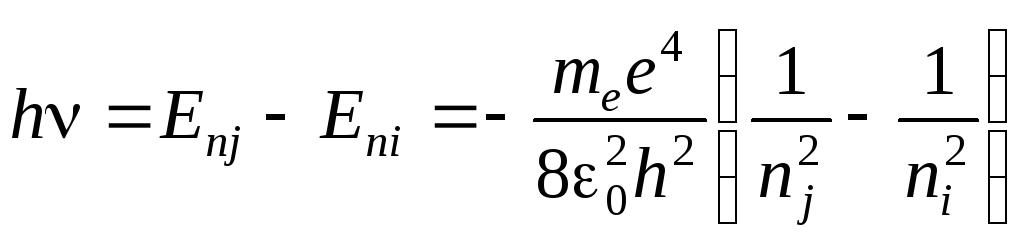 .
.
Частота испущенного фотона:
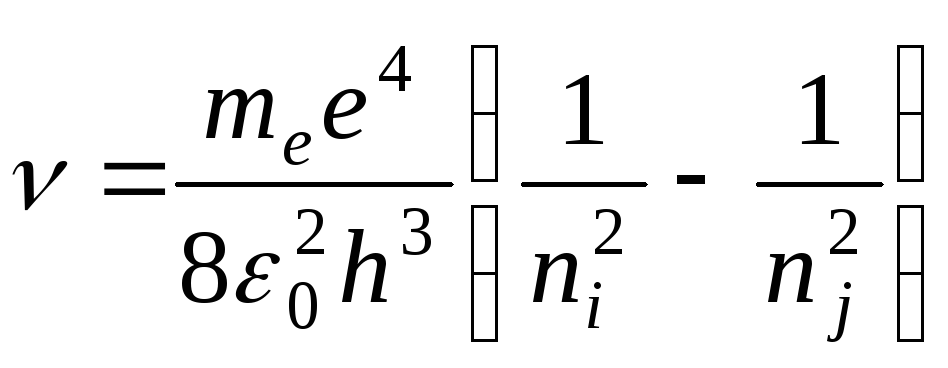 .
(10)
.
(10)
Учитывая, что
![]() ,
получим:
,
получим:
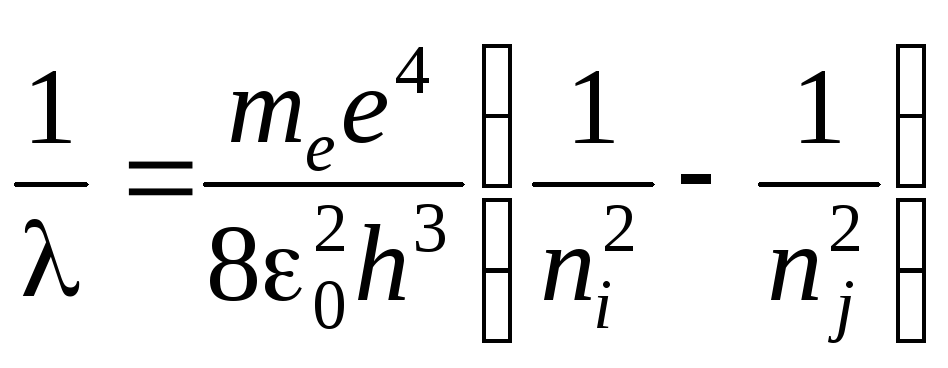 .
(11)
.
(11)
Получена обобщенная формула Бальмера, причем для постоянной Ридберга определено значение:
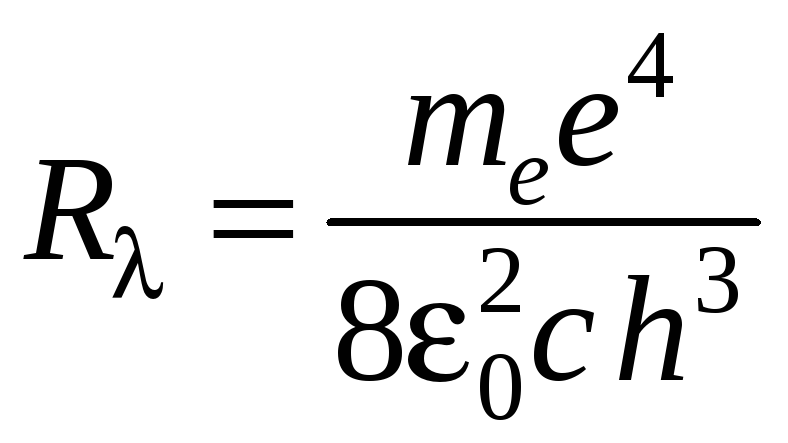 ,
(12)
,
(12)
Тогда
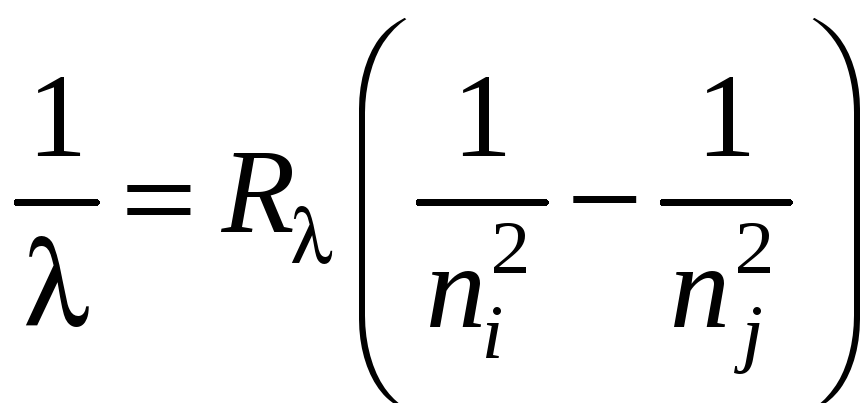 .
(13)
.
(13)
Из формулы (13) следует,
что все линии в спектре водорода могут
быть объединены в серии. Серией называется
совокупность линий, длины волн которых
описываются формулой (13) при
![]() ,
т.е. серия возникает при переходе
электрона с вышележащих энергетических
уровней на уровень с данным квантовым
числом (
,
т.е. серия возникает при переходе
электрона с вышележащих энергетических
уровней на уровень с данным квантовым
числом (![]() ).
).