Материал: КФ №2
Таблица 3.1
|
Линия |
№ п/п |
|
|
|
|
|
|
1 2 3 |
|
|
|
|
|
|
1 2 3 |
|
|
|
|
|
|
1 2 3 |
|
|
|
|
-
Тумблер 4 на лицевой панели источника питания 3 поставить в положение «ВЫКЛ».
-
Выключить из сети вилку сетевого шнура источника питания 3.
-
Обработка результатов
-
Найти значения длин волн
 для каждой из линий спектра водорода
для каждой из линий спектра водорода
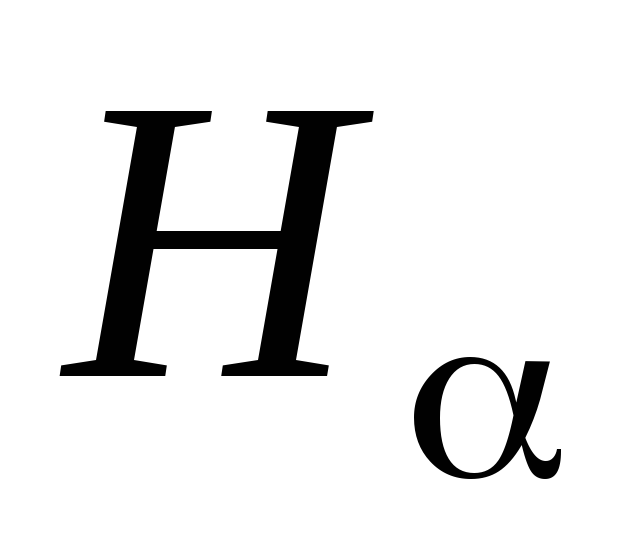 (красная),
(красная),
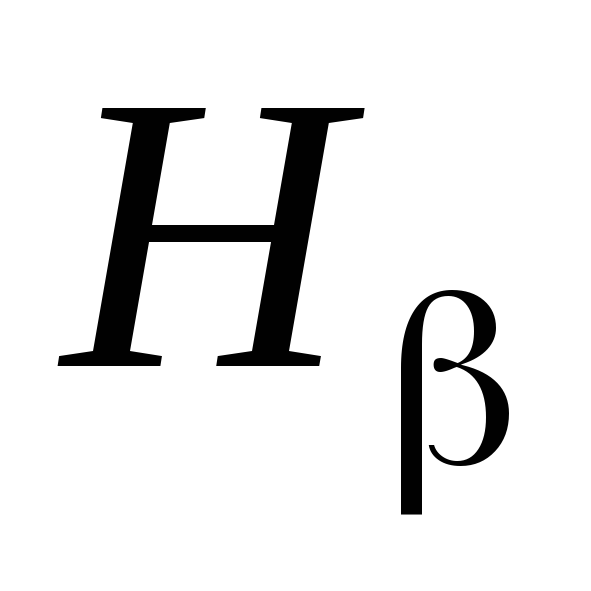 (голубая),
(голубая),
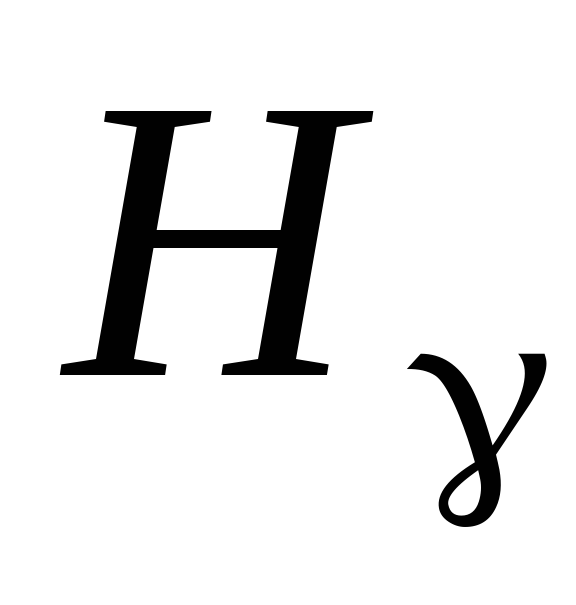 (фиолетовая) с помощью градуировочного
графика и значений
(фиолетовая) с помощью градуировочного
графика и значений
 ,
полученных в эксперименте (таблица
3.1). Значения
,
полученных в эксперименте (таблица
3.1). Значения
 также занести в таблицу 3.1.
также занести в таблицу 3.1. -
Определить среднее значение
 для каждой длины волны
для каждой длины волны
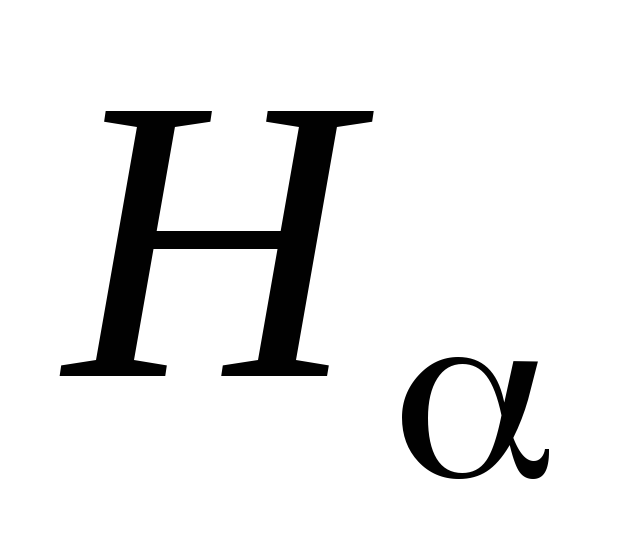 ,
,
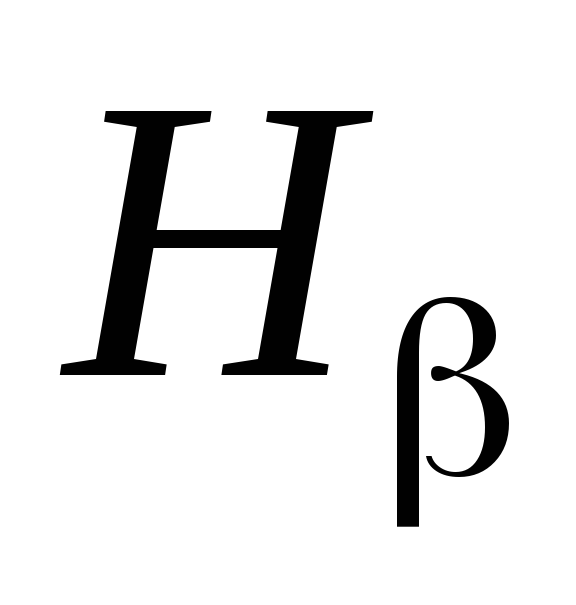 ,
,
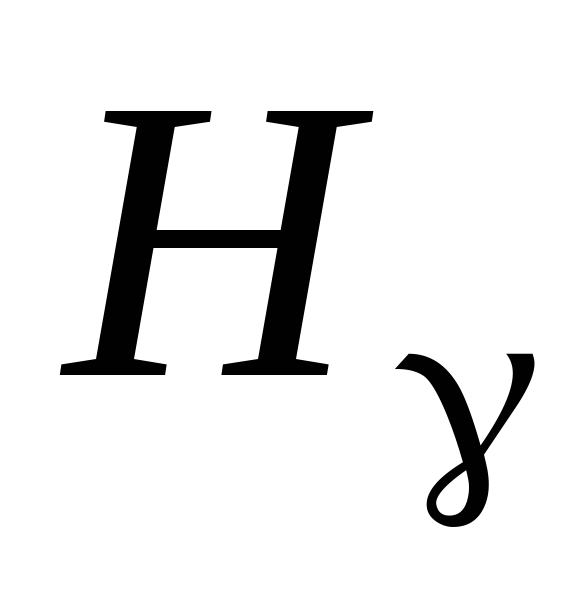 .
. -
Произвести расчет ошибок в определении длин волн (
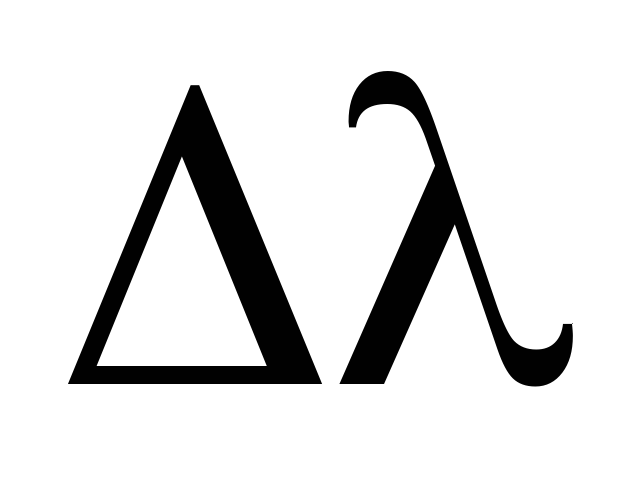 ).
Найти среднее значение (
).
Найти среднее значение (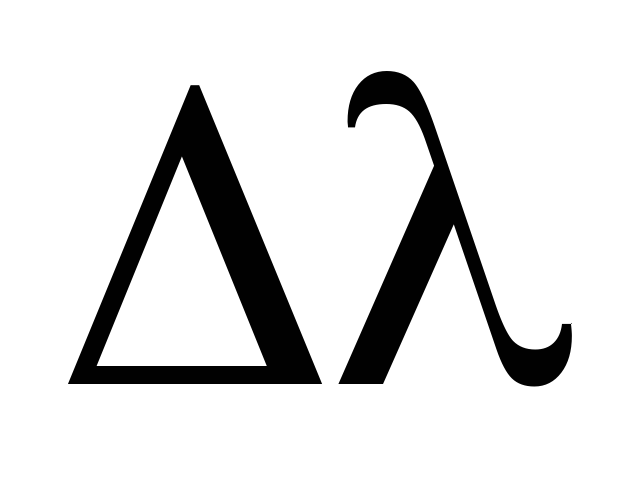 ).
Записать в таблицу 3.1.
).
Записать в таблицу 3.1. -
По полученным значениям длин волн
 построить цветным карандашом спектрограмму
серии Бальмера (подобно рис.1.1).
построить цветным карандашом спектрограмму
серии Бальмера (подобно рис.1.1). -
Сравнить значения
 ,
определенные экспериментально, с их
табличными значениями (таблица 1.1).
,
определенные экспериментально, с их
табличными значениями (таблица 1.1). -
Начертить схему энергетических уровней атома водорода и стрелками отметить переходы, соответствующие линиям
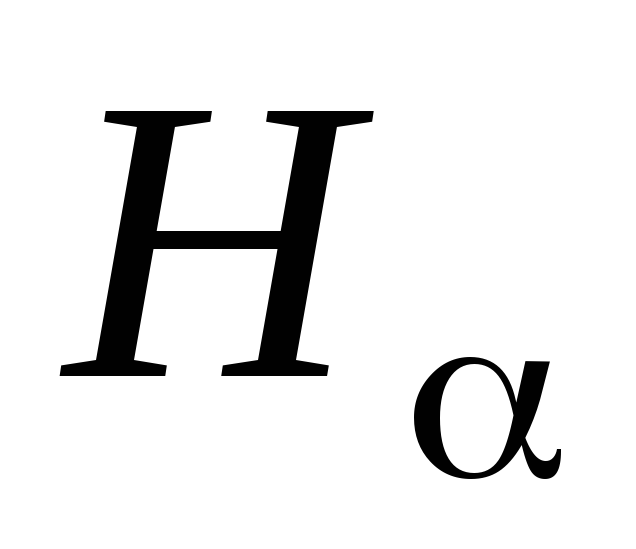 ,
,
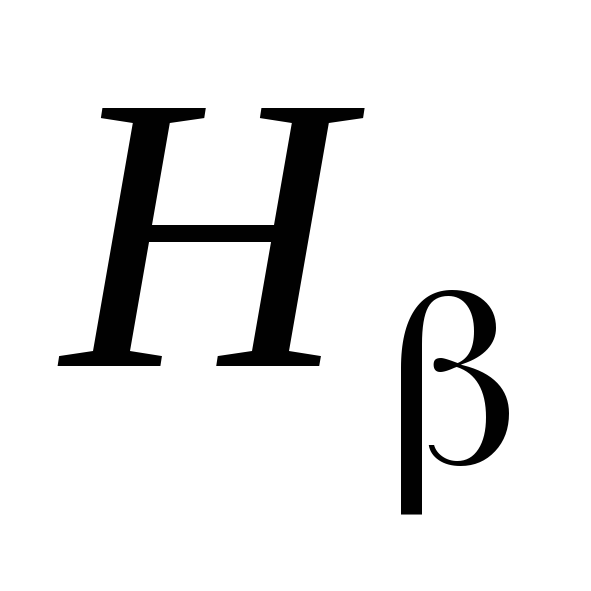 ,
,
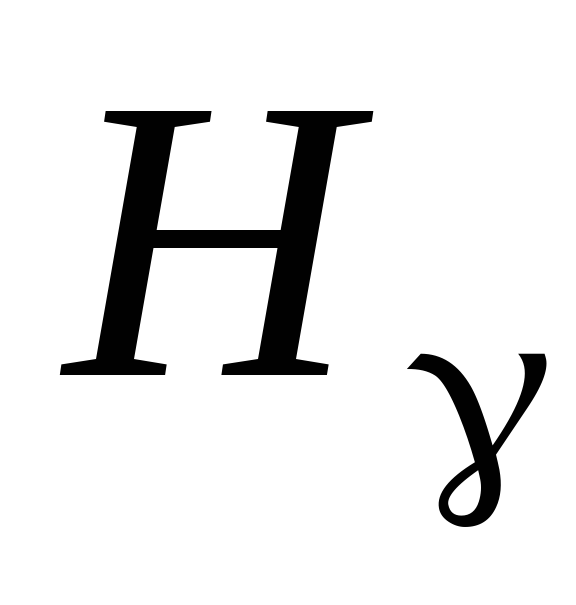 .
(рис. 1.2).
.
(рис. 1.2). -
Найти постоянную Ридберга, используя формулу (1.4) и найденные в эксперименте значения длин волн
 для красной, голубой и фиолетовой линии
(
для красной, голубой и фиолетовой линии
(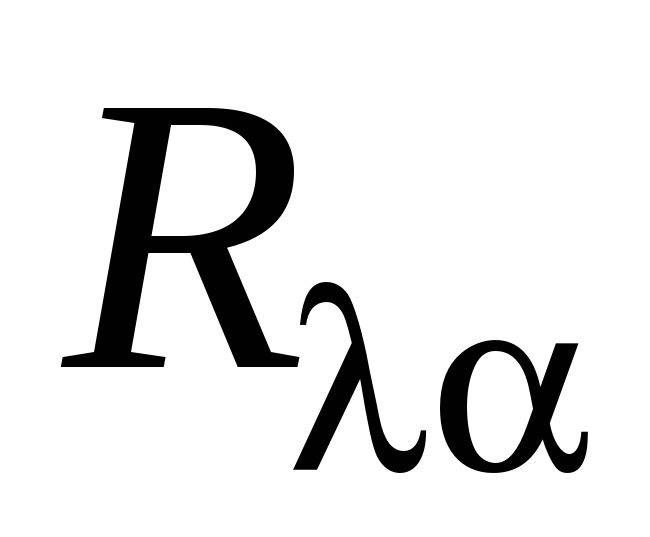 ,
,
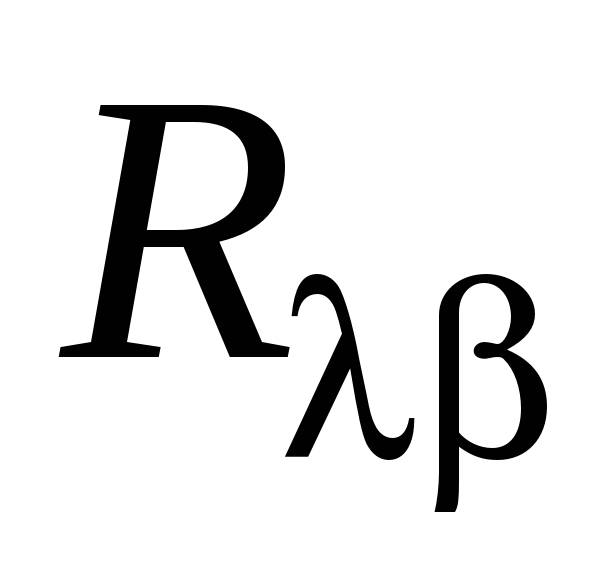 ,
,
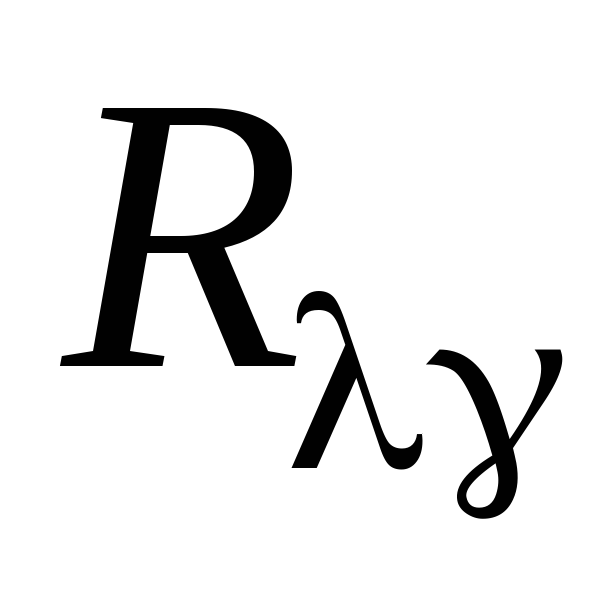 ).
). -
Найти среднее значение постоянной Ридберга по формуле:
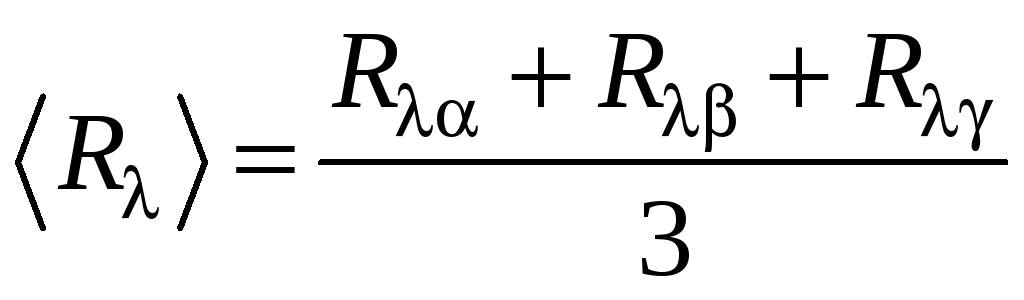 .
.
-
Сравнить полученные значения
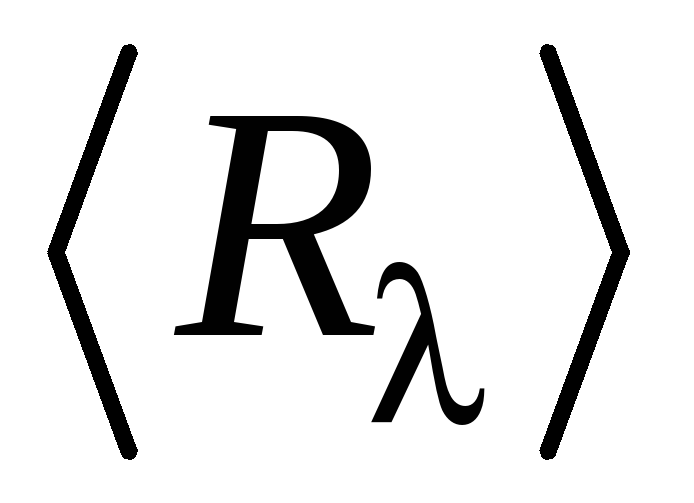 с табличным значением постоянной
Ридберга
с табличным значением постоянной
Ридберга
 .
Определить относительную погрешность
эксперимента.
.
Определить относительную погрешность
эксперимента. -
Определить по найденной
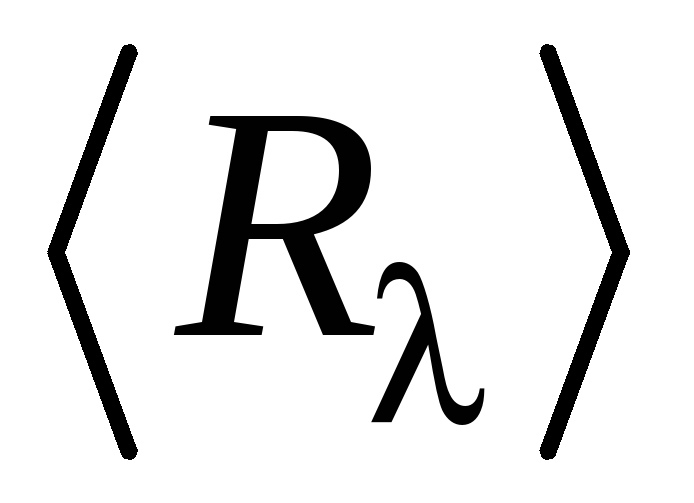 массу электрона, используя формулу
(1.10).
массу электрона, используя формулу
(1.10).
-
Требования к оформлению отчета
Отчет должен содержать:
-
Цель работы.
-
Список приборов и оборудования с указанием точности используемого прибора.
-
Основные расчетные формулы.
-
Таблицу 1.3 с внесенными в нее экспериментальными результатами.
-
Рассчитанные из эксперимента средние значения длин волн
 для красной, голубой и фиолетовых линий
спектра излучения атома водорода.
для красной, голубой и фиолетовых линий
спектра излучения атома водорода. -
Построенную цветным карандашом спектрограмму серии Бальмера.
-
Схему энергетических уровней атома водорода (рисунок 1.2) с изображенными на ней стрелками переходов, соответствующих линиям
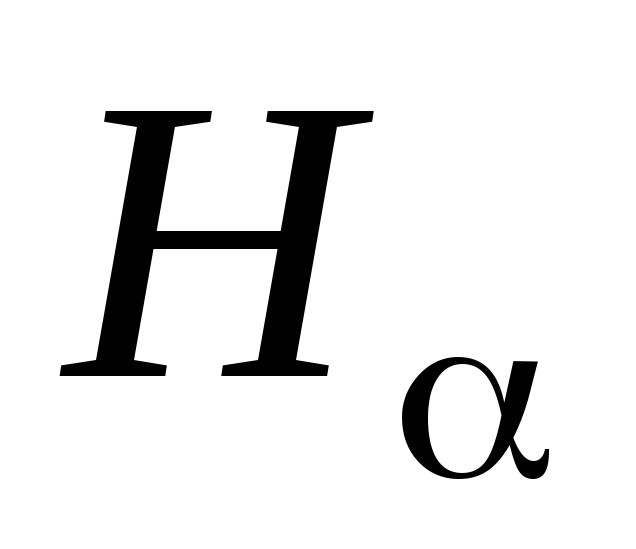 ,
,
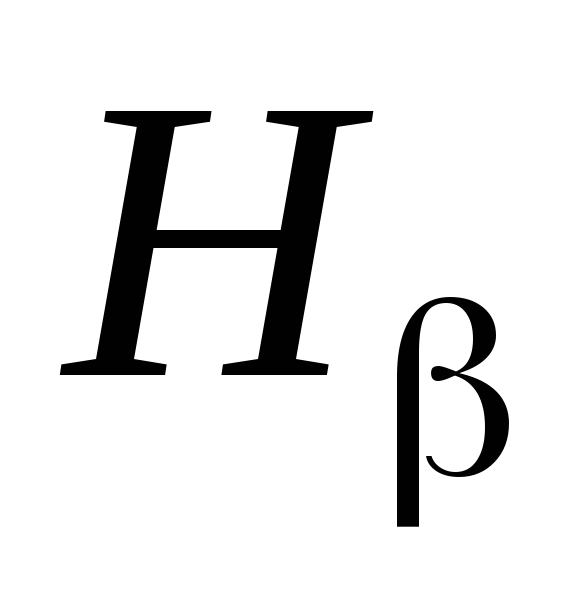 ,
,
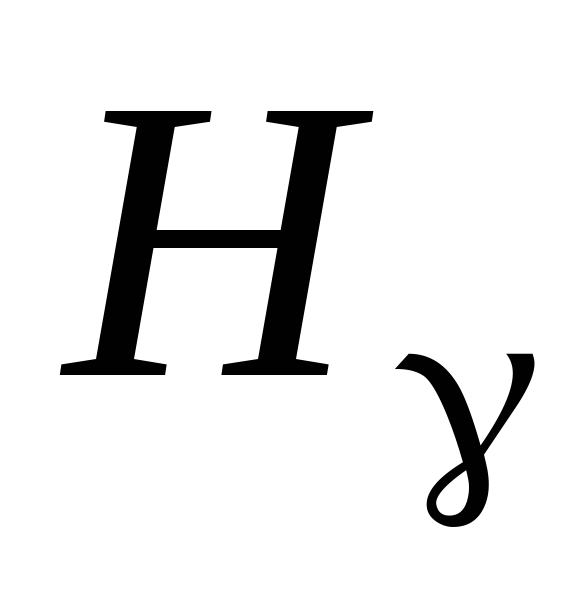 ,
,
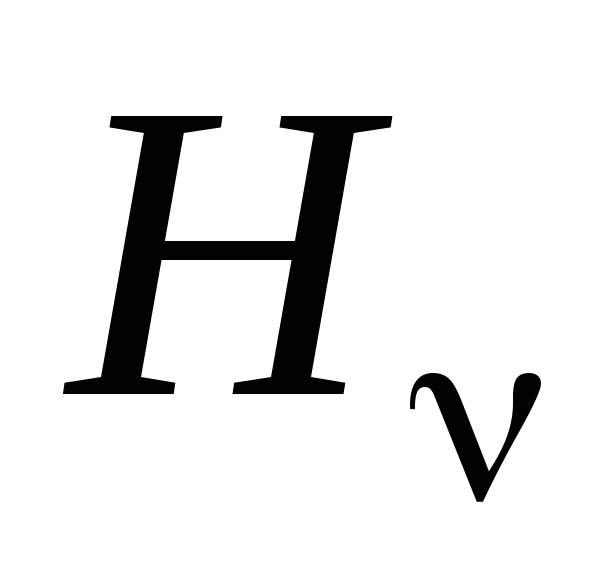 .
. -
Таблицу 5.1 с экспериментально полученными значениями постоянной Ридберга для красной, голубой и фиолетовых линий спектра.
Таблица 5.1
|
Линия спектра |
|
|
|
|
Красная |
|
|
|
|
Голубая |
|
|
|
|
Фиолетовая |
|
|
|
-
Средние значения постоянной Ридберга и массы электрона те, полученную из формулы (1.10) и их квадратичную ошибку.
-
Сравнение полученных результатов
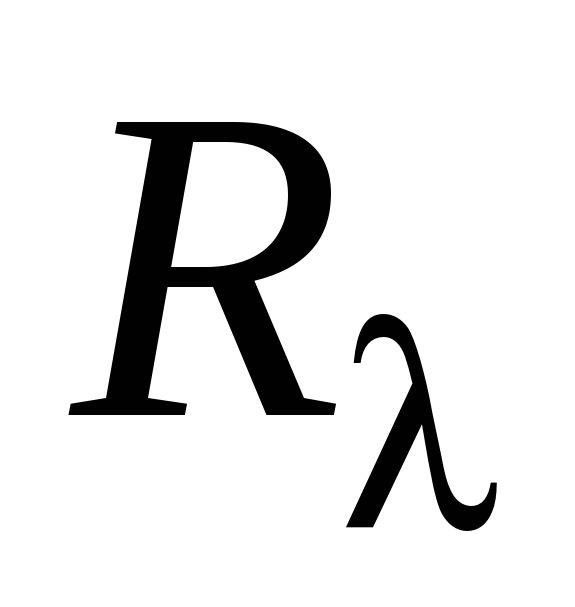 и те с их теоретическими
значениями.
и те с их теоретическими
значениями. -
Выводы.
-
Контрольные вопросы
-
Записать формулу, описывающую длины волн спектральных линий в серии Бальмера.
-
Как рассчитать коротковолновую границу серии Бальмера
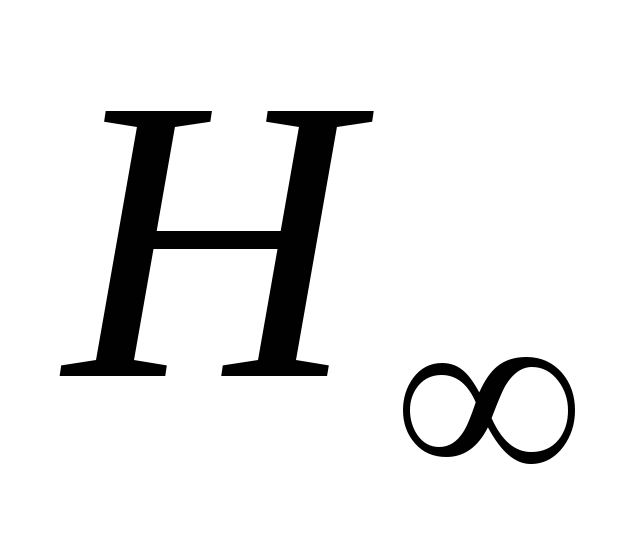 ?
? -
Рассказать о квантовых числах и физических величинах, которые они определяют.
-
Указать физический смысл постоянной Ридберга.
-
Каким образом изменяется (увеличивается, уменьшается) расстояние между соседними энергетическими уровнями DЕ в атоме водорода с ростом главного квантового числа?
-
Показать, используя энергетическую диаграмму, что серии Лаймана соответствуют наиболее энергичные кванты.
-
При каких энергетических переходах наблюдаются: красная линия
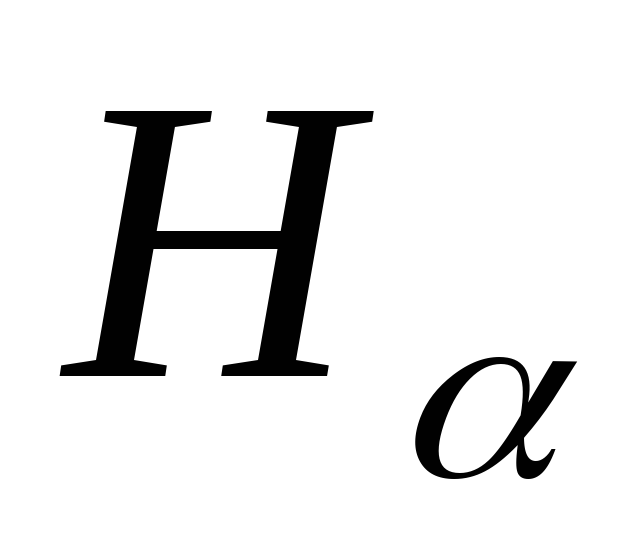 ,
голубая линия
,
голубая линия
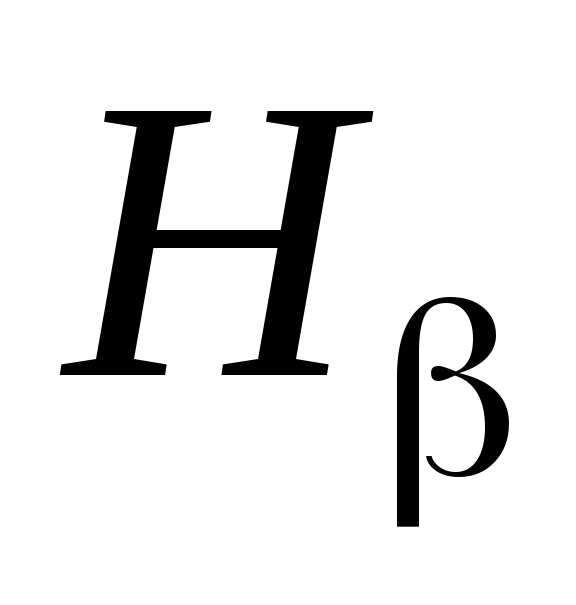 ,
фиолетовая линия
,
фиолетовая линия
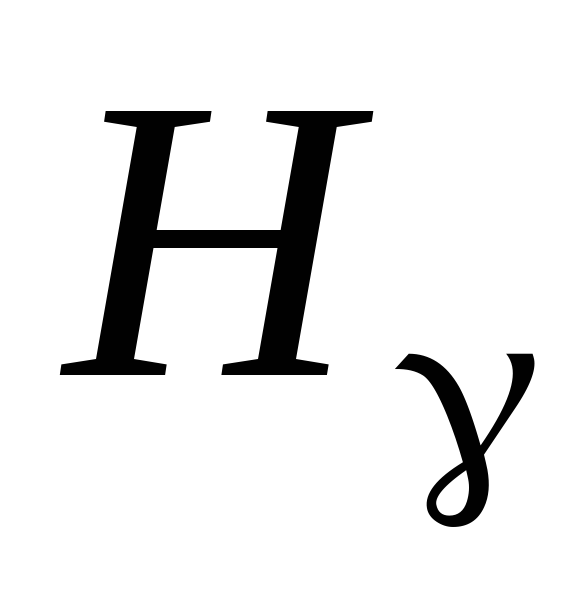 серии Бальмера?
серии Бальмера? -
Какие серии наблюдаются в спектре излучения водорода?
-
Какие серии наблюдаются в спектре поглощения водорода?
-
Каким образом в данном эксперименте сообщается атомам энергия, необходимая для их возбуждения?
-
Литература
1. Савельев И.В. Курс общей физики [Текст]/ И.В. Савельев.– т. 3. – С.П.б: Изд-во «Лянь», 2006, 512 с.
2. Иродов И.Е. Квантовая физика. Основные законы [Текст]/ И.Е. Иродов.– М.: Лаборатория Базовых Знаний, 2001–256 с.
Приложение элементарная боровская теория водородного атома
Первая попытка построения неклассической теории атома была предпринята Бором. В теории Бора не содержалось принципиального отказа от описания поведения электрона в атоме при помощи законов классической физики. Бор считал модель атома Резерфорда правильной. Цель его теории состояла в освобождении этой модели от противоречий. В постулатах, лежащих в основе теории, Бор показал, от каких положений классической физики следует отказаться, чтобы устранить противоречия между теорией и экспериментом. Постулаты Бора построены так, чтобы объяснить:
а) устойчивость атома;
б) сериальный характер спектров.
Формулируются постулаты следующим образом:
-
Из бесконечного множества электронных орбит, возможных с точки зрения классической механики, в действительности осуществляются лишь некоторые дискретные орбиты, удовлетворяющие определенным квантовым условием. Электроны, находящиеся на одной из этих орбит, не излучают.
-
При переходе из одного стационарного состояния в другое атомы испускают или поглощают излучение в виде кванта энергии
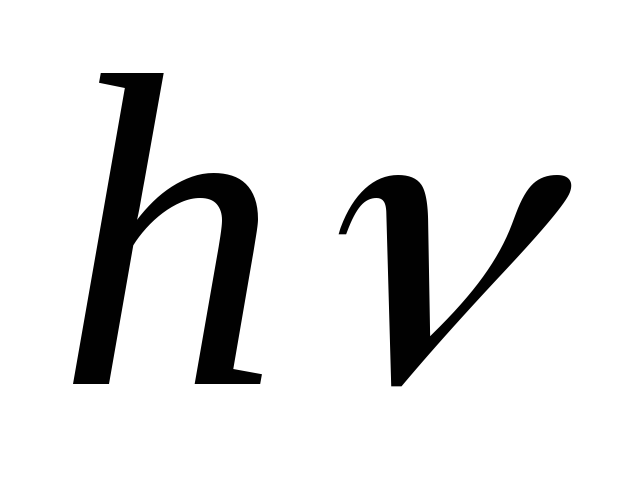 .
Величина кванта энергии равна разности
энергий тех стационарных состояний,
между которыми совершается квантовый
переход:
.
Величина кванта энергии равна разности
энергий тех стационарных состояний,
между которыми совершается квантовый
переход:
![]() .
(1)
.
(1)
Согласно
квантовому условию Бора, из всех круговых
орбит электрона в атоме водорода,
возможных с точки зрения классической
механики, осуществляются лишь те, для
которых момент импульса
![]() равен целому кратному постоянной Планка
равен целому кратному постоянной Планка
![]() ,
(2)
,
(2)
где те
– масса электрона;
![]() – его скорость;
– его скорость;
![]() – радиус орбиты; п – главное
квантовое число.
– радиус орбиты; п – главное
квантовое число.
На электрон,
движущийся в поле атомного ядра с зарядом
![]() ,
действует сила Кулона:
,
действует сила Кулона:
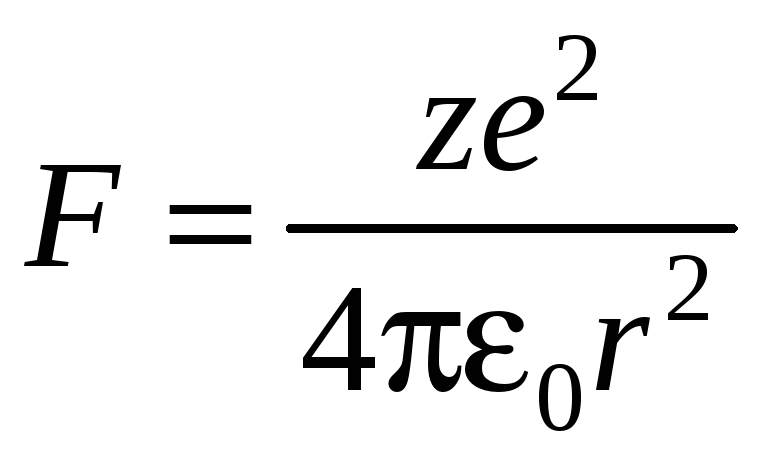 ,
(3)
,
(3)