Материал: КФ №2
Министерство образования и науки Российской Федерации
Федеральное агентство по образованию
Рыбинская государственная авиационная технологическая
академия им. П.А. Соловьева
КАФЕДРА ОБЩЕЙ И ТЕХНИЧЕСКОЙ ФИЗИКИ
Утверждено
на заседании методического
семинара кафедры
Общей и технической физики
« » _________ 2007 г.
Зав.каф. Пиралишвили Ш.А.
Лаборатория «Квантовая физика»
ЛАБОРАТОРНАЯ РАБОТА № КФ – 2
Изучение спектральных
зависимостей атома водорода при помощи монохроматора МУМ
|
Нормоконтроль: |
Автор: к. ф–м. н., доцент Шалагина Е.В. |
|
|
. |
|
____________ |
___________________ |
|
|
|
|
|
Рецензент: к. т. н., доцент Суворова З.В. |
|
|
___________________ |
Рыбинск 2007 инструкция по технике безопасности
Работа выполняется в соответствии с общими требованиями техники безопасности, действующими в учебных лабораториях кафедры О и ТФ.
– Во избежание разрушения спектральная трубка устанавливается только преподавателем;
– Не оставляйте без присмотра включенный прибор;
– Запрещается извлекать трубку из прибора при включенном напряжении питания;
– Для продления срока службы спектральных трубок не оставляйте прибор включенным более 45 минут.
ЦЕЛЬ РАБОТЫ:
-
Знакомство с элементами квантово-механической теории строения атома водорода на примере изучения его спектральных закономерностей.
-
Экспериментальное определение длин волн
 спектральных линий серии Бальмера в
видимой части спектра при помощи
монохроматора МУМ (визуальный метод
наблюдения спектра).
спектральных линий серии Бальмера в
видимой части спектра при помощи
монохроматора МУМ (визуальный метод
наблюдения спектра). -
Расчет по найденным в эксперименте значениям длин волн
 для серии Бальмера постоянной Ридберга
и массы электрона.
для серии Бальмера постоянной Ридберга
и массы электрона.
ПРИБОРЫ И ОБОРУДОВАНИЕ: универсальный монохроматор МУМ, водородная газоразрядная трубка в металлическом кожухе, высоковольтный источник питания водородной трубки, выпрямитель.
-
Теоретические сведения
Излучение невзаимодействующих друг с другом атомов состоит из отдельных спектральных линий. В соответствии с этим спектр испускания атомов называется линейчатым. Было замечено, что линии в спектрах атомов расположены не беспорядочно, а объединяются в группы, называемые сериями. Длины волн (частоты) каждой серии описываются определенной закономерностью (формулой). Спектр атома водорода выделяется своей простотой, что объясняется простотой структуры этого атома, состоящего из ядра и одного электрона, движущегося в поле точечного заряда. Спектр атома водорода состоит из нескольких серий: серии Лаймана (в ультрафиолетовой части спектра), серии Бальмера (видимая и близкая ультрафиолетовая область) и серий Пашена, Брэкета, Пфунда и др., лежащих в инфракрасной области спектра. На рисунке 1.1 представлена часть спектра атомного водорода в видимой и близкой ультрафиолетовой области (серия Бальмера).
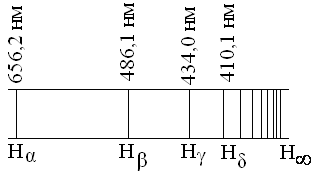
Рис.1.1
Символами
![]() обозначены соответственно красная,
голубая и две фиолетовые линии, находящиеся
в видимой области спектра,
обозначены соответственно красная,
голубая и две фиолетовые линии, находящиеся
в видимой области спектра,
![]() указывает границу серии Бальмера,
лежащую в ультрафиолетовой области.
Расстояние между линиями закономерно
убывает по мере перехода от более длинных
волн к коротким.
указывает границу серии Бальмера,
лежащую в ультрафиолетовой области.
Расстояние между линиями закономерно
убывает по мере перехода от более длинных
волн к коротким.
Частоты всех спектральных линий атома водорода можно представить одной формулой, которая была получена экспериментально и называется обобщенной формулой Бальмера:
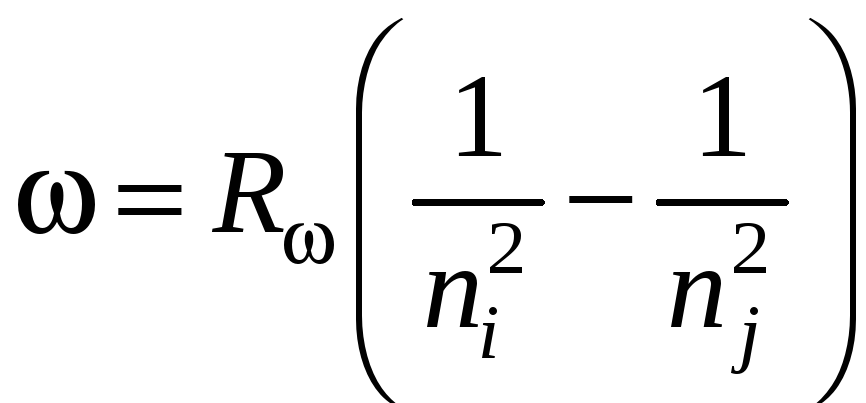 ,
(1.1)
,
(1.1)
где
![]() – циклическая (круговая) частота;
– циклическая (круговая) частота;
![]() – постоянная Ридберга,
– постоянная Ридберга,
![]() с-1;
с-1;
![]() – целые числа, которые для различных
серий и различных линий спектра принимают
следующие значения:
– целые числа, которые для различных
серий и различных линий спектра принимают
следующие значения:
-
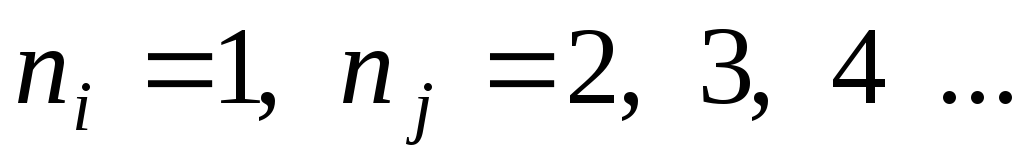 – для серии Лаймана;
– для серии Лаймана;
-
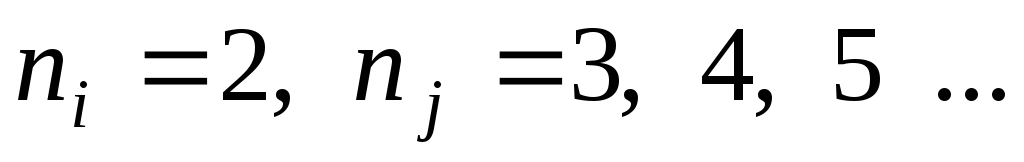 – для серии Бальмера;
– для серии Бальмера;
-
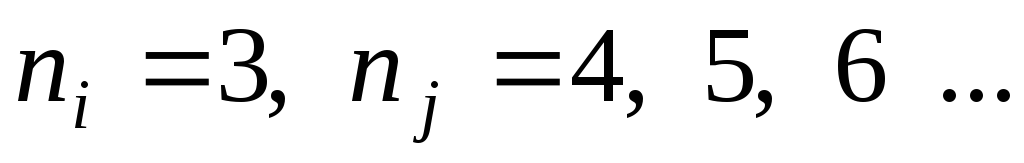 – для серии Пашена и т.д.
– для серии Пашена и т.д.
Таким образом, частоты спектральных линий в серии Бальмера опишутся формулой:
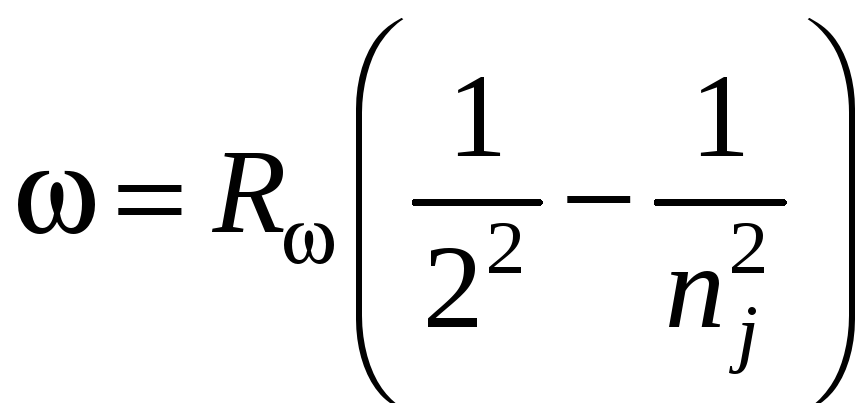 ,
(1.2)
,
(1.2)
где
![]() ….
….
В спектроскопе принято характеризовать спектральные линии не частотой, а обратной длине волны величиной:
![]() .
(1.3)
.
(1.3)
Формула Бальмера в этом случае имеет вид:
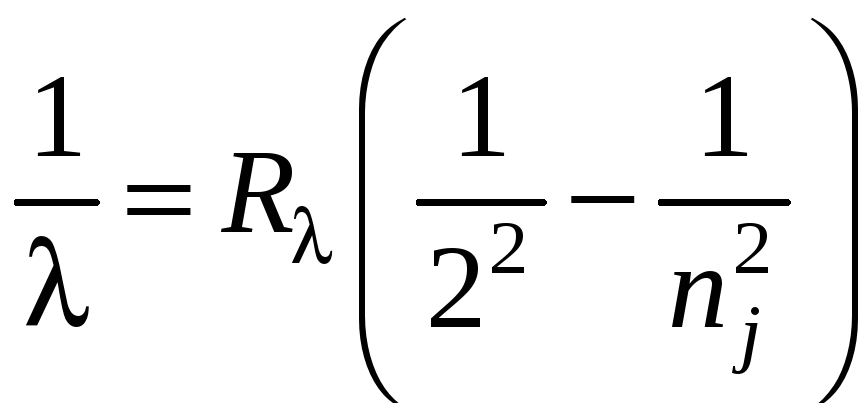 .
(1.4)
.
(1.4)
Постоянная Ридберга
![]() в формуле (1.4) имеет значение
в формуле (1.4) имеет значение
![]() и измеряется в м-1.
и измеряется в м-1.
В таблице
1.1 приведены значения длин волн
![]() серии Бальмера, рассчитанные по формуле
(1.4).
серии Бальмера, рассчитанные по формуле
(1.4).
При возрастании
![]() длина волны
длина волны
![]() стремится к предельному значению
стремится к предельному значению
![]() ,
которое называется границей серии. Для
серии Бальмера (
,
которое называется границей серии. Для
серии Бальмера (![]() )
граница серии обозначается символом
)
граница серии обозначается символом
![]() .
.
Таблица 1.1
|
Название линии |
Цвет |
|
Длина волны в м |
|
|
Красная |
3 |
6,5628×10-7 |
|
|
Голубая |
4 |
4,8813×10-7 |
|
|
Фиолетовая |
5 |
4,3405×10-7 |
|
|
Фиолетовая |
6 |
4,1017×10-7 |
|
|
Ультрафиолетовая |
¥ |
2,7434×10-8 |
Теоретическое объяснение спектральных закономерностей атома водорода впервые дано в полуклассической теории Бора (см. приложение к настоящей работе).
После открытия волновых свойств вещества стало ясно, что теория Бора является переходным этапом на пути к созданию последовательной теории атомных явлений. Такой теорией явилась квантовая механика.
В квантовой
механике состояние электрона в атоме
водорода определяется заданием полной
энергии электрона Е, величины момента
импульс М, ориентации этого момента
на некоторое направление в пространстве
![]() .
.
Состояние
электрона можно также задать с помощью
набора квантовых чисел
![]() ,
которые и определяют значения Е, М
и МZ.
,
которые и определяют значения Е, М
и МZ.
Параметр п, называется главным квантовым числом, определяет собственные (дозволенные) значения энергии электрона в атоме водорода. Согласно законам квантовой механики, электрон может находиться в ряде устойчивых (стационарных) состояний, характеризуемых набором дискретных значений полной энергии Еп:
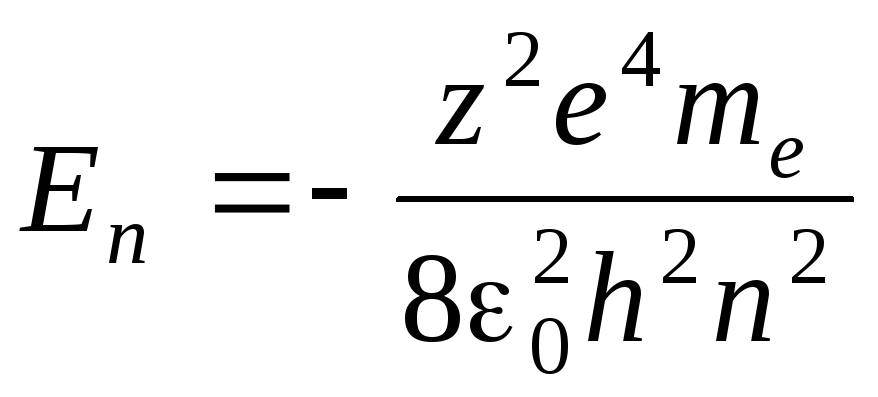 ,
(1.5)
,
(1.5)
где
![]() – порядковый номер элемента в таблице
Менделеева. Для водорода
– порядковый номер элемента в таблице
Менделеева. Для водорода
![]() = 1;
= 1;
е – заряд электрона, е = 1,6×10-19 Кл;
![]() – электрическая постоянная,
– электрическая постоянная,
![]() =8,85×10-12
Ф×м-1;
=8,85×10-12
Ф×м-1;
![]() – постоянная Планка,
– постоянная Планка,
![]() =6,62×10-34
Дж×с;
=6,62×10-34
Дж×с;
те – масса электрона, те = 9,1×10-31 кг.
Главное квантовое число принимает значения п = 1, 2, 3, … .
Полная энергия электрона Еп отрицательна, это означает, что атом – устойчивая система, для разрушения которой необходимо затратить энергию. Энергия ионизации атома водорода 13,6 эВ.
При переходе
из одного стационарного состояния в
другое атомы испускают или поглощают
излучение в виде кванта энергии
![]() ,
равного разности энергий тех стационарных
состояний, между которыми совершается
квантовый переход:
,
равного разности энергий тех стационарных
состояний, между которыми совершается
квантовый переход:
![]() ,
(1.6)
,
(1.6)
где
![]() ,
,![]() – энергия состояния, из которого
совершается переход;
– энергия состояния, из которого
совершается переход;
![]() – энергия состояния, в которое атом
переходит.
– энергия состояния, в которое атом
переходит.
Если для
определения энергии
![]() и
и
![]() использовать формулу (1.5), то для атома
водорода:
использовать формулу (1.5), то для атома
водорода:
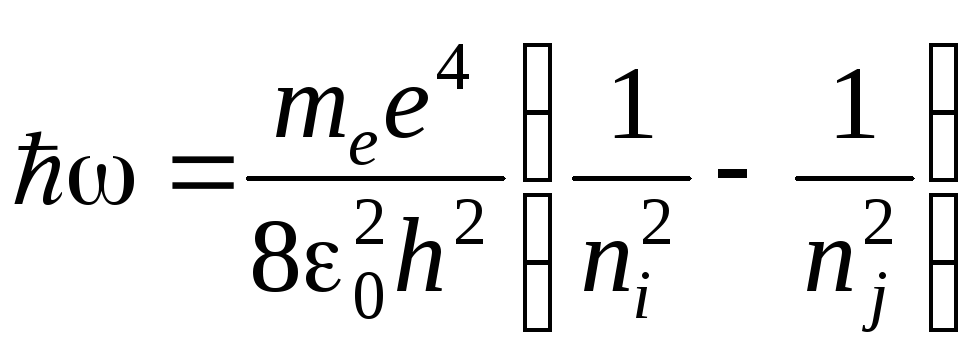 ,
,
откуда
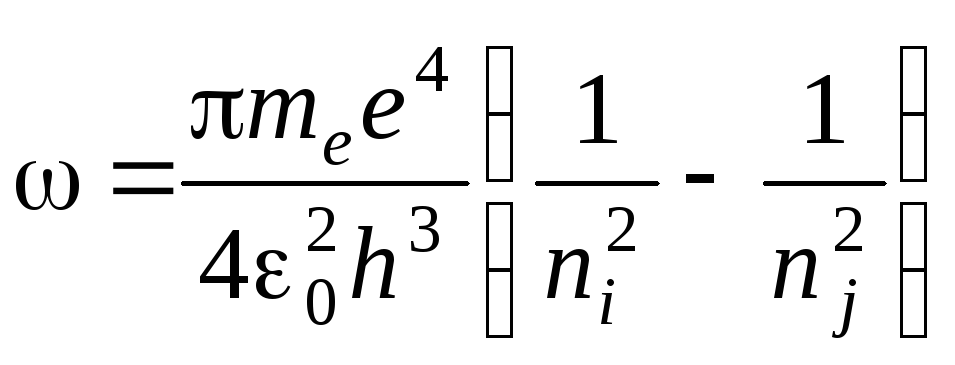 ,
(1.7)
,
(1.7)
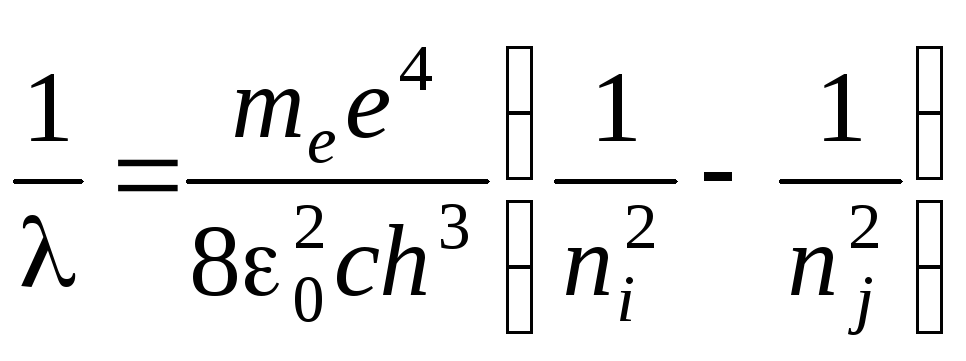 .
(1.8)
.
(1.8)
Сравнивая формулы, полученные квантовой механикой (1.7), (1.8), с экспериментально найденными закономерностями (1.1) и (1.4) соответственно, можно определить теоретическое значение постоянной Ридберга:
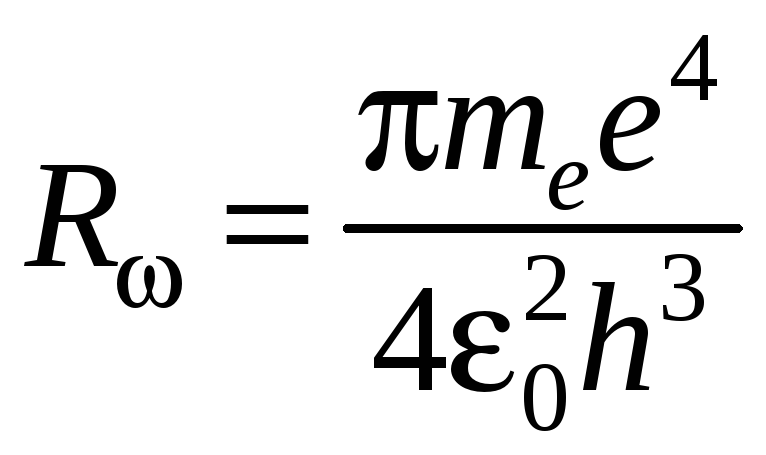 ,
(1.9)
,
(1.9)
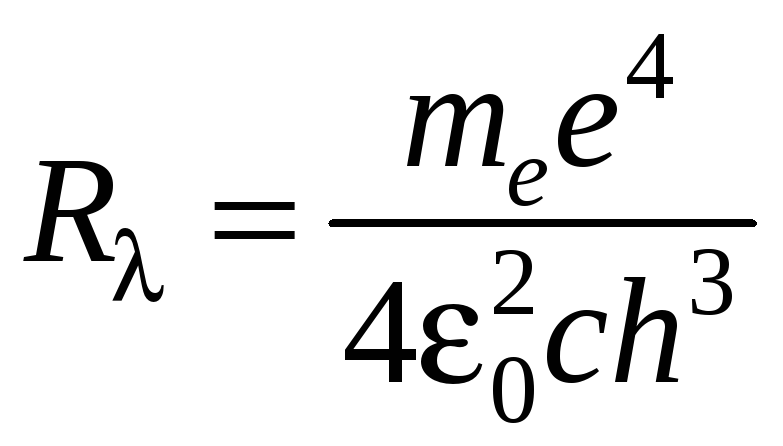 .
(1.10)
.
(1.10)
Значения, предсказанные квантовой механикой, хорошо совпадают с экспериментально найденными.
Таким образом,
постоянная Ридберга представляет
величину, пропорциональную энергии
атома в основном (![]() )
состоянии.
)
состоянии.
Параметр
![]() называется орбитальным квантовым
числом, которое определяет величину
(модуль) момента импульса электрона в
атоме по формуле:
называется орбитальным квантовым
числом, которое определяет величину
(модуль) момента импульса электрона в
атоме по формуле:
![]() .
(1.11)
.
(1.11)
При заданном
главном квантовом числе п орбитальное
квантовое число может принимать одно
из следующих значений:
![]() =
0, 1, 2, …п – 1, т.е. всего п –
значений.
=
0, 1, 2, …п – 1, т.е. всего п –
значений.
Параметр
![]() называется магнитным квантовым числом
и определяет проекцию момента импульса
электрона на некоторое направление
называется магнитным квантовым числом
и определяет проекцию момента импульса
электрона на некоторое направление
![]() в пространстве по формуле:
в пространстве по формуле:
![]() .
(1.12)
.
(1.12)