Материал: КФ №2
При данном
квантовом числе
![]() квантовое число
квантовое число
![]() может принимать
может принимать
![]() различных значений, а именно:
различных значений, а именно:
![]() .
.
Таким образом,
атом водорода, находящийся в стационарном
состоянии, характеризуемом определенной
энергией, может находиться в состояниях,
отличающихся модулем М, либо его
проекцией
![]()
Состояния с
одинаковым значением энергии, но
различными значениями модуля момента
импульса или его проекции на некоторое
направление
![]() называются вырожденными, а число
различных квантовых состояний с одним
и тем же значением энергии называется
кратностью вырождения соответствующего
уровня. Кратность вырождения
называются вырожденными, а число
различных квантовых состояний с одним
и тем же значением энергии называется
кратностью вырождения соответствующего
уровня. Кратность вырождения
![]() уровней атома водорода определяется
по формуле:
уровней атома водорода определяется
по формуле:
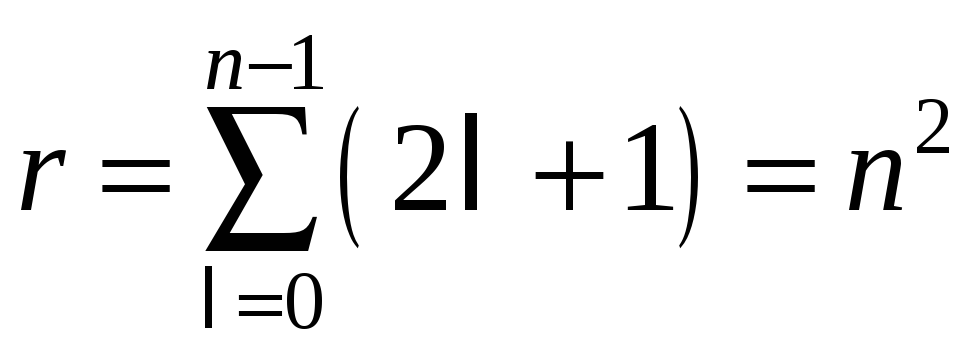 .
(1.13)
.
(1.13)
В атомной
физике используются условные обозначения
состояний электрона с различными
значениями момента импульса М.
Состояние с
![]() обозначается как
обозначается как
![]() –
состояние,
–
состояние,
![]() обозначается как
обозначается как
![]() –
состояние,
–
состояние,
![]() обозначается как
обозначается как
![]() –
состояние,
–
состояние,
![]() обозначается как
обозначается как
![]() –
состояние и т.д. (по алфавиту)
–
состояние и т.д. (по алфавиту)
При обозначении
состояния значение главного квантового
числа указывается перед обозначением
квантового числа
![]() .
Поскольку
.
Поскольку
![]() принимает значения от 0 до п – 1, то
возможны следующие состояния:
принимает значения от 0 до п – 1, то
возможны следующие состояния:
п = 1,
![]() ® 1
® 1![]() – состояние,
– состояние,
п = 2,
![]() ® 2
® 2![]() и
2р – состояния,
и
2р – состояния,
п = 3,
![]() ®
3
®
3![]() ,
3р, 3
,
3р, 3![]() – состояния и т.д.
– состояния и т.д.
Схема энергетических уровней атома водорода представлена на рис. 1.2. На схеме отражено частичное вырождение уровней. Видно, что энергия электрона зависит лишь от главного квантового числа.
По оси ординат на диаграмме отложены значения энергии электрона в электрон – вольтах (эВ).
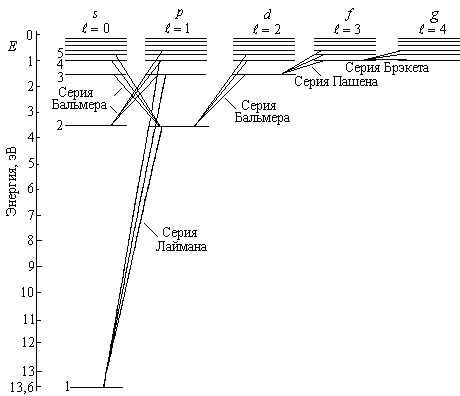
Рис. 1.2
Состояние
1![]() является
основным состоянием атома водорода. В
этом состоянии атом обладает минимальной
энергией. Ее величину можно определить
из формулы (1.6) при п = 1:
является
основным состоянием атома водорода. В
этом состоянии атом обладает минимальной
энергией. Ее величину можно определить
из формулы (1.6) при п = 1:
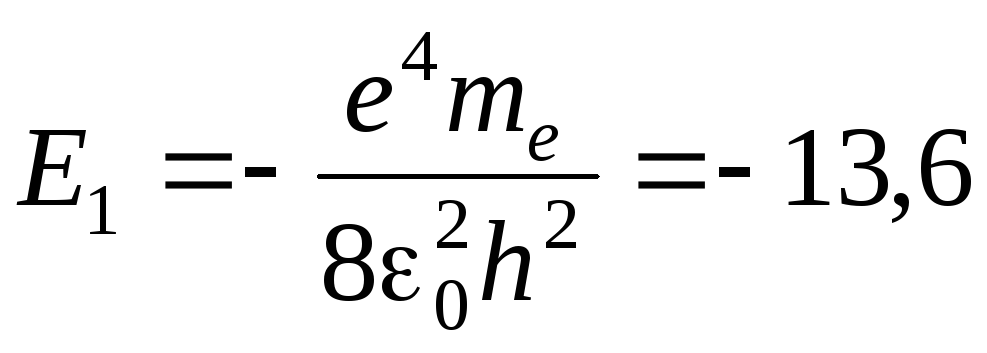 эВ.
эВ.
Таким образом, энергия, необходимая для ионизации атома водорода, равна 13,6 эВ.
Энергию электрона в состояниях с п = 2, 3, 4 и т.д. можно определить также из формулы (1.5), подставив в нее соответствующее значение квантового числа п. Из диаграммы энергетических уровней видно, что с ростом главного квантового числа п уровни сближаются.
Чтобы перевести атом из основного состояния в возбужденное (т.е. в состояние с большей энергией), ему необходимо сообщить энергию. Это может быть осуществлено за счет теплового соударения атомов или за счет столкновения атома с достаточно быстрым электроном (ускоренным электрическим полем в газовом разряде) или за счет поглощения атомом фотона.
Фотон при
поглощении его атомом передает ему всю
свою энергию (фотон неделим), поэтому
атом может поглощать только те фотоны,
энергия которых в точности равна разности
энергий двух его уровней. Поскольку
поглощающий атом обычно находится в
основном состоянии 1![]() ,
спектр поглощения водородного атома
должен состоять из линий, соответствующих
переходам
,
спектр поглощения водородного атома
должен состоять из линий, соответствующих
переходам
1![]() ®пр
(п = 2, 3, 4 …)
®пр
(п = 2, 3, 4 …)
Эти переходы отвечают серии Лаймана. Следовательно, в обычных условиях в спектре поглощения водорода наблюдается единственная серия Лаймана.
При переходе
из состояний с большей энергией в
состояние с меньшей энергией атом
излучает квант энергии
![]() .
Длина волны (частота) излучения
определяется формулами (1.2), (1.8) или
(1.4), (1.7). В квантовой механике доказывается,
что для орбитального квантового числа
существует правило отбора, согласно
которому возможны лишь такие переходы,
при которых
.
Длина волны (частота) излучения
определяется формулами (1.2), (1.8) или
(1.4), (1.7). В квантовой механике доказывается,
что для орбитального квантового числа
существует правило отбора, согласно
которому возможны лишь такие переходы,
при которых
![]() изменяется на единицу:
изменяется на единицу:
![]() .
(1.14)
.
(1.14)
Это связано
с тем, что фотон обладает спиновым
моментом импульса, равным
![]() ,
и правило отбора является следствием
закона сохранения момента импульса.
,
и правило отбора является следствием
закона сохранения момента импульса.
На рис. 1.2 показаны переходы, разрешенные правилом (1.14). Пользуясь условными обозначениями состояний электрона, переходы, приводящие к серии Лаймана можно записать в виде:
пр ®1![]() (п = 2, 3 …).
(п = 2, 3 …).
Это означает,
что в формулах (1.2), (1.4), (1.7), (1.8)
![]() ,
,
![]() .
.
Таким образом,
серия Лаймана возникает, если атом
переходит со всех вышележащих
энергетических уровней на уровень
![]() .
.
Серия Бальмера
наблюдается, если атом переходит со
всех вышележащих энергетических уровней:
![]() на уровень
на уровень
![]() (формулы (1.2), (1.4), (1.7), (1.8)). Серии Бальмера
соответствуют переходы:
(формулы (1.2), (1.4), (1.7), (1.8)). Серии Бальмера
соответствуют переходы:
![]()
![]()
![]() .
.
Красная линия
![]() имеет наибольшую длину волны в серии
Бальмера, а соответствующий ей квант
имеет наименьшую энергию
имеет наибольшую длину волны в серии
Бальмера, а соответствующий ей квант
имеет наименьшую энергию
![]() .
Поэтому линия
.
Поэтому линия
![]() наблюдается при переходе атома в
состояние
наблюдается при переходе атома в
состояние
![]() из «ближайшего» к нему энергетического
состояния с
из «ближайшего» к нему энергетического
состояния с
![]() ,
т.е.
,
т.е.
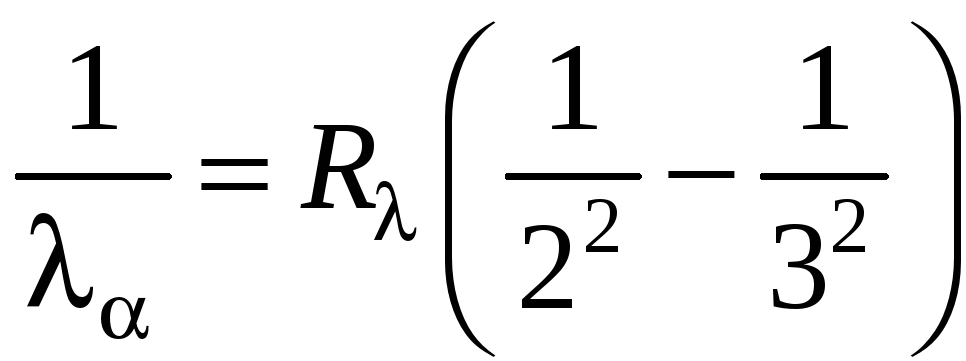 .
(1.15)
.
(1.15)
По аналогичным
соображениям, голубой линии
![]() в серии Бальмера соответствует переход
из состояния
в серии Бальмера соответствует переход
из состояния
![]() в
в
![]() ,
фиолетовой линии
,
фиолетовой линии
![]() соответствует
переход из
соответствует
переход из
![]() в
в
![]() и т.д. Следовательно,
и т.д. Следовательно,
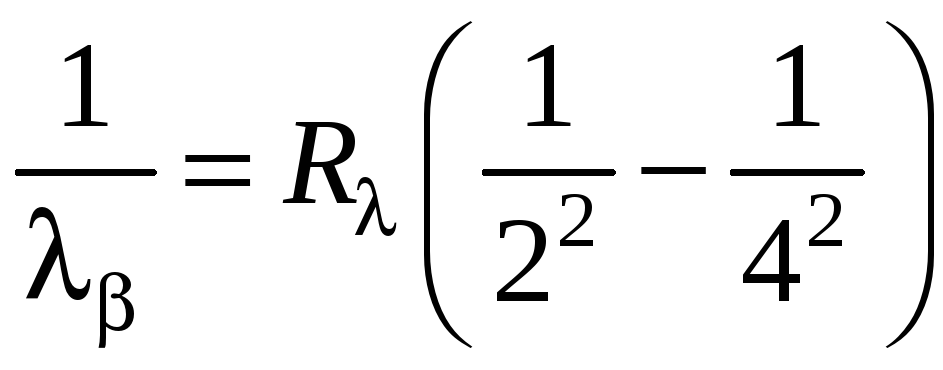 ,
(1.16)
,
(1.16)
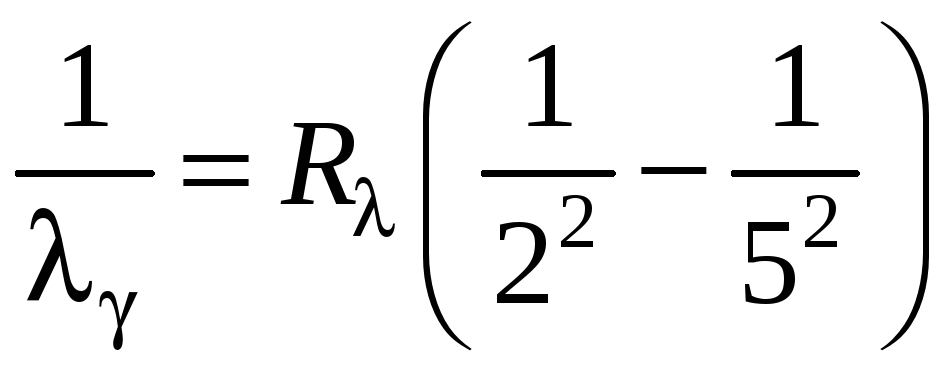 .
(1.17)
.
(1.17)
Серия Пашена
возникает, если атом переходит со всех
вышележащих энергетических уровней на
уровень
![]() т.д.
т.д.
В связи с
тем, что с ростом квантового числа п
энергетические уровни в атоме водорода
сближаются, наиболее энергичные кванты
излучаются при переходах атома с
вышележащих уровней на уровень
![]() ,
поэтому соответствующая этим переходам
серия Лаймана находится в ультрафиолетовом
диапазоне, серии же Пашена, Брэкета и
др. лежат в инфракрасной области спектра.
В видимой и близкой к ультрафиолетовой
области находится серия Бальмера.
,
поэтому соответствующая этим переходам
серия Лаймана находится в ультрафиолетовом
диапазоне, серии же Пашена, Брэкета и
др. лежат в инфракрасной области спектра.
В видимой и близкой к ультрафиолетовой
области находится серия Бальмера.
-
Описание установки и методики измерения
Установка для изучения спектра излучения атома водорода визуальным методом при помощи монохроматора МУМ приведена на рис.2.1.


Рис. 2.1
Лабораторная установка состоит из следующих элементов: источника излучения (спектральная трубка с водородом) 1; монохроматора МУМ 2; источника питания 3 для спектральных трубок.
На передней панели источника питания 3 расположен выключатель питания 4. В качестве источника излучения используется газоразрядная трубка, наполненная водородом под небольшим давлением. Атомы водорода в трубке переходят в возбужденное состояние при взаимодействии с электронами, ускоренными электрическим полем, которое создается между электродами газоразрядной трубки. Возбужденные атомы излучают энергию, в результате газ в трубке светится розовым цветом.
Монохроматор 2 предназначен для определения в нанометрах длин волн в видимой части спектра атома водорода. Оптика монохроматора состоит из коллиматора 5, дифракционной решетки с поворотным механизмом и зрительной трубы. Коллиматор создает параллельный пучок света, падающий на дифракционную решетку. Дифракционная решетка разлагает свет в спектр, который наблюдается в окуляре 6 зрительной трубы монохроматора. Газоразрядная трубка устанавливается перед входной щелью 7 монохроматора. Сменная щель 8 подбирается так, чтобы линии спектра в окуляре 6 были узкими, но достаточно четко видимыми. Регулировка сменной щели производится лаборантом.
Излучение от газоразрядной трубки проходит через входную щель 8, через дифракционную решетку, помещенную внутри монохроматора МУМ, и через выходную щель 9 попадает в расположенный за ней окуляр 6 зрительной трубы. Сканирование (просмотр) спектра осуществляется поворотом дифракционной решетки вокруг оси при помощи винта 10, расположенного на боковой стенке монохроматора. Непосредственный отчет длины волны излучения в нанометрах выполняется при помощи шкалы 11 цифрового механического счетчика, вмонтированного в корпус монохроматора.
-
Порядок выполнения работы
-
Водородную газоразрядную трубку в кожухе 1 установить перед входной щелью.
-
Включить в сеть вилку сетевого шнура источника питания 3.
-
Тумблер на лицевой панели источника питания поставить в положение «вкл». При этом в трубке 1 возникает самостоятельный разряд розового цвета. В поле зрения окуляра 6 должны появиться отдельные линии спектра водорода.
-
Просмотреть видимую часть спектра водорода, медленно поворачивая винт 10. Установить, какие линии принадлежат спектру излучения атомарного водорода:
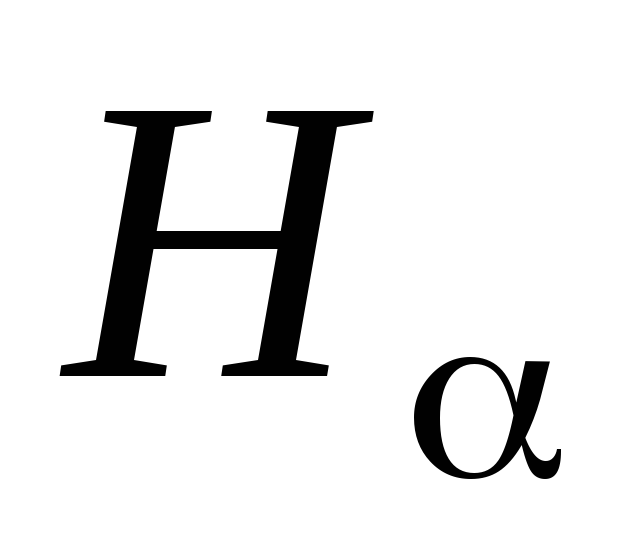 (красная),
(красная),
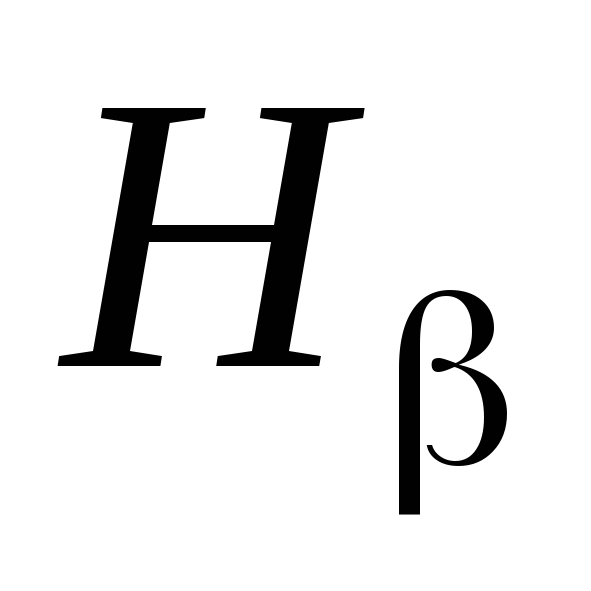 (голубая),
(голубая),
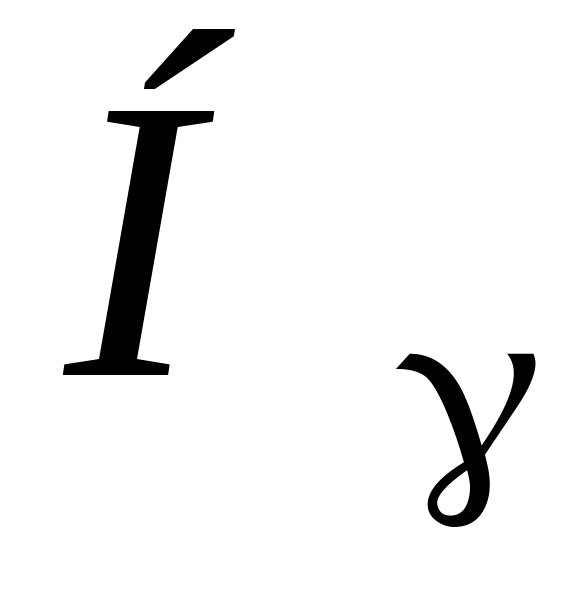 (фиолетовая). В поле зрения также могут
наблюдаться линии различного цвета
молекулярного водорода.
(фиолетовая). В поле зрения также могут
наблюдаться линии различного цвета
молекулярного водорода.
-
Совместить указатель в поле зрения окуляра 6 с линиями
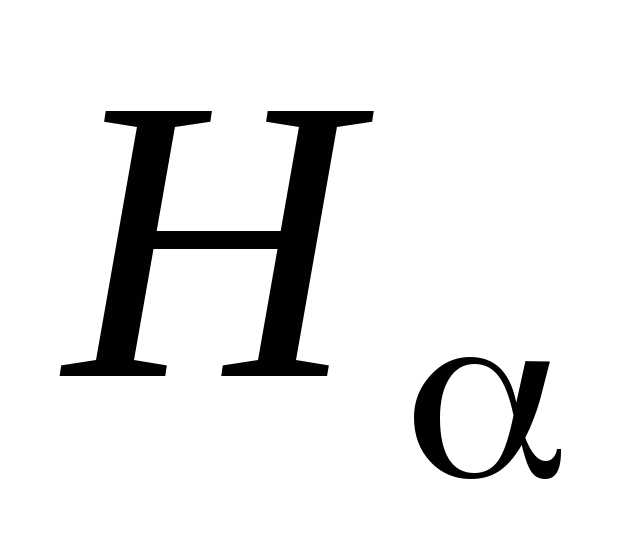 ,
,
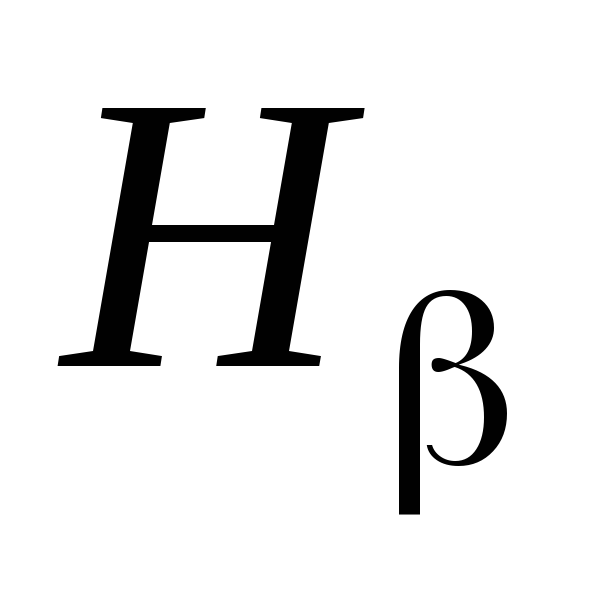 ,
,
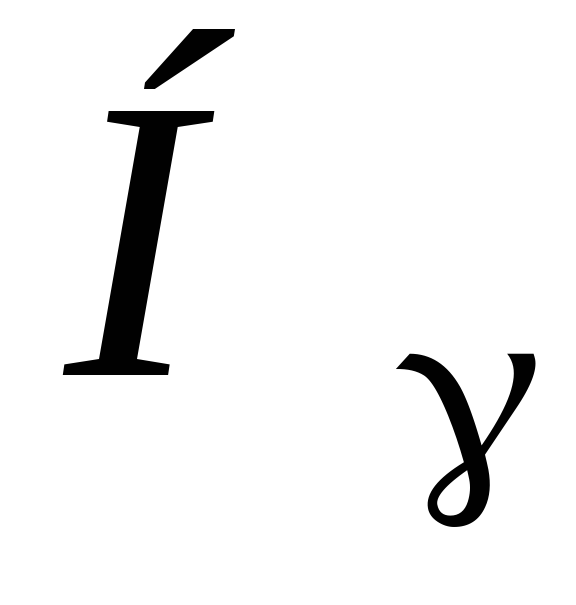 – последовательно и произвести каждый
раз соответствующий отсчет длины волны
– последовательно и произвести каждый
раз соответствующий отсчет длины волны
 в нанометрах при помощи шкалы 11 цифрового
механического счетчика. Измерения для
каждой линии спектра произвести не
менее трех раз.
в нанометрах при помощи шкалы 11 цифрового
механического счетчика. Измерения для
каждой линии спектра произвести не
менее трех раз. -
Результаты измерений
 в нм записать в таблицу 3.1.
в нм записать в таблицу 3.1.