Материал: Изучение воздействия электромагнитного поля на водные растворы белков и ДНК
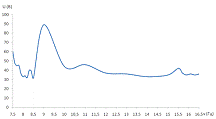
Рисунок 14 - График зависимости интенсивности
хемилюминесценции водных растворов ДНК от частоты ЭМП НЧ при различных частотах
воздействия.
Для анализа полученных результатов в таблицу 5
сведены значения максимумов интенсивности хемилюминесценции водных растворов
ДНК для каждой применяемой частоты ЭМП (таблица 5). Этот график наглядно
показывает пики резонансных частот ЭМП, которые использовались для обработки
растворов ДНК.
Таблица 5 - Значения максимумумов напряжения хемилюминесценции в зависимости от частоты облучения ДНК.
|
ν (Гц) |
U (В) |
ν (Гц) |
ν (Гц) |
U (В) |
ν (Гц) |
U (В) |
|
|
7,5 |
60 |
8,1 |
34 |
9 |
89 |
15,5 |
42 |
|
7,6 |
48 |
8,2 |
32 |
10 |
44 |
15,7 |
37 |
|
7,7 |
45 |
8,3 |
40 |
11 |
46 |
15,9 |
35 |
|
7,8 |
45 |
8,4 |
39 |
12 |
37 |
16,1 |
36 |
|
7,9 |
36 |
8,5 |
32 |
13 |
36 |
16,3 |
35 |
|
8 |
33 |
|
|
14 |
33 |
16,5 |
36 |
|
|
|
|
|
15 |
35 |
|
|
.4.2 Регистрация спектров хемилюминесценции растворов белка
В отличие от ДНК, белок при облучении не имел
ярко выраженного импульса при 9 Гц (Рисунок 15). Это скорее всего связано с
тем, что молекулярная структура белка не имеет четко выраженной спиралевидной,
правильной формы, такой как у ДНК. Отсюда следует, что форма молекулы является
очень важным признаком проявления резонансного эффекта. Возможно так же, что
помимо ДНК, другие сложные полимерные молекулы, имеющие спиральную форму, имеют
свою собственную резонансную частоту отклика на воздействие ЭМП.
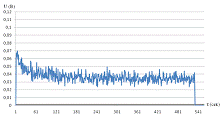
Рисунок 15 - Регистрация световых потоков после облучения раствора белка при частоте 9 Гц
При частоте 7,5 Гц раствор белка имел более
высокие средние показания напряжения на ФЭУ, чем раствор белка, облученный при
9 Гц (Рисунок 16).
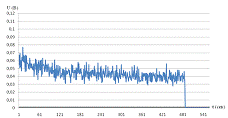
Рисунок 16 - Регистрация световых потоков после облучения раствора белка при частоте 7,5 Гц.
В целом белок в виду своей конформационной сложности и неправильной геометрии, сильно уступает ДНК по величине резонансного отклика на излучение.
График максимальных значений релаксационных
частот для растворов белка с концентрацией 40,9 г/л альбумина сывороточного
вследствие этого отличается короткими пиками, не превышающие 0,060 В как это
видно на рисунке 17.
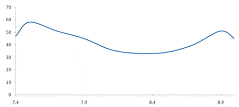
Рисунок 17 - График релаксационных частот
максимальных значений напряжения ФЭУ для раствора сывороточного альбумина с
концентрацией 40,9 г/л.
В таблицу 6 сведены значения максимумов
интенсивности хемилюминесценции водных растворов ДНК для каждой применяемой
частоты ЭМП.
Таблица 6 - Значения максимумумов напряжения хемилюминесценции в зависимости от частоты облучения водных растворов сывороточного альбумина с концентрацией 40,9 г/л.
|
ν (Гц) |
7,4 |
7,5 |
7,7 |
7,9 |
8,3 |
8,5 |
8,7 |
8,9 |
9 |
|
|
U (В) |
58 |
47 |
51 |
45 |
36 |
33 |
34 |
40 |
51 |
45 |
.5 Предполагаемое создание полимерной матрицы и
осаждение на нее ДНК-структур
Как уже упоминалось, ДНК является спиралевидной, близкой к правильной симметрии молекулой. Есть предположение, что резонансный эффект возникает за счет изменения собственной энергии молекулы, потому маловероятным является то, что выброс энергии происходит за счет поглощения фотонов столь малой энергии.
Полагаю, что молекула ДНК испытывает искривление под воздействием резонансного излучения, при этом очень важную роль играет вода. Без нее резонансный эффект не возможен. Возможно, искривление происходит за счет спинового изменения знака атомов в молекуле ДНК. Поэтому, на молекулу действует только магнитное поле, а не электромагнитное поле в целом.
Искривление структуры происходит в промежуток времени, когда через воду проникает излучение. Когда оно кончается, начинается возврат формы ДНК в стабильное состояние и при этом меняется состояние химических соединений в ДНК, которое и провоцирует излучение.
Возможности эксперимента предусматривают создание некоторых устройств для прикладного использования этого эффекта.
Оказалось актуальным осаждение ДНК молекул на положительно заряженную полимерную матрицу для создания датчика отклика тепловых фотонов. В таком датчике можно было бы количественно менять сумму фотонов излучаемое ДНК, за счет изменения площади облучения самой полимерной матрицы.
Структуры ДНК нужно наносить из капель рабочего раствора (раствора буфера, водно-спиртовой среды и т.п.) на поверхность слюды, модифицированной ионами двух (и более) валентных металлов. Эти ионы, служат связующими мостиками между отрицательно заряженной слюдой (в водных растворах) и отрицательно заряженными фосфатными группами молекулы ДНК. Модификация слюды может предшествовать процессу адсорбции макромолекул - в этом случае свежесколотую слюду помещают для предварительной обработки на некоторое время в раствор, содержащий катионы металлов, затем промывают и высушивают. После этого на модифицированную поверхность наносят рабочий раствор с исследуемыми структурами.
После того как рабочий раствор нанесен,
полимерную матрицу нужно поместить в небольшой слой воды и изолировать тонкой и
твердой оболочкой. Затем данную подложку необходимо подобрать резонансное ЭМИ
НЧ и попытаться зарегистрировать импульсы электро-магнитного излучения с
подложки. Достоинство данного метода будет в том, что можно будет работать с
поверхностью и при этом достаточно точно предсказать то резонансное излучение,
которое будет поступать.
Заключение
В ходе выполнения дипломной работы были сделаны следующие результаты:
1 Количественно выделено ДНК из различного биологического материала и проведение ПЦР с целью получения коротких ампликонов.
2 Проведена обработка водных растворов нуклеиновых кислот, их ампликонов и растворов белка ЭМП НЧ.
Изучены зависимости интенсивностей хемилюминесценции модельных растворов нуклеиновых кислот и водных растворов белков (альбумина) от различных параметров ЭМП НЧ.
Определены степени влияния ЭМП низких частот на водные модельные растворы ДНК.
Теоретические обоснованы эффекты флуоресценции растворов сложных органических молекул.
Предложены пути возможного применения полученных результатов для создания нанотехнологичных устройств шифрования информации.
Связывание ОН - группы после обработки ЭМП НЧ вызывает изменение рН растворов ампликонов ДНК, что может приводить к разрывам водородных связей в макромолекулах ДНК, нарушению стейкинга ее оснований, в целом к изменению конформации спирали. При переходе системы (водного раствора ампликонов ДНК) в первоначальное состояние происходит испускание энергии, которое и фиксируется на спектрах хемилюминесценции.
Кроме того, свойства воды в гидратационном слое заметно отличаются от свойств обычной воды. Среднее время жизни водородных связей в гидратационном слое в 5-10 раз больше, чем в воде. Время жизни водородных связей между полярными группами макромолекулы (ампликонов ДНК) и поверхностными молекулами воды также заметно больше, чем время жизни водородных связей между двумя молекулами воды в чистой воде. Флуктуация плотности, а также такие свойства воды, как трансляционная диффузия или ориентационная релаксация значительно замедлены в гидратационном слое.
Мы полагаем, что изменение гидратационной оболочки ДНК под действием низкочастотного электромагнитного поля, возможно, также приводит к восстановлению водородных связей, образованию сшивок и в целом к репарации ДНК, что согласуется с мнением ряда авторов.
Имея разные свойства по отношению к
гидратационной оболочке макромолекул, ЭМП НЧ способно существенно влиять на
равновесные концентрации функционально важных состояний биологических
макромолекул in vivo и таким образом способно оказывать влияние на
функциональные метаболические свойства биосистем.
Список использованных источников
1. Формирование нанокластеров в водной среде под действием электромагнитного поля / М.Г. Барышев, Н.С. Васильев, С.С. Джимак и др. // Труды международной научно-практической конференции "Перспективные нано и биотехнологии в производстве продуктов функционального назначения" Краснодар, 2007. - С. 39-40.
. Кухлинг Х. Справочник по физике / Х. Кухлинг. - М.: Мир, 1983. - 310 с.
3. Долуханов М.П. Распространение радиоволн / М.П. Долуханов. - М.: Связь, 1972. - 37 с.
4. Schlegel K. Weltweite Ortung von Blitzen: 50 Jahre Schumann-Resonanzen / K. Schlegel, M. Schlegel // Füllekrug Weltweite. - 2002. - Vol. 1. - P. 256-261.
5. Бартон Д. Общая органическая химия / Д. Бартон, У.Д. Оллис. - М.: Химия, 1986. - С. 32-40.
. Страйер Л. Биохимия / Л. Страйер. - М.: Мир, 1985. Т. 3. С. 6-16.
. Антонов А.Н. Строение ДНК и положение организмов в системе / А.Т. Антонов. - М.: Полином, 2002. - 238 с.
. Мушкамбаров Н.Н. Молекулярная биология / Н.Н. Мушкамбаров, С.Л. Кузнецов. - М.: Медицинское информационное агентство, 2007. - С. 53-55.
. Айала Ф. Современная генетика / Ф. Айала, Дж. Кайгер. - М.: Мир, 1986. - 97 с.
. Коничев А.С. Молекулярная биология / А.С. Коничев, Г.А. Севастьянова. - М.: Академия, 2003. - С. 46-51.
. Щелкунов С.Н. Генетическая инженерия / С.Н. Щелкунов. - М.: Сибирское университетское издательство, 2004. - С. 48-53.
. Ребриков Д.В. ПЦР "в реальном времени" / Д.В. Ребриков, Г.А. Саматов, Д.Ю. Трофимов. - М.: БИНОМ, 2009. - 10 с.
. Ленинджер А. Основы биохимии / А. Ленинджер. - М.: Мир, 1985. - С. 43-46.
14. Validation of a method based on polymerase chain reaction for the detection of genetically modified organisms in various processed foodstuffs / M. Lipp, A. Eyquem, L. Kruse et al. // Euro. F .Res. Tech. - 2012. - Vol. 13. - №3. - P. 497-504.
. Lakowicz R. J. Principles of Fluorescence Spectroscopy / R. J. Lakowicz // N.Y.: Springer Science. - 2006. - Vol.2. - №5. - P. 3-12.
16. Лакович. Дж. Основы флуоресцентной спектроскопии / Дж. Лакович. - М.: Мир, 1986. - С. 10-15.
. Chemiluminescence - based detection principles and analytical / Baeyensa W. R. G, Schulman S. G, Calokerinos A.C, Zhao Y et al. // Elsevier. - 1997. - Vol. 7. - №7. - P. 101-120.
. Dodeigne C. Chemiluminescence as diagnostic tool / C. Dodeigne, L. Thunus, R. Lejeune // Elsevier. - 2001. - Vol. 2. - №3. - P. 120-129.
19. Берковский А.Г. Вакуумные фотоэлектронные приборы / А.Г. Берковский, В.А. Гаванин, И.Н. Зайдель. - М.: Прибормаш, 1976. - С. 56-57.
. Бучаченко А.Л. Новые механизмы биологических эффектов электромагнитных полей / А.Л. Бучаченко, Д.А. Кузнецов, В.Л. Бердинский // Биофизика сложных систем. - 2006. - Т. 51.- №3. - С. 545-552.
. Новиков В.В. Комбинированное действие слабых постоянного и переменного низкочастотного магнитных полей, на ионные токи в водных растворах аминокислот / В.В. Новиков, М.Н. Жадин // Биофизика. - 1997. - Т. 39. - №3. - C. 537-548.
. Емец Б.Г. О физическом механизме влияния низкоинтенсивного электромагнитного излучения на биологические клетки / Б.Г Емец // Биофизика. -1999. - Т. 44. - №3. - С. 555-558.
. Новиков В.В. Инициирующее действие слабых магнитных полей на образование межмолекулярных связей в водных растворах аминокислот / В.В. Новиков // Биофизика. - 1994. - Т. 39. №5. - С. 344-412.
. Воздействие низкоэнергетического миллиметрового электромагнитного излучения на стабильность молекул ДНК в растворе / Ю.С. Бабаян, А.Ш. Маркарян, В.П. Калантарян и др. // Биофизика. - 2007. - Т. 52. - №2. - С. 382-383.
. Акопян С.Н. Исследование удельной электропроводности воды при воздействии постоянного магнитного поля, электромагнитного поля и низкочастотных механических колебаний / С.Н. Акопян // Биофизика. - 2005. - Т. 50. - №2. - С. 265-270.
.
Влияние слабых магнитных полей на свойство ряда белков и полиаминокислот
образовывать комплексы с ДНК / В.В. Новиков, В.В. Кувичкин, Н.Н. Новикова, и
др. // Биофизика. - 2000. - №2. - С. 240-244.