Материал: Изучение воздействия электромагнитного поля на водные растворы белков и ДНК
Изучение воздействия электромагнитного поля на водные растворы белков и ДНК
Министерство образования и науки Российской Федерации
Федеральное государственное бюджетное образовательное учреждение
высшего профессионального образования
"Кубанский государственный университет"
(ФГБОУ ВПО "КубГУ")
Физико-технический факультет
Кафедра
радиофизики и нанотехнологий
Допустить к защите в ГАК
Заведующий кафедрой
д-р физ.-мат. наук, профессор
Г.Ф. Копытов
Выпускная квалификационная работа бакалавра
Изучение
воздействия электромагнитного поля на водные растворы белков и ДНК
Работу выполнил
Хачатрян Андраник Шотаевич
Научный руководитель
канд. хим. наук, доцент
Е.Е. Текуцкая
Нормоконтролер
канд. хим. наук М.Е. Соколов
Краснодар 2014
Реферат
Дипломная работа: 49 с., 17 рисунка, 6 таблиц, 26 источников.
Нуклеиновые кислоты, низкочастотное электромагнитное излучение, хемилюминисценция, флюоресценция.
Объектом исследования данной работы являются водные растворы нуклеиновых кислот и белков, выделенных из биологического материала.
Целью данной работы являлось изучение действия низкочастотного электромагнитного излучения на водные растворы нуклеиновых кислот и белков.
В процессе выполнения работы были получены ДНК
из цельной крови и белок из сыворотки крови. Было изучено влияние отклика
электромагнитного поля на нуклеиновые и белковые структуры, а так же были
изучены релаксационные частоты спектров. Намечены пути дальнейшего применения
биологических структур для создания нанотехнологичных устройств, а именно
устройств, для хранения и шифрования информации.
Содержание
белок нуклеиновый хемилюминесценция электромагнитный
Обозначения и сокращения
Введение
. Литературный обзор
.1 Электромагнитное излучение. Радиоволны
.2 Дизоксирибонуклеиновая кислота (ДНК)
.2.1Физико-химические свойства ДНК
.2.2 Репликация и трансляция
.2.3 Репарация
.2.4 Полимеразная цепная реакция (ПЦР)
.2.5 Белковые структуры
.3 Методы люминесценцентного анализа
.3.1 Флуоресценция
.3.2 Теоретические основы флуоресценции
.3.3 Хемилюминесценция
.3.4 Фотоэлектронный умножитель
.4 Механизмы биологических эффектов электромагнитных полей
.4.1 Комбинированное действие слабых постоянного и переменного НЧ магнитных полей на ионные токи в водных растворах аминокислот
.4.2 Инициирующее действие слабых магнитных полей на образование межмолекулярных связей в водных растворах аминокислот
.4.3 Воздействие низкочастотного миллиметрового ЭМИ на стабильность молекул ДНК в растворе
.4.4 Влияние слабых магнитных полей на свойства ряда белков и полиаминокислот образовывать комплексы с ДНК
. Экспериментальная часть
.1 Выделение ДНК из различного биологического материала
.2 Проведение ПЦР с целью получения коротких ампликонов
.3 Схема и режим установки для облучения образцов
.3.1 Устройство хемилюминометра
.4 Обработка водных растворов нуклеиновых кислот и их ампликонов ЭМИ. Обработка белковой структуры (альбумина) ЭМИ
.4.1 Снятие спектров хемилюминесценции модельных растворов нуклеиновых кислот
.4.2 Регистрация спектров хемилюминесценции раствора белка
.5 Предполагаемое создание полимерной матрицы и осаждение на нее ДНК-структур
Заключение
Список
использованных источников
Обозначения и сокращения
ЭМП - электромагнитное поле
НЧ - низкая частота
ФЭУ - фотоэлектронный умножитель
ДНК - дезоксирибонуклеиновая кислота
ПЦР - полимеразная цепная реакция
ВКО - внутренний контрольный образец
ОКО - отрицательный контрольный образец
Введение
В настоящее время накопилось достаточно большое количество достоверных экспериментальных данных о нетепловых эффектах электромагнитных полей низкой частоты (ЭМП НЧ), а также о чрезвычайно высокой чувствительности к электромагнитным полям живых организмов самых различных классов - от одноклеточных до человека. Особый интерес привлекают биополимеры на основе нуклеиновых кислот. Многочисленными экспериментами установлено, что в молекуле ДНК возможен перенос заряда на большие расстояния, а также возможно испускание фотонов при возбуждении или после возбуждения молекулы ДНК. Кроме того в работах указывается, что некоторые вирусные ДНК-последовательности могут индуцировать низкочастотные электромагнитные волны в водных растворах высокой степени разведения.
На сегодняшний день, во многих исследовательских институтах зарубежья и России ведутся активные исследовательские работы над биополимерами на основе нуклеиновых кислот и белков. В частности их облучение низкочастотным электромагнитным полем и их способностью откликаться потоком фотонов теплового спектра. Эти факты открывают перспективы в бионанотехнологии и наноэлектронике [1].
Актуальность данной работы связана с возможностью использования молекул ДНК в качестве переносчика информации и создания новых типов наноструктурных устройств для регистрации электромагнитного излучения.
Целью данной работы являлось изучение воздействия ЭМП НЧ на ДНК и белки растворы методом хемилюминесценции.
Задачи работы:
Выделение ДНК из различного биологического материала.
Проведение ПЦР с целью получения коротких ампликонов.
Обработка водных растворов нуклеиновых кислот и их ампликонов ЭМП НЧ.
Изучение зависимости интенсивности хемилюминесценции модельных растворов нуклеиновых кислот и водных растворов белков (альбумина) от различных параметров ЭМП НЧ.
Определение степени влияния ЭМП низких частот на водные модельные растворы ДНК.
Теоретические объяснения эффектов флуоресценции растворов сложных органических молекул.
Описание возможных применений
полученных результатов для создания нанотехнологичных устройств шифрования информации.
1. Литературный обзор
.1 Электромагнитное излучение. Радиоволны
Электромагнитное излучение - возмущение
электромагнитного поля, распространяющееся в пространстве. Среди
электромагнитных полей вообще, порожденных электрическими зарядами и их движением,
принято относить собственно к излучению ту часть переменных электромагнитных
полей, которая способна распространяться наиболее далеко от своих источников -
движущихся зарядов, затухая наиболее медленно с расстоянием (таблица 1) [2].
Таблица 1- Спектр электромагнитных частот

Радиоволны - электромагнитные волны с частотами
определенного спектра, от ![]() до
до ![]() Гц.
Гц.
В данной работе используются электромагнитные
колебания крайне низкой частоты (КНЧ). КНЧ - это диапазон частот от 3-30 Гц.
Энергия фотонов такого излучения![]() колеблется от
12,4-124 фэВ [3].
колеблется от
12,4-124 фэВ [3].
Резонанс Шумана - явление образования стоячих
электромагнитных волн низких и сверхнизких частот между поверхностью Земли и
ионосферой (рис. 1).
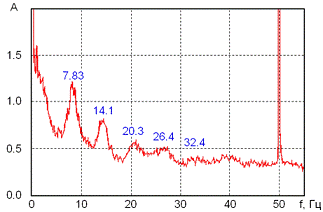
Рисунок 1 - Типичный спектр электромагнитных
колебаний сверхнизкой частоты с резонансами Шумана. Пик на 50 Гц обусловлен
частотой переменного тока в промышленной электросети.
Частота резонанса Шумана составляет 7,83 Гц.
Из-за волновых процессов плазмы внутри Земли наиболее чётко наблюдаются пики на
частотах примерно 8, 14, 20, 26, 32 Гц. Для основной, самой низкой частоты,
возможны вариации в пределах 7-11 Гц, но большей частью в течение суток разброс
резонансных частот обычно лежит в пределах ±(0,1-0,2) Гц. Спектральная
плотность колебаний составляет 0,1 мВ/м [4].
.2 Дезоксирибонуклеиновая кислота (ДНК)
Дезоксирибонуклеиновая кислота (ДНК) - молекула наследственности. ДНК - очень длинная нитевидная молекула, состоящая из большого числа рибонуклеотидов.
Пуриновые и пиримидиновые основания ДНК несут
генетическую информацию, тогда как сахарные и фосфатные группы выполняют
структурную роль. (Рис. 2) ДНК содержит четыре типа основания: два пуриновых
основания - аденин и гуанин; два пиримидиновых основания - тимин и цитозин.
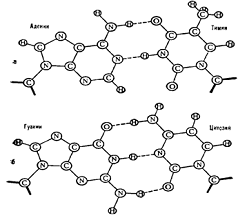
Рисунок 2 - Водородные связи в структуре ДНК
(а-аденин-тимин, б-гуанин-цитозин)
Для обеспечения основных характеристик клеток и
организмов данной популяции необходимо точное хранение структуры и стабильности
функций генетического материала на протяжении тысяч и миллионов лет, несмотря
на действие различных мутагенных факторов. Для поддержания стабильной функции
ДНК существует несколько механизмов. Во-первых, это высокая химическая
стабильность самой молекулы ДНК, а во-вторых, - наличие специальных механизмов
самокоррекции и репарации возникающих изменений. Генетическая информация может
надежно храниться в нуклеотидных последовательностях ДНК только том, что
широкий набор различных репликационный ферментов осуществляет непрерывный
"осмотр" ДНК и удаляет из нее повреждённые нуклеотиды [5].
.2.1 Физико-химические свойства ДНК
Изучение межнуклеотидных связей в ДНК показало строгую их однотипность. Во всех случаях связь между дезоксирибонуклеотидными остатками в цепи главных валентностей ДНК осуществляется за счет образования фосфатного мостика между третьим и пятым гидроксилами дезоксирибозных компонентов двух соседних дезоксирибонуклеотидных остатков (Рисунок 3).
Никаких разветвлений в цепи ДНК нет. Все природные ДНК представляют собой частицы с очень большим молекулярным весом (4-16 млн., а в случае ДНК из фагов до 150 млн.) и состоят из десятков тысяч нуклеотидов.
ДНК хорошо растворяются в воде, в слабых и
крепких водносолевых растворах, образуя вязкую жидкость; осаждается 2-3
объемами 96%-ого этанола, образуя студнеобразный или волокнистый осадок. ДНК
денатурирует при нагревании водных растворов до 100˚, при их подкислении
(до pH 1-2) или подщелачивании (до pH 10-12). При кислотном гидролизе
происходит отщепление пуринов и частичный гидролиз эфирных связей в молекуле
ДНК; при мягком кислотном гидролизе ДНК удается получить апуриновую ДНК.
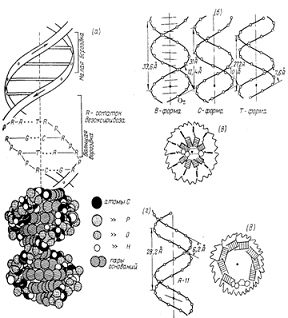
Рисунок 3 - Модели ДНК. Спираль Уотсона - Крика
При нагревании с гидразином расщепляется
пиримидиновые основания - образуется апиримидиновая ДНК. При действии на ДНК
дизоксирибонуклеазы происходит гидролиз основных фосфоэфирных связей ДНК.
Изучение природных ДНК из различных организмов показало, что они неодинаковы
как биологически, там и химически, и каждый вид организмов характеризуется,
по-видимому, своей специфической ДНК [6].
.2.2 Репликация и трансляция
Репликация - процесс синтеза дочерней молекулы дезоксирибонуклеиновой кислоты на матрице родительской молекулы ДНК. В ходе последующего деления материнской клетки каждая дочерняя клетка получает по одной копии молекулы ДНК, которая является идентичной ДНК исходной материнской клетки. Этот процесс обеспечивает точную передачу генетической информации из поколения в поколение.
Трансляция - процесс синтеза белка из аминокислот на матрице информационной (матричной) РНК осуществляемый рибосомой. Принцип комплементарности используется в синтезе ДНК. Это строгое соответствие соединения азотистых оснований, соединёнными водородными связями, в котором аденин соединяется с тимином, а гуанин с цитозном. Это фундаментальное значение для молекулярной биологии. На нем построен механизм самоудвоения ДНК - редупликации, обеспечивающий передачу наследственно информации в момент деления клеток. На протяжении жизни клетки используют этот принцип при считывании с отдельных фрагментов ДНК копий в виде информационных РНК (и-РНК) - в процессе транскрипции. В этом процессе матрицей служит лишь одна из цепей ДНК.
Под действием физических и химических агентов, а
также при нормальном биосинтезе ДНК в ней могут возникать повреждения.
Оказалось, что клетки имеют механизмы исправление повреждений в нитях ДНК.
Способность клеток к исправлению повреждений в молекулах ДНК получила название
репарации [7].
1.2.3 Репарация
Процесс репарации ДНК состоит в том, что генетическая информация представлена в ДНК двумя копиями - по одной в каждом из двух цепей двойной спирали ДНК. Благодаря этому случайное повреждение, в одной из цепей может быть удалено репликационный ферментом и поврежденный участок цепи возвращается в свой нормальный вид за счет информации, содержащейся в неповрежденной цепи. По времени осуществления в клеточном цикле различают дорепликативную, репликативную и пострепликативную репарацию.
Дорепликативная репарация - это процесс восстановления поврежденной ДНК к ее удвоению. В простейших случаях разрывы могут быть восстановлены ферментом лигазы. В других случаях используется полная ферментативная система репарации.
Репликативная репарация - это совокупность процессов восстановления ДНК в ходе репликации. При этом поврежденный участок удаляется на протяжении репликации в зоне роста цепи. В обеспечении высокой точности репликации значительная роль принадлежит механизму самокоррекции, который осуществляется ДНК-полимеразой или тесно связанным с ней ферментом эндонуклеазой. Этот процесс связан с определением ошибки включенного в цепь нуклеотида, отщеплением его и заменой на соответствующий. В результате этого частота ошибок снижается в 10 раз. Пострепликативная репарация и ее механизм точно не изучен. При пострепликативной репарации происходит вырезание поврежденного участка и сшивания концов. При этом клетка может сохранять жизнеспособность и передавать дефектную ДНК дочерним клеткам. Допускают возможность разных вариантов синтеза ДНК на поврежденной матрице.
По механизмам развития репарации различают: эксцизионную, неэксцизионную и рекомбинативную репарацию. При эксцизионной репарации устраняются повреждения, появившиеся под воздействием ионизирующей радиации, химических веществ и других факторов. Это основной тип репарации, обнаружен как у прокариот, так и в клетках эукариот. Эксцизионная репарация ДНК отличается тем, что не только разрезаются димеры (как при световой), но и вырезаются большие участки молекулы ДНК (до нескольких сотен нуклеотидов). Очевидно, могут удаляться цепи генов, после чего происходит комплементарный матричный синтез с помощью фермента ДНК-полимеразы.
На основе одной из предложенных моделей установлены пять последовательных этапов эксцизионной репарации:
"Распознавания" повреждения ДНК эндо-нуклеаз.
Разрезание эндонуклеазы одного из цепей молекулы ДНК вблизи повреждения.
"Вырезание" поврежденного участка и его расширение экзонуклеазами.
Матричный синтез новой цепи ДНК-полимеры (репаративная репликация).
Повторное соединение участков с нитью ДНК под влиянием фермента ДНК-лигазы [8].
Способность к репарации была обнаружена у бактерий, подвергались воздействию ультрафиолетовых лучей. В результате облучения целостность молекул ДНК нарушается, потому что у них возникают димеры, т.е. сцеплены между собой соседние пиримидиновые основания. Димеры могут формироваться между двумя тиминами, тимин и цитозин, двумя цитозинами, тимином и урацилом, двумя урацилами. Однако облученные клетки на свете выживают гораздо лучше, чем в темноте. После тщательного анализа причин этого явления установлено, что в поврежденных клетках на светлые происходит репарация ДНК (фоторепарация). Она осуществляется специальным ферментом ДНК-фотолигазою, которая активируется квантами видимого света. Фермент соединяется с поврежденной ДНК, разъединяет связи в димерах и восстанавливает целостность нити ДНК. ДНК-фотолигаза фотореактивизируется и не может является видоспецифичной к ним, то есть действует на различные виды ДНК. В нем есть циано - кобаламин (витамин В12), поглощающий кванты видимого света и передает энергию молекуле фермента. На ранних стадиях эволюции живых организмов, когда отсутствовал озоновый экран, который задерживает большую часть потока губительных для организмов солнечных ультрафиолетовых лучей, фоторепарация играла особенно важную роль.