Материал: Изучение воздействия электромагнитного поля на водные растворы белков и ДНК
Если, например, димеры тимина не устранены до рекомбинации, то это приводит к изменению структуры дочерних ДНК. Такие нарушения могут присутствовать непосредственно в процессе кроссинговера. Но при этом не происходит устранение димера, он удаляется уже после репликации.
Способность клеток осуществлять эффективную
репарацию генетического материала может иметь значение также в клеточных
механизмах старения. Существуют наблюдения, что линии мышей-долгожителей
отличаются более стабильными хромосомами, а у мышей с непродолжительным сроком
жизни хромосомы характеризуются большим повреждением, возникновением
структурных аберраций, которые являются следствием нарушения процессов
репарации. Существуют наблюдения, свидетельствуют о снижении интенсивности
процессов репарации ДНК с возрастом. Но трудно сказать, эти изменения - причина
старения организма, или его следствие [9].
.2.4 Полимеразная цепная реакция (ПЦР)
Полимеразная цепная реакция - один из мощнейших инструментов исследования нуклеиновых кислот, не доступный ранее. ПЦР используют для анализа индивидуальных вариаций нуклеотидных последовательностей в определенных локусах, для повышения эффективности клонирования целевых последовательностей изучаемых геномов и их прямого секвенирования, для детекции патогенных микроорганизмов и. т. п.
Другими словами это экспериментальный метод молекулярной биологии, позволяющий добиться значительного увеличения малых концентраций определённых фрагментов нуклеиновой кислоты (ДНК) в биологическом материале. Ход реакции:
Денатурация - двухцепочечную ДНК-матрицу нагревают до 94-96°C (или до 98°C, если используется особенно термостабильная полимераза) на 0,5-2 мин, чтобы цепи ДНК разошлись.
Отжиг - в момент расхождения цепей, температуру понижают, чтобы праймеры могли связаться с одноцепочечной матрицей.
Элонгация - ДНК-полимераза реплицирует
матричную цепь, используя праймер в качестве затравки [10, 11].
.2.5 Белковые структуры
Белки - это высокомолекулярные соединения, у
которых сотни и даже тысячи остатков α-аминокислот
соединены друг с другом кетоимидными (пептидными) связями (-CO-NH-), образуя длинные
цепи главных валентностей - полипептидные цепи:
![]() (1)
(1)
где R’,R",R"’ … - боковые группы или
боковые цепи у отдельных аминокислотных остатков. Пептидные связи образуются
путем отщепления воды от карбоксильной группы одной аминокислоты и аминогруппы
другой. В состав белков входят остатки более 20 различных аминокислот.
Структура белков характеризуется не только химическим составом и порядком
чередования различных аминокислотных остатков в полипептидной цепи, но так же и
расположением этих цепей в пространстве, что обуславливает существование
практически необозримого множества белков с разнообразными свойствами. В белках
различают четыре порядка морфологической организации или четыре структуры.
Первый порядок, или первичная структура, - полипептидная цепь с определенной
последовательностью чередования аминокислотных остатков. Второй порядок - та
пространственная конфигурация, которую принимает сама полипептидная цепь.
Вторичной структурой может быть, например α-спираль
Полинга - Кори, имеющая 3,7 аминокислотных остатков в одном витке. Третий
порядок - конфигурация, возникающая в результате складывания или закручивания
структур, соответствующих второму порядку.
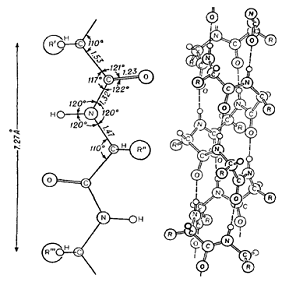
Рисунок 4 - Схемы первичной и вторичной белковой
структуры
Четвертый порядок - объединение нескольких
частиц с третичной структурой в одну более крупную частицу [12, 13].
.3 Методы люминесценцентного анализа
Люминесценция представляет собой особый вид излучения, избыточное над тепловым и продолжающееся в течение времени, значительно превышающий период световых колебаний. Вообще говоря, люминесценцию следуют отличать от светового рассеяния и от светового отражения тем, что при ней в периоды между поглощением и испусканием, происходят процессы промежуточного характера, длительность которых превышает период световой волны. Люминесценцию часто называют холодным свечением.
Люминесценцию следует классифицировать по длительности, механизму преобразования и накапливания энергии, а так же по временным характеристикам излучения. А именно:
Фотолюминесценцию - возбуждение светом.
Электролюминесценцию - возбуждение электрическим полем.
Триболюминесценцию - возбуждение при механических воздействиях.
Хемилюминесценцию - возбуждение, протекающее в химических реакциях.
По длительности свечения различают как флуоресценцию (быстро затухающая люминесценция) и фосфоресценция (длительная люминесценция). По механизму процессов различают как спонтанную, резонансную, вынужденную и рекомбинационную люминесценцию.
В данной работе рассматривается возбуждение,
протекающее в химических реакциях, т.е. хемилюминесценция. Так как в данной
работе используется метод хемилюминесценции, то следует рассмотреть основные
особенности флуоресценции и хемилюминесценции, принцип работы хемилюминометра,
а так же работу фотоэлектронного умножителя как один из основных элементов
хемилюминометра [14].
.3.1 Флуоресценция
Флуоресценция - люминесценция, затухающая в течение короткого времени. Разделение люминесценции на флуоресценцию и фосфоресценцию устарело, приобрело условный смысл качественной характеристики её длительности. По механизму преобразования энергии возбуждения флуоресценция, как правило, является спонтанной люминесценцией, поэтому её длительность определяется временем жизни на возбуждённом уровне энергии (в случае запрещённых переходов флуоресценции в этом смысле может иметь значительную длительность).
Флуоресценция наблюдается в атомных и молекулярных
газах. Многие органические вещества обладают флуоресценцией в жидких и твердых
растворах, а также в кристаллическом состоянии. Спектры флуоресценции, её
поляризация и кинетика связаны со структурой и симметрией центров люминесценции
или молекул, характером их взаимодействия, зависят от концентрации растворов,
вида возбуждения и т.д. Поэтому с помощью флуоресценция изучают структуру
вещества и физические процессы, происходящие в них. Флуоресценцию используют в
люминесцентном анализе, сцинтилляционных счётчиках, дефектоскопии,
микробиологии, медицине, биофизике и т.д. [15].
.3.2 Теоретические основы флуоресценции
Флуоресценция - физический процесс,
разновидность люминесценции. Флуоресценцией обычно называют излучательный
переход возбужденного состояния с самого нижнего синглетного колебательного
уровня S1 в основное состояние S0. В общем случае флуоресценцией называют
разрешенный по спину излучательный переход между двумя состояниями одинаковой
мультиплетности: между синглетными уровнями ![]() или
триплетными
или
триплетными ![]() . Типичное время
жизни такого возбужденного состояния составляет 10−11−10−6 с.
Флуоресценцию следует отличать от фосфоресценции - запрещенного по спину
излучательного перехода между двумя состояниями разной мультиплетности.
. Типичное время
жизни такого возбужденного состояния составляет 10−11−10−6 с.
Флуоресценцию следует отличать от фосфоресценции - запрещенного по спину
излучательного перехода между двумя состояниями разной мультиплетности.
Согласно представлениям квантовой химии, электроны в атомах расположены на энергетических уровнях. Расстояние между энергетическими уровнями в молекуле зависит от её строения. При облучении вещества светом возможен переход электронов между различными энергетическими уровнями (Рисунок 5).
После поглощения света часть полученной системой
энергии расходуется в результате релаксации. Часть же может быть испущена в
виде фотона определённой энергии. Разница энергии между энергетическими
уровнями и частота колебаний поглощенного света соотносятся между собой
уравнением (III постулат Бора):
![]() (2)
(2)
где ![]() и
и
![]() -
энергия перехода
-
энергия перехода
hν - общая энергия
фотона
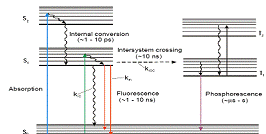
Рисунок 5 - Схема энергетических переходов в
молекуле при возникновении люминесценции.
Квантовый выход флуоресценции показывает, с какой эффективностью проходит данный процесс. Он определяется как отношение количества испускаемых и поглощаемых фотонов.
Квантовый выход флуоресценции может быть
рассчитан по формуле:
![]() (3)
(3)
где ![]() -
количество испускаемых в результате флуоресценции фотонов
-
количество испускаемых в результате флуоресценции фотонов
![]() - общее количество
поглощаемых фотонов.
- общее количество
поглощаемых фотонов.
Ф - квантовый выход флуоресценции [16].
1.3.3 Хемилюминесценция
Хемилюминесценция - сверхравновесное излучение,
яркость которого превышает яркость температурного излучения. При прохождении
химической реакции и происходит отступление от равновесия. Хемилюминесценция
является частным случаем люминесценции (Рисунок 6).
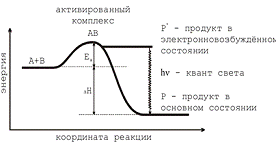
Рисунок 6 - Энергетика процесса
хемилюминесценции для реакции A+B+AB …реакция…->Р+hν
Процесс хемилюминесценции в общем случае принято делить на две стадии:
Стадия возбуждения - образование при прохождении химической реакции с достаточной энергией продукта реакции (Р) в возбужденном состоянии (Р*) в котором излучательный переход возможен:
+B+ …реакция…->Р* +К+М+… (другие продукты)
(4)
Стадия люминесценции: Р* -> люминесценция
-> P + ![]()
Интенсивность излучения и скорость реакции
связаны соотношением:
![]() γ;
(5)
γ;
(5)
где ![]() число
молекул продукта, образующееся в единицу времени в единицу объема;
число
молекул продукта, образующееся в единицу времени в единицу объема;
![]() - квантовый выход
возбуждения, это отношение числа возбужденных молекул к общему числу образующихся
молекул;
- квантовый выход
возбуждения, это отношение числа возбужденных молекул к общему числу образующихся
молекул;
![]() квантовый выход
люминесценции отношение числа молекул Р*, отдавших энергию в виде излучения, к
общему числу возбужденных молекул; интенсивность самой хемилюминесценции
квантовый выход
люминесценции отношение числа молекул Р*, отдавших энергию в виде излучения, к
общему числу возбужденных молекул; интенсивность самой хемилюминесценции
![]() число фотонов
излучаемых из единицы объема реагирующей смеси за единицу времени.
число фотонов
излучаемых из единицы объема реагирующей смеси за единицу времени.
Хемилюминесценция возникает при многих химических реакциях - например, при рекомбинации свободных радикалов или в реакциях окисления (при свободнорадикальном окислении паров белого фосфора в газовой фазе, окислении люминола в водном растворе и т.п.). В этом случае, как и в реакциях биолюминесценции, выделяющаяся энергия не рассеивается в виде тепла, как это происходит в ходе большинства экзотермических химических реакций, а расходуется на образование одного из продуктов реакции в возбуждённом электронном состоянии. Для излучения света в ходе хемилюминесцентной реакции необходимо выполнение, как минимум, двух условий: во-первых, энергия, выделяющаяся в ходе реакции должна превышать ~41-71,5 ккал/моль и, во-вторых, разница энергий основного и возбуждённого состояния продукта реакции должна быть ниже энтальпии химической реакции.
При соблюдении этих условий возможно образование
с достаточно высоким выходом окисленной формы люциферина в возбуждённом
состоянии и дальнейший переход в основное состояние с испусканием фотона
видимого спектрального диапазона. Отношение числа излученных фотонов к общему
числу элементарных актов реакции называется квантовым выходом реакции,
квантовые выходы биолюминесценции, в отличие от большинства хемилюминесцентных
реакций, очень высоки и достигают значений 0,1-1. Такие квантовые выходы для
реакций, протекающих в водных растворах при нейтральных значениях pH необычны для
хемилюминесцентных процессов и обусловлены специфичной ферментативной природой
окислительных реакций биолюминесценции, катализируемых люциферазными
комплексами [17, 18].
.3.4 Фотоэлектронный умножитель
Фотоэлектронный умножитель - прибор для
преобразования слабых световых сигналов в электрические, основанный на
фотоэлектронной и вторичной электронных эмиссиях. Состоит из фотокатода и
нескольких электродов (динодов) с высоким коэффициентом вторичной электронной
эмиссией и коллектора. Напряжение на каждом диноде относительно фотокатода на
50-100 вольт выше, чем у предыдущего. Свет, падающий на фотокатод, вырывает
электронами которые, попадая на диноды, "размножаются", за счёт
вторичной электронной эмиссии. Коэффициент усиления электронного тока:
К= sn (6)
где n - число динодов
Число динодов достигает 109-1011, так что даже
отдельные фотоэлектроны создают на выходе ФЭУ импульсы тока большой амплитуды
[19].
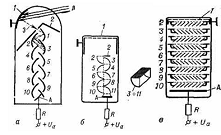
а - с корытообразными динодами, б - коробчатого типа, в - жалюзийного типа; 1 - фотокатод, 2 - экран, 3-11 - диноды, Л - световой поток, А - анод, Э - траектория электронов, R - нагрузка.
Рисунок 7 - Фотоэлектронные умножители разных типов
1.4 Механизмы биологических эффектов
электромагнитных полей
Микроволновое электромагнитное поле может изменять ориентацию углового момента (спина) неспаренного электрона радикала, однако химическая реакционная способность радикала не зависит от ориентации его спина и поэтому индивидуальные радикалы не могут обеспечить ни магнитно-полевых, ни электромагнитных биологических эффектов.
Такие эффекты могут появляться только в условиях, когда имеются пары радикалов или ион - радикалов. Спиновые состояния таких пар - синглетные (с полным электронным спином нуль) или триплетные (со спинов нуль) - сильно различаются по реакционной способности, обнаруживая высокую спиновую селективность. Микроволновое поле может индуцировать спиновые триплет-синглетные переходы в таких парах (спин - селективные нанореакторы), изменять их спиновое состояние и их реакционную способность. Именно эта физически ясная и экспериментально обоснованная концепция лежит в основе микроволновой спиновой химии. Она уже привела к открытию микроволнового изотопного эффекта.
После открытия магнитного изотопного эффекта
магния в реакция фосфорилирования: было показано, что в реакциях
фосфорилирования в митохондриях оба фосфорилирующих фермента (креатинкиназа и
АТФаза) производят аденозинтрифосфат - главный энергоноситель в живых
организмах - с высокой скоростью, если в активном центре фермента находится ион
магния с магнитным ядром магния 25. Ферменты с этим магнитным изотопом работают
почти на порядок активнее, чем с немагнитными изотопами магний 24 и магний 26.
Фактический магнитный изотоп магния 25 (спин ядра S = 5/2, естественное
содержание 11%) является спиновым катализатором биохимической реакции. Это
открытие является прямым и надежным доказательством того, что ключевые
биохимические реакции синтеза энергоносителей в организме происходят в спин -
селективных нанореакторах. Эти реакции зависят от магнитного момента ядер, а
также неизбежно должны зависеть и от магнитного поля, и от резонансного
микроволнового поля [20].
.4.1 Комбинированное действие слабых постоянного и переменного низкочастотного магнитных полей на ионные токи в водных растворах аминокислот
Исследовалось влияние совместного действия
постоянного и переменного магнитных полей на ионный ток через водный раствор
аминокислоты. Обследовались аспарагин, глутаминовая кислота, аргинин и тирозин.
На кривой зависимости тока от частоты переменного поля, параллельного
постоянному, наблюдались отчетливые (30-50% от фонового тока) узкополосные пики
на частотах, близких к циклотронной частоте ионизированной молекулы
соответствующей аминокислоты. Других пиков не отмечалось. Воспроизводилось
эффекта - 100%. При перпендикулярных полях, также как и при отсутствии
постоянного поля эффекта нет. Эффект наблюдается только при очень слабом (0,05
мкТл) переменном поле (рисунок 8). С увеличением амплитуды переменного поля
эффект исчезает. Концентрация аминокислоты ![]() ,
фоновый катодный ток на порядке наноамперов [21].
,
фоновый катодный ток на порядке наноамперов [21].