Материал: Изучение воздействия электромагнитного поля на водные растворы белков и ДНК
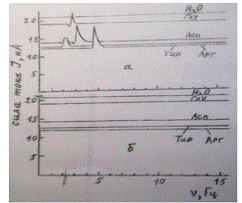
Рисунок 8 - Зависимость силы ионного тока через водный раствор
аминокислоты от частоты переменного поля а - при
![]() =
0,05 мкТл,
=
0,05 мкТл, ![]() = 25 мкТл, б - при
= 25 мкТл, б - при
![]() =
0,05 мкТл и
=
0,05 мкТл и ![]() = 0 мкТ
= 0 мкТ
1.4.2 Инициирующее действие слабых магнитных полей на образование межмолекулярных связей в водных растворах аминокислот
Комбинированное воздействие слабым параллельным постоянным и переменным магнитными полями на раствор глутаминовой кислоты влияет на ионный ток через раствор аминокислоты на определенной частоте переменного тока, соответствующей частоте циклотронного резонанса ионизированной формы молекулы глутаминовой кислоты. Реакция тока на воздействие имеет тонкую структуру, содержащую колебательные компоненты, характеризуется определенными особенностями динамики и ограниченным временем жизни. Суммарная амплитуда эффекта составляет до 30% от уровня фонового тока. При управляемом снижении температуры раствора в процессе воздействия полями происходит формирование устойчивых молекулярных комплексов глутаминовой кислоты, отличающихся по ряду физико-химических характеристик от свободных молекул.
Эксперимент, проведенный авторами [22] заключался в следующем: Кювета находилась в системе, состоящей из двух магнитных катушек, расположенных одна в другой. Оси катушек совпадали. Электродная система в кювете была ориентирована так, чтобы вектор напряженности электростатического поля между электродами был перпендикулярен оси катушек. Катушки располагались в защищенной от внешних магнитных полей зоне в двуслойной камере из пермаллоя с коэффициентом экранирования 58 по постоянному полю. Через одну катушку пропускали постоянный ток, который создавал магнитное поле B в зоне кюветы с неоднородностью менее 1%. Исследования проводились при индукции В = 30 мкТл.
На вторую катушку подавался положительный
синусоидальный сигнал, содержащий постоянную составляющую, равную амплитуде
переменной составляющей, который формировал в кювете однородное переменное
магнитное поле, параллельное постоянному. Проводилось автоматическое сканирование
частоты переменного тока от 1 до 10 Гц со скоростью 0,01 Гц/с. Амплитуда
индукции переменного магнитного поля B составляла 25 нТл. Ионный ток измеряли с
помощью измерительного блока полярографического анализатора до воздействия
переменного поля и во время воздействия при частотном сканировании [23].
.4.3 Воздействие низкоэнергетического миллиметрового электромагнитного излучения на стабильность молекул ДНК в растворе
Исследовано влияние миллиметровых
электромагнитных волн слабой мощности на водно-солевой раствор ДНК, выделенной
из печени здоровых крыс и крыс с саркомой 45. Полученные данные представлены в
табл.2. Из кривых плавления необлученной и облученной ДНК определяли
характеристические параметры температуру и интервал плавления. В зависимости от
длительности облучения интервал плавления практически не меняется, а
термостабильность ДНК увеличивается; при облучении до 90 мин температура
плавления ДНК из опухоли увеличивается на ~1,5°С. Предположено, что увеличение
термостабильности ДНК обусловлено дегидратацией присутствующих в растворе ионов
Na+, вследствие чего повышается эффективность стабилизации двойной спирали
[24].
Таблица 2 - Температура плавления и интервал плавления ДНК, выделенных из печени здоровых крыс и саркомы 45
|
Длительность облучения, мин |
зДНК |
оДНК |
||||||
|
|
|
|
|
|
69,4 ± 0,1 |
7,2 ± 0,2 |
68,8 ± 0,2 |
7,9 ± 0,2 |
|
90 |
70,3 ± 0,2 |
7,2 ± 0,2 |
70,2 ± 0,2 |
7,6 ± 0,2 |
||||
.4.4 Влияние слабых магнитных полей на свойство ряда белков и полиаминокислот образовывать комплексы с ДНК
Белок - нуклеиновые взаимодействия, играют ключевую роль в экспрессии генетической информации в клетке. Связь гистонов и негистоновых белков с хроматином не только определяет нативную конформацию ДНК, но и степень экспрессии тех или иных генов. Поэтому исследование взаимодействий структурных белков ядер с ДНК важно для понимания ее матричной функции в клетке.
Показано, что в предварительная обработка
слабыми комбинированными постоянным (42 мкТл) и низкочастотным переменным
(3,5-5 Гц; 0,06 мкТл) магнитными полями, формально настроенными на циклотронный
резонанс ионов заряженных в естественных условиях аминокислот, белкового
компонента комплекса ДНК-белок приводит к существенному изменению
комплексообразования и формированию комплексов ионного типа, чем в отсутствии
этой обработки [25, 26].
2. Экспериментальная часть
.1 Выделение ДНК из различного биологического
материала
Объектом исследования в данной работе были нуклеиновые кислоты (ДНК, РНК) цельной крови человека и белки. Ампликоны получили из контрольной панели, длина ампликона составляла примерно 410 нуклеотидных пар.
Проведение анализа: Лизирующий раствор и раствор
для отмывки 1 прогрели до температуры 65![]() до полного растворения кристаллов. Отобрали необходимое количество одноразовых
пробирок. Внесли в каждую пробирку по 10 мкл внутренний контрольный образец
(ВКО) и по 300 мл лизирующего раствора. Затем в пробирки с лизирующим раствором
и ВКО внесли 100 мкл проб, используя наконечники с аэрозольным барьером. В
пробирку отрицательного контроля выделения внесли 100 мкл ОКО. В пробирку
положительного контроля выделения внесли 90 мкл ОКО и 10 мкл положительный
контрольный образец (ПКО). Пробы тщательно перемешали на вортексе и прогрели до
5 минут при температуре 65
до полного растворения кристаллов. Отобрали необходимое количество одноразовых
пробирок. Внесли в каждую пробирку по 10 мкл внутренний контрольный образец
(ВКО) и по 300 мл лизирующего раствора. Затем в пробирки с лизирующим раствором
и ВКО внесли 100 мкл проб, используя наконечники с аэрозольным барьером. В
пробирку отрицательного контроля выделения внесли 100 мкл ОКО. В пробирку
положительного контроля выделения внесли 90 мкл ОКО и 10 мкл положительный
контрольный образец (ПКО). Пробы тщательно перемешали на вортексе и прогрели до
5 минут при температуре 65![]() .
.
Процентрифугировали 5 секунд при 5 тыс. об/мин
на микроцетрифуге и использовали для выделения ДНК насадочную жидкость,
перенеся ее в новую пробирку. Тщательно ресуспендировали сорбент универсальный
на вортексе. В каждую пробирку отдельным наконечником добавили по 25 мкл
ресуспендированного сорбента универсального. Перемешали на вортексе, поставив в
штатив на 2 минуты, еще раз перемешали и оставили в штативе на 5 минут. Осадили
сорбент универсальный в пробирках центрифугированием при 5 тыс./об в течение 30
сек. Удалили насадочную жидкость, используя вакуумный отсасыватель и отдельный
наконечник для каждой пробы. Повторяя процедуру отмывки, удалили насадочную
жидкость полностью. Пробирки поместили в термостат при температуре 65![]() на 5 минут, периодически встряхивая на вортексе. Процентрифугировали пробирки
при 12 тыс. об/мин в течение 1 минуты на микроцентрифуге. Насадочная жидкость
содержит очищенную ДНК. Данный метод выделения позволяет получить концентрацию
ДНК в конечном растворе до 30 мкг/мл. ДНК из биопроб выделяли с помощью
коммерческих наборов АмплиСенс - "ДНК-сорб-В", состав которого
приведен в таблице 3.
на 5 минут, периодически встряхивая на вортексе. Процентрифугировали пробирки
при 12 тыс. об/мин в течение 1 минуты на микроцентрифуге. Насадочная жидкость
содержит очищенную ДНК. Данный метод выделения позволяет получить концентрацию
ДНК в конечном растворе до 30 мкг/мл. ДНК из биопроб выделяли с помощью
коммерческих наборов АмплиСенс - "ДНК-сорб-В", состав которого
приведен в таблице 3.
Таблица 3 - Состав набора для выделения ДНК
|
Реактив |
Описание |
Вариант 50 |
Вариант 100 |
||
|
|
|
Объем (мл) |
Кол-во |
Объем (мл) |
Кол-во |
|
Лизирующий раствор |
Прозрачная бесцветная жидкость |
15 |
1 флакон |
30 |
1 флакон |
|
Раствор для отмывки 1 |
Прозрачная бесцветная жидкость |
15 |
1 флакон |
30 |
1 флакон |
|
Раствор для отмывки 2 |
Прозрачная бесцветная жидкость |
50 |
1 флакон |
100 |
1 флакон |
|
Сорбент универсальный |
Суспензия белого цвета |
1,25 |
1 пробирка |
1,25 |
2 пробирка |
|
TE - буфер для элюции ДНК |
Прозрачная бесцветная жидкость |
5,0 |
1 пробирка |
5,0 |
2 пробирка |
.2 Проведение ПЦР с целью получения коротких
ампликонов
Для проведения ПЦР использовали амплификатор
роторного типа "Rotor Gene". Программа амплификации, которая
задавалась на приборе, включала в себя следующее (таблица 4):
Таблица 4 - Параметры проведения ПЦР с помощью Rotor Gene
|
|
Этап |
Температура |
Продолжительность этапа |
Измерение флуоресценции |
Количество циклов |
||||
|
Плавление |
Hold/Удерж. темп |
50 |
15 мин |
- |
1 |
95 |
15 мин |
- |
1 |
|
Отжиг праймеров |
Cycling1/Циклирование |
95 |
5 с |
- |
5 |
||||
|
|
|
60 |
20 с |
- |
|
||||
|
|
|
72 |
15 с |
- |
|
||||
|
Накопление концентрации ампликонов |
Cycling2/Циклирование |
95 |
5 с |
- |
40 |
||||
|
|
|
60 |
20 с |
FAM/Green, JOE/Yellow ROX/Orange Cy5/Red |
|
||||
|
|
|
72 |
15 с |
- |
|
На первом этапе происходит расплетение вторичной
структуры ДНК (плавление) в течение 30 минут. На втором этапе к определенным
участкам ДНК присоединяются праймеры (отжиг праймеров). На заключительном этапе
с помощью находящейся в растворе полимеразы происходит накопление участков ДНК,
ограниченных праймерами.
2.3 Схема установки и режим облучения образцов
Для обработки ДНК раствора и раствора белка ЭМП
низких частот, было использовано специальное оборудование, блок-схема которой
представлена на рисунке 9. Она состоит из генератора ГЗ-118, катушки
индуктивности, имеющей 1200 витков и экранированной камеры. Вектор магнитной
индукции ЭМП, создаваемого катушкой, составляет 30 млТл, удельное сопротивление
катушки 320 Ом, и напряжение на катушке равно 14 В.
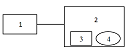
- генератор ГЗ-118, 2 - экранированная камера, 3 - катушка индуктивности, 4 - исследуемый образец.
Рисунок 9 - Блок-схема установки для воздействия
ЭМП НЧ на ДНК и белки.
Нужная частота выставлялась на панели генератора
низкочастотных сигналов ГЗ-118, который передавал сигнал, с необходимыми
характеристиками, на катушку. Экранированная камера была необходима для
локализации магнитного поля, создаваемого катушкой внутри камеры, и ослабления
его характеристик за пределами камеры. Эппендорфы с исследуемыми образцами (ДНК
раствор, белковый раствор), помещались в экранированную камеру, в которой
располагалась катушка индуктивности, и подвергались воздействию ЭМП НЧ.
Температура, при которой производили облучение, составляла 23-250С.
По истечению данного времени содержимое эппендорфа моментально было перемещено
в кювету хемилюминометра для регистрации воздействия электромагнитного поля
данной частоты, вызвавшего стимуляцию к протеканию экзотермических реакций
окисления с выделением энергии в виде потока фотонов, что и представляет из
себя явление хемилюминесценции.
.3.1 Устройство хемилюминометра
Хемилюминометр - аппаратно-программный комплекс,
предназначенный для регистрации и анализа сверхслабых световых потоков,
сопровождающих химические и биологические процессы, протекавшие с образованием
свободных радикалов. Блок-схема приведена на рисунке 10.
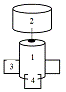
Рисунок 10 - Блок-схема основных функциональных
элементов хемилюминометра Lum-5773
Хемилюминометр состоит из следующих функциональных блоков:
Кюветное отделение - предназначенное для размещения в приборе исследуемых образцов.
Миксер - выполняет функцию светоизоляции исследуемых образцов от внешней среды, а так же перемешивание исследуемых образцов с помощью встроенного электромотора.
Термостат - предназначен для поддержания постоянной температуры исследуемых образцов.
Фотоэлектронный умножитель - предназначен для измерения интенсивности свечения исследуемых образцов.
Блок электроники - предназначен для
управления всеми компонентами прибора и передачи результатов измерений на
компьютер.
.4 Обработка водных растворов нуклеиновых кислот
и их ампликонов ЭМИ. Обработка белковой структуры (альбумина) ЭМИ
После полимеразной цепной реакции, водный раствор нуклеиновых кислот их ампликонов белков низкочастотным электромагнитным излучением.
Облучение проводили в специальном стеклянном
сосуде при комнатной температуре. Время облучения составляло 8-10 минут.
Обработка водных растворов нуклеиновых кислот и их ампликонов осуществлялась
низкочастотным излучением на частотах от 7.5-8.5 Гц с шагом 0,1 Гц, от 9-15 Гц
с шагом 1 Гц и от 15,5-16,5 с шагом 0,2 Гц. Обработка водных растворов белков
осуществлялась на частотах 7,4 - 8,5 Гц с шагом 0,1-0,2 Гц. Толщина облученного
образца ~ 2 мм; Напряженность поля в месте нахождения образца - 30 мкТл.
.4.1 Снятие спектров хемилюминесценции модельных растворов нуклеиновых кислот
Полученные зависимости напряжения
фотоэлектронного умножителя от времени для необлученного образца раствора ДНК
представлены на рисунке 11.
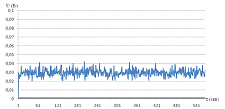
Рисунок 11- Регистрация световых потоков необлученного раствора ДНК (калибровка)
Обнаружено в ходе проведенного эксперимента, что наибольшее влияние на растворы ДНК оказывает частота ЭМП 9 Гц. Именно при этой частоте наблюдается максимальная величина интенсивности хемилюминесценции.
Эта частота является резонансной, а интенсивность хемилюминесценции образцов ДНК, полученная при этой частоте, гладко убывающей, что подтверждает ее верность относительно условных погрешностей и аппаратных флуктуаций хемилюминометра.
Из рисунка 11 видно, что раствор без источника возбуждения, не имеет фотонного отклика, а среднее значение напряжения ФЭУ достаточно мало. На рисунке 12 фотонный отклик заметно увеличивается, вероятно, потому что частота облучения близка к Шумановской резонансной частоте.
Интенсивность хемилюминесценции образца с более
высоким импульсом колебаний относительно остальных частот приведен на рисунке
12 , а образца с самым высоким колебательным спектром - на рисунке 13.
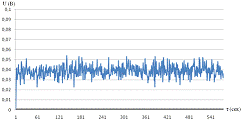
Рисунок 12 - Регистрация световых потоков после
облучения раствора ДНК при частоте 7,8 Гц
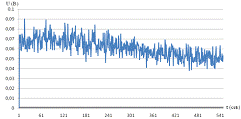
Рисунок 13 - Регистрация световых потоков после облучения раствора ДНК при частоте 9 Гц
Довольно высокие импульсы получились при облучении раствора частотой 9 Гц. Тот факт, что произошел резонансный отклик именно на этой частоте, подтверждает эксперимент.
В виду чрезвычайно малой частоты колебаний генератора, допускается так же некоторая погрешность генератора ЭМИ. Поэтому вполне возможно, что определить абсолютно точно частоту, вызвавшую резонанс, сложно.
Для наглядности общего эксперимента по облучению
ДНК, целесообразно представить общий усредняющий график зависимости
интенсивности хемилюминесценции водных растворов ДНК от частоты ЭМП НЧ при
различных частотах воздействия (рисунок 14).