Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с
40 |
Глава 2 |
|
|
Пример. Найдем относительное число N/N частиц, рассеянных в интервале углов от 1 до 2. Остальное предполагается заданным.
Величина N/N пропорциональна согласно (2.9) площади кольца, внутренний и внешний радиусы которого равны b1 и b2, т. е.
N/N n( b |
2 |
b |
2 ). |
(*) |
|
2 |
|
1 |
Значения же b1 и b2 однозначно связаны с углами 1 и 2 формулой (2.1) или (2.2). Заменив параметр b в (*) выражением (2.2), получим:
N |
0 |
2 |
|
|
|
|
|
|||
|
n |
|
|
ctg2 |
2 |
ctg2 |
1 |
. |
||
N |
2K |
2 |
2 |
|||||||
|
|
|
|
|
||||||
Вот и весь расчет. Практически так и следует поступать.
Проверка формулы Резерфорда. Формула (2.7) была подтверждена экспериментально. В качестве налетающих частиц использовали -частицы (их заряд q 2e) от радиоактивного источника. Кинетическая энергия -частиц была порядка нескольких МэВ.
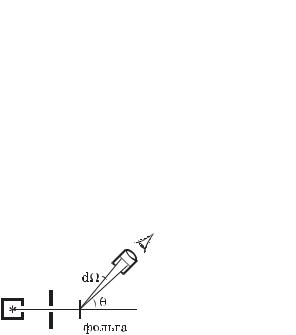
Если зафиксировать телесный угол d , в котором подсчитывают рассеянные -частицы, и менять при этом угол (рис. 2.3), то из формулы (2.7) следует, что
|
dN · sin4( /2) const. |
(2.11) |
|
На опыте прежде всего было прове- |
|
|
рено соблюдение именно этого усло- |
|
|
вия. Оказалось, что, несмотря на то, |
|
|
что каждый из сомножителей в левой |
|
|
части (2.11) изменялся (в процессе из- |
|
|
менения угла ) на три порядка, их |
|
|
произведение с хорошей |
точностью |
Рис. 2.3 |
оставалось постоянным. Это означает, |
|
|
что формула (2.7) правильно описыва- |
|
|
ет процесс рассеяния -частиц. |
|
Опыты, подтверждающие формулу Резерфорда, могут рассматриваться как косвенное доказательство справедливости закона Кулона на весьма малых расстояниях (от 10–12 до 10–9 см).

Атом Резерфорда — Бора |
41 |
|
|
Кроме того, они свидетельствуют в пользу предположения, что масса атома практически сосредоточена в очень малой его области — в ядре, размеры которого не превышают 10–12 см.
Пример. Найдем расстояние, на которое приблизится -частица к неподвижному ядру атома золота, двигаясь точно по направлению к его центру. Порядковый номер атома золота Z 79 и кинетическая энергия налетающей -частицы вдали от ядра K 5,7 МэВ.
В момент остановки -частицы ее кинетическая энергия целиком переходит в потенциальную: K 2Ze2/rмин. Отсюда
rмин |
2 Ze2 |
|
2 79 (4,8 10 10 )2 |
4 10 12 см. |
|
K |
5,7 1,6 10 6 |
||||
|
|
|
Из вышесказанного не следует, что закон Кулона справедлив на любых расстояниях между налетающей частицей и ядром. Опыты по рассеянию, например, протонов, ускоренных ускорителем, показали, что при достаточно больших энергиях наблюдаются резкие отступления от закона Кулона, когда прицельный параметр становится менее 10–12 cм. На таких расстояниях проявляют свое действие ядерные силы притяжения, значительно превосходящие кулоновские силы отталкивания.
Итак, результаты опытов по рассеянию -частиц говорят в пользу ядерной (планетарной) модели атома, предложенной Резерфордом. Однако эта модель оказалась в резком противоречии с законами классической электродинамики.
Предположение, что электроны движутся вокруг ядра по траекториям, подобно планетам вокруг Солнца, наталкивается на непреодолимую (с точки зрения классики) трудность. Двигаясь по искривленным траекториям, электрон испытывает ускорения, а значит неизбежно должен излучать электромагнитные волны. Этот процесс сопровождается потерей энергии, в результате чего электрон должен в конечном счете упасть на ядро. Время жизни такого атома оказывается порядка 10–11 с (см. задачу 2.5). Этот результат красноречиво говорит о степени неустойчивости рассмотренной модели атома.
42 |
Глава 2 |
|
|
§2.2. Спектральные закономерности
Впервую очередь нас будут интересовать спектры, обусловленные излучением невзаимодействующих друг с другом атомов. Эти спектры состоят из отдельных узких спектральных линий, и их называют линейчатыми.
Наличие многих спектральных линий указывает на сложность внутреннего строения атома. Изучение атомных спектров послужило ключом к познанию внутренней структуры атомов. Прежде всего было замечено, что спектральные линии расположены не беспорядочно, а образуют серии линий. Изучая линейчатый спектр атомарного водорода, Бальмер (1885) установил следующую закономерность. В современных обозначениях она выглядит так*:
|
1 |
|
1 |
|
|
R |
|
|
|
, n 3, 4, 5, ..., |
(2.12) |
|
|
||||
22 |
|
n2 |
|
|
|
где — циклическая частота, соответствующая каждой спектральной линии ( 2 c/ ), R — постоянная Ридберга:
R 2,07 · 1016 с–1. |
(2.13) |
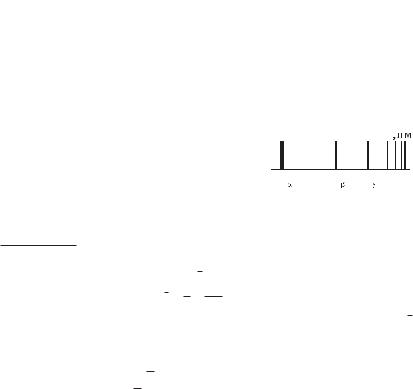
Формулу (2.12) называют формулой Бальмера, а соответствующую серию спектральных линий — се- 
 рией Бальмера (рис. 2.4). Основные ли-
рией Бальмера (рис. 2.4). Основные ли-  нии этой серии находятся в видимой части спектра.
нии этой серии находятся в видимой части спектра. 
Дальнейшие исследования спектра
Рис. 2.4
атомарного водорода показали, что имеется еще несколько серий. В ультрафиолетовой части спек-
*В спектроскопии принято характеризовать спектральные линии не частотой, а
так называемым волновым числом n:
1
=2 c см–1,
где — длина волны. Формула Бальмера, написанная для волнового числа n, имеет такой же вид, как (2.12):
|
|
|
|
|
1 |
|
1 |
|
|
|
|
|
|
|
|
||||
|
n |
= R |
|
|
|
|
, |
||
|
|
|
|
|
22 |
|
n 2 |
|
|
где постоянная Ридберга R имеет значение
R = R/2 c = 109737,31 см–1.

Атом Резерфорда — Бора |
|
|
|
43 |
|
|
|
|
|
|
|
тра — серия Лаймана: |
|
|
|
|
|
1 |
|
1 |
|
|
|
R |
|
|
|
, n 2, 3, 4, ..., |
(2.14) |
|
|
||||
12 |
|
n2 |
|
|
|
а в инфракрасной части спектра — серия Пашена:
|
1 |
|
1 |
|
|
R |
|
|
|
, n 4, 5, 6, ..., |
(2.15) |
|
|
||||
32 |
|
n2 |
|
|
|
а также серии Брэкета и Пфунда.
Все эти серии можно представить в виде обобщенной формулы Бальмера:
|
1 |
|
1 |
|
|
|
|
|
|
|
|
||
R |
2 |
2 |
|
, |
(2.16) |
|
n0 |
|
n |
|
|
|
|
где n0 1 для серии Лаймана, n0 2 для серии Бальмера и т. д. При заданном n0 число n принимает все целочисленные значения, начиная с п0 1.
Максимальной длине волны серии Лаймана (2.14) отвечает
n 2, это макс 2 c/ мин 8 c/3R 121,6 нм. Соответствующую спектральную линию называют резонансной линией водорода.
С ростом n частота линий в каждой серии стремится к предельному значению R/n20 , которое называют границей серии (см. рис. 2.4). За границей серии спектр не обрывается, а становится сплошным. Это присуще не только всем сериям водорода, но и атомам других элементов.
Пример. Найдем спектральный интервал, в пределах которого расположены линии серии Бальмера атомарного водорода (в длинах волн).
Границы данного интервала — это головная линия серии, 32, соответствующая n 3 в формуле (2.12), и граница серии, (n ). Имея в виду, что частота связана с длиной волны как 2 c/ , получим
32 |
|
2 c |
656 нм, |
|
|
2 c |
365 нм. |
|
|
||||||
|
|
R(5/36) |
|
|
R/4 |
||
Таким образом, интересующая нас серия заключена в спектральном интервале от 365 до 656 нм, т. е. действительно, все основные линии ее расположены в видимой области спектра.

44 |
Глава 2 |
|
|
§ 2.3. Постулаты Бора. Опыты Франка и Герца
Постулаты Бора. Абсолютная неустойчивость планетарной модели Резерфорда и вместе с тем удивительная закономерность атомных спектров, и в частности их дискретность, привели Н. Бора к необходимости сформулировать (1913) два важнейших постулата квантовой физики:
1.Атом может длительное время* находиться только в определенных, так называемых стационарных состояниях, которые характеризуются дискретными значениями энергии E1, E2, E3, ...
Вэтих состояниях, вопреки классической электродинамике, атом не излучает.
2.При переходе атома из стационарного состояния с боль-
шей энергией E2 в стационарное состояние с меньшей энергией E1 происходит излучение кванта света (фотона) с энергией h :
h E2 – E1. |
(2.17) |
|
|
Такое же соотношение выполняется и в случае поглощения, когда падающий фотон переводит атом с низшего энергетического уровня E1 на более высокий E2, а сам исчезает.
Соотношение (2.17) называют правилом частот Бора. Заметим, что переходы атома на более высокие энергетические уровни могут быть обусловлены и столкновением с другими атомами.
Таким образом, атом переходит из одного стационарного состояния в другое скачками (их называют квантовыми). Что происходит с атомом в процессе перехода — этот вопрос в теории Бора остается открытым.
Опыты Франка и Герца (1913). Эти опыты дали прямое доказательство дискретности атомных состояний. Идея опытов заключается в следующем. При неупругих столкновениях электрона с атомом происходит передача энергии от электрона атому. Если внутренняя энергия атома изменяется непрерыв-
*Это время порядка 10–8 с. В макроскопическом масштабе такое время крайне мало. Однако в атомной шкале времени оно весьма велико, поскольку на мно-
го порядков превосходит период обращения электрона вокруг ядра, например, атома водорода, равный порядка 10–16 с.