Материал: Иродов. т5 Квантовая физика Основные законы. 2014, 256с

Атом Резерфорда — Бора |
45 |
|
|
но, то атому может быть передана любая порция энергии. Если же состояния атома дискретны, то его внутренняя энергия при столкновении с электроном должна изменяться также дискретно — на значения, равные разности внутренней энергии атома в стационарных состояниях.
Следовательно, при неупругом столкновении электрон может передать атому лишь определенные порции энергии. Измеряя их, можно определить значения внутренних энергий стационарных состояний атома.
Это и предстояло проверить экспериментально с помощью установки, схема которой показана на рис. 2.5. В баллоне с парами ртути под давлением порядка 1 мм 

 рт. ст. (% 130 Па) имелись три электрода:
рт. ст. (% 130 Па) имелись три электрода: 

 K — катод, С — сетка и A — анод. Элек-
K — катод, С — сетка и A — анод. Элек- 
 троны, испускаемые горячим катодом
троны, испускаемые горячим катодом 
 вследствие термоэлектронной эмиссии,
вследствие термоэлектронной эмиссии, 
 ускорялись разностью потенциалов V
ускорялись разностью потенциалов V
между катодом и сеткой. Величину V можно было плавно менять. Между сет-
кой и анодом создавалось слабое тормозящее поле с разностью потенциалов около 0,5 В.
Таким образом, если какой-то электрон проходит сквозь сетку с энергией, меньшей 0,5 эВ, то он не долетит до анода. Только те электроны, энергия которых при прохождении сетки больше 0,5 эВ, попадут на анод, образуя анодный ток I, доступный измерению. 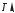
В опытах (см. рис. 2.5) исследовалась зависимость анодного тока I (гальванометром G) от ускоряющего напряжения V (вольтметром V). Полученные результаты представлены на рис. 2.6.
Максимумы |
соответствуют значениям |
|
энергии E1 4,9 эВ, E2 2E1, E3 3E1 |
||
и т. д.* |
Рис. 2.6 |
|
|
|
|
*Заметим, что кривая I(V) на рис. 2.6 имеет такой вид лишь в случае, если отсутствует внешняя контактная разность потенциалов между катодом и сеткой. Наличие же приводит к смещению кривой I(V) влево или вправо.
Относительное же расположение максимумов зависит только от рода газа (атомов). Величину можно исключить, если энергию E1 измерять по «расстоянию» между соседними максимумами, что обычно и делают.
46 |
Глава 2 |
|
|
Такой вид кривой объясняется тем, что атомы действительно могут поглощать лишь дискретные порции энергии, равные 4,9 эВ.
При энергии электронов, меньшей 4,9 эВ, их столкновения с атомами ртути могут быть только упругими (без изменения внутренней энергии атомов), и электроны достигают сетки с энергией, достаточной для преодоления тормозящей разности потенциалов между сеткой и анодом. Когда же ускоряющее напряжение V становится равным 4,9 В, электроны начинают испытывать вблизи сетки неупругие столкновения, отдавая атомам ртути всю энергию, и уже не смогут преодолеть тормозящую разность потенциалов в пространстве за сеткой. Значит, на анод А могут попасть только те электроны, которые не испытали неупругого столкновения. Поэтому, начиная с ускоряющего напряжения 4,9 В, анодный ток I будет уменьшаться.
При дальнейшем росте ускоряющего напряжения достаточное число электронов после неупругого столкновения успевает приобрести энергию, необходимую для преодоления тормозящего поля за сеткой. Начинается новое возрастание силы тока I. Когда ускоряющее напряжение увеличится до 9,8 В, электроны после одного неупругого столкновения достигают сетки с энергией 4,9 эВ, достаточной для второго неупругого столкновения. При втором неупругом столкновении электроны теряют всю свою энергию и не достигают анода. Поэтому анодный ток I начинает опять уменьшаться (второй максимум на рис. 2.6). Аналогично объясняются и последующие максимумы.
Из результатов опытов следует, что разница внутренних энергий основного состояния атома ртути и ближайшего возбужденного состояния равна 4,9 эВ, что и доказывает дискретность внутренней энергии атома.
Аналогичные опыты были проведены в дальнейшем с атомами других газов. И для них были получены характерные разности потенциалов, их называют резонансными потенциалами или первыми потенциалами возбуждения. Резонансный потенциал соответствует переходу атома с основного состояния в ближайшее возбужденное. Для обнаружения более высоких возбужденных состояний была использована более совершенная методика, однако принцип исследования оставался тем же.

Атом Резерфорда — Бора |
47 |
|
|
Итак, все опыты такого рода приводят к заключению, что состояния атомов изменяются лишь дискретно.
Опыты Франка и Герца подтверждают также и второй постулат Бора — правило частот. Оказывается, что при достижении ускоряющего напряжения 4,9 В пары ртути начинают испускать ультрафиолетовое излучение с длиной волны 253,7 нм. Это излучение связано с переходом атомов ртути из первого возбужденного состояния в основное. Действительно, из условия (2.17) следует, что
E2 |
E1 |
|
2 c |
|
2 3 1010 1,054 10 27 |
4,9 эВ. |
|
|
253,7 10 7 1,6 10 12 |
||||||
|
|
|
|
|
Этот результат хорошо согласуется с предыдущими измерениями.
§ 2.4. Боровская модель атома водорода
Чтобы получить согласие с результатами наблюдений, Бор предположил, что электрон в атоме водорода движется только по тем круговым орбитам*, для которых его момент импульса
M nh, n 1, 2, 3, ..., |
(2.18) |
где n — квантовые числа.
С помощью этого правила квантования можно найти радиусы круговых стационарных орбит водородоподобных систем (H, He+, Li++...) и соответствующие им энергии. Пусть заряд ядра водородоподобной системы равен Ze. Масса ядра значительно больше массы электрона, поэтому ядро при движении электрона можно считать неподвижным. Следуя Бору, будем предполагать, что электрон движется вокруг ядра по окружности радиуса r.
Согласно 2-му закону Ньютона
m |
v |
2 |
|
Ze |
2 |
, |
(2.19) |
|
|
|
|
||||
|
|
|
|
||||
|
r |
r2 |
|
||||
*Позднее Зоммерфельд обобщил рассуждения Бора на эллиптические орбиты. Однако в настоящее время это потеряло значение, и мы оставим данный вопрос без внимания.

48 Глава 2
где т —масса электрона. Отсюда кинетическая энергия электрона
K |
mv 2 |
|
Ze |
2 |
, |
(2.20) |
|
|
|
22r
иполная энергия электрона в кулоновском поле ядра
E K U |
mv 2 |
|
Ze 2 |
|
Ze |
2 |
. |
(2.21) |
2 |
r |
|
|
|||||
|
|
|
2r |
|
||||
Согласно правилу квантования (2.18), rmv nh, откуда
v nh/rm. |
(2.22) |
После подстановки (2.22) в (2.19) получим выражение для радиуса n-й стационарной орбиты:
rn |
|
2 |
|
|
n |
2 |
. |
(2.23) |
|
|
|
|
|
||||
me |
2 |
|
|
|
||||
|
|
|
Z |
|
||||
Радиус первой стационарной орбиты электрона в атоме водорода (n 1, Z 1) равен
r |
h2/me2 0,529 10–8 см. |
(2.24) |
1 |
|
|
Его называют боровским радиусом.
Энергия En электрона на n-й стационарной орбите определяется формулой (2.21), в которой под r надо понимать (2.23). И мы приходим к следующему выражению для Еn:
En |
|
me 4 |
|
Z |
2 |
. |
(2.25) |
2 2 |
|
|
|
||||
|
|
|
n 2 |
|
|||
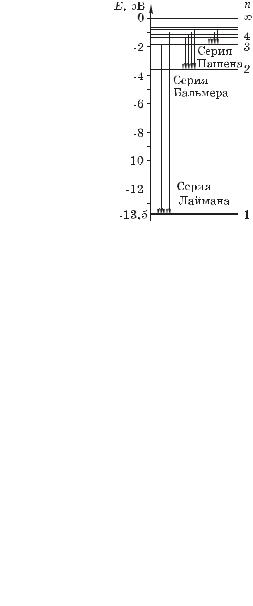
Эта формула описывает уровни энергии стационарных состояний электрона в водородоподобной системе. Для атома водорода схема энергетических уровней, соответствующих (2.25), показана на рис. 2.7. При n & уровни энергии сгущаются к своему предельному значению E 0.
Состояние атома с наименьшей энергией (n 1) называют основным. Для атома водорода основному состоянию соответствует энергия E1 –13,53 эВ. Эта энергия (по модулю) является
Атом Резерфорда — Бора |
49 |
|
|
энергией связи электрона в основном со- |
|
стоянии: Eсв E1. Именно такую энер- |
|
гию надо сообщить электрону в основ- |
|
ном состоянии (n 1), чтобы удалить его |
|
из атома водорода. По этой причине ее |
|
называют еще и энергией ионизации: |
|
Eион Eсв 13,6 эВ. |
|
Это значение, полученное из боровской |
|
теории атома, находится в хорошем со- |
|
гласии с результатами эксперимента. |
|
Пример. Найдем скорость электрона на пер- |
|
вой боровской орбите атома водоро- |
|
да. |
|
Для этого в формулу (2.22) подста- |
Рис. 2.7 |
|
вим (2.23) с учетом того, что в на-
шем случае Z 1 и n 1. В результате получим:
v1 e2/h 2,2 · 106 м/с.
Спектральные серии водородоподобных систем. Согласно второму постулату Бора (2.17), определяющему энергию фотонов при переходе системы из одного стационарного состояния в другое, и формуле (2.24) имеем:
|
|
|
|
|
|
|
me |
4 |
Z |
2 |
1 |
|
1 |
|
|
|||||||
E |
|
E |
|
|
|
|
|
|
|
|
. |
(2.26) |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
2 |
|
|
1 |
|
|
|
2 |
2 |
|
|
|
|
2 |
|
n |
2 |
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
n |
1 |
|
2 |
|
|
||||
Отсюда частота фотона |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
me |
4 |
Z |
2 |
1 |
|
|
|
1 |
|
|
|
|
|
||||||
|
|
|
|
|
|
|
. |
|
|
(2.27) |
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
2 |
3 |
|
|
2 |
|
|
|
n |
2 |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
n1 |
|
|
|
2 |
|
|
|
|
|
|||||
Таким образом, мы пришли к обобщенной формуле Бальмера (2.16), установив при этом, от каких величин зависит постоянная Ридберга:
R |
me |
4 |
. |
(2.28) |
|
|
|||
|
|
|||
|
2 3 |
|
||