Материал: Ионика твёрдого тела
5. Гальванические элементы
.1 Общие замечания
Кроме общеизвестного применения в качестве химических источников тока,
гальванические элементы могут также использоваться как источники информации о
веществах и процессах. Объединив три известных уравнения:
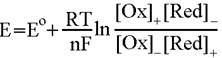
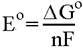
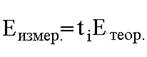
получим
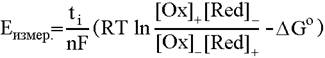
Здесь индексами + и - помечены концентрации (точнее, активности или парциальные давления) окисленных и восстановленных форм на положительном и отрицательном электроде соответственно, взятые в степенях, соответствующих коэффициентам в уравнении потенциалопределяющей реакции.
Не следует забывать, что эдс определяется в условиях термодинамического
равновесия, т.е. в отсутствие тока. Поэтому для её измерения применяется либо
компенсационный (мостовой) метод, либо вольтметр с очень большим входным
сопротивлением, порядка 109 Ом и более. Если сопротивление вольтметра не очень
велико, то в цепи течёт заметный ток, и электроды поляризуются, равновесие
нарушается. Кроме того, если велико внутреннее сопротивление гальванического
элемента, на него приходится значительная доля эдс, и вольтметр показывает
заниженное значение даже в отсутствие поляризации электродов. При пользовании
таким вольтметром измеряемое напряжение может при нагревании гальванической
ячейки возрастать (из-за уменьшения внутреннего сопротивления ячейки), даже
если эдс при нагревании убывает.
5.2 Гальванические элементы с твёрдыми
электролитами
Задание: собрать твёрдофазный элемент, изучить его эдс в зависимости от температуры и определить термодинамические параметры протекающей реакции. Для учебных целей предлагаются не самые технически важные, а самые простые в исполнении гальванические ячейки. Предлагаемые варианты: Ag | AgI | C, S и Ag | AgI | C, V2O5, но по указанию преподавателя возможны и другие варианты.
Эти элементы выбраны потому, что окислители и восстановитель относительно устойчивы на воздухе, а электролит пластичен, и хороший контакт достигается простым прессованием. В обоих случаях окислитель - диэлектрик, и к нему для электронной проводимости примешивается сажа или толчёный графит. Кроме того, для улучшения контакта рекомендуется подмешать твёрдый электролит. Таким образом, катодная масса готовится перетиранием в ступке иодида серебра, углерода и окислителя (серы или оксида ванадия). Оптимальное соотношение нужно подбирать опытным путём, но удовлетворительный результат получается при одинаковых массовых долях всех трёх фаз. Поскольку сажа - самый лёгкий компонент, её объёмная доля будет наибольшей.
Подготовьте серебряный электрод, как описано выше в подразделе 3.7, положите его на дно прессформы, засыпьте порошком электролита и слегка придавите пуансоном (не прессом, а вручную). Затем засыпьте катодную массу и опять придавите. Количества порошков подбираются так, чтобы толщина каждого слоя в прессованном виде была 1,5-3 мм. В ряде случаев (см. ниже) рекомендуется сделать прослойку из одного углерода, засыпав его поверх катодной массы. Для повышения прочности туда можно подмешать в ступке каплю органического клея (резинового, БФ-6 и т.п.). Окончательно придавите всё это гидравлическим прессом для получения монолитного гальванического элемента. Если он после выдавливания из прессформы рассыпается, нужно его переделать. Если боковая сторона электролита запачкана углеродом - осторожно счистите его наждачной бумагой, иначе элемент получится короткозамкнутым.
Установите элемент в нагреваемую ячейку и зажмите его между контактами. Чтобы сера при плавлении не вытекала на серебро, она должна быть снизу. Впрочем, при небольшом содержании она удерживается капиллярными силами. Особое внимание следует уделить контакту с катодом. Если он будет точечным, то может расколоть прессовку. Если он будет из материала, способного реагировать с окислителем (например, из того же серебра), то появятся продукты их взаимодействия, осложняющие эксперимент. Поэтому необходима прослойка из инертного электронного проводника. При использовании серы металлические прослойки не годятся, нужно использовать графитовую пластинку или припрессованный углерод, как описано выше. Под него уже можно положить серебряную или платиновую фольгу для более равномерного распределения нагрузки. При использовании оксида ванадия можно вместо углерода проложить платиновую фольгу.
Термостатируйте элемент при нескольких температурах и измеряйте эдс, отмечая полярность. Постройте зависимость эдс от температуры. Обратите внимание на фазовые переходы: плавление серы при 119°С и полиморфное превращение AgI при 146°С. Отражаются ли они на графике? Согласуется ли это с теоретическими ожиданиями?
Обратите внимание, что в системе с оксидом ванадия можно ожидать
образования как ванадатов, например, AgVO3, так и ванадиевой бронзы AgxV2O5. Напишите уравнения электродных
процессов, суммарные уравнения потенциалопределяющих реакций и предложите, как
выбрать правильный вариант без анализа продукта (ведь его образуется ничтожно
мало). Вычислите DG° для каждой температуры, где есть признаки установления равновесия, а
также средние значения DH° и DS°. Если они определены и ниже, и выше точки плавления серы, то
по ним можно найти также DH° и DS° процесса плавления серы. Найдите в справочниках эти
термодинамические параметры, сравните со своими результатами и, если есть
существенные различия, обсудите их возможные причины.
5.3 Литиевый аккумулятор
В коммерческих литий-ионных аккумуляторах стараются обеспечить минимальное внутреннее сопротивление, поэтому предельно сближают электроды, а для отрицательного электрода используют специально подготовленный углерод для внедрения лития, который лучше циклируется, чем чистый литий, и не образует дендритов. Но в данной работе предлагается не изготовление мощного малогабаритного аккумулятора (хотя такую задачу надо всегда иметь в виду!), а изучение свойств оксидного материала положительного электрода, поэтому для чистоты эксперимента используется чистый литий, а во избежание короткого замыкания используется большое межэлектродное расстояние. В таких случаях применяют трёхэлектродную стеклянную ячейку в виде буквы Ш или Ж: в среднее колено помещают исследуемый электрод, а в боковые - два литиевых электрода. Через один из них (рабочий или токовый) пропускают ток при заряде и разряде аккумулятора, а другой (электрод сравнения или потенциальный) не поляризуется, т.к. ток через него не идёт, и относительно него измеряется потенциал оксидного электрода.
В качестве активных материалов положительного электрода можно испытать LiCoO2, LiNiO2, LiMn2O4, полученные твердофазными реакциями из разных исходных веществ, при разных температурах, с разным размером частиц, с разными легирующими добавками, или Li2Ni2MnO6, полученный ионным обменом (см. п. 2.4.5). Для придания электронной проводимости к ним подмешивается сажа, а для лучшего сцепления - связующее, нерастворимое в электролите, например, политетрафторэтилен в виде раствора в 1-метил-2-пирролидоне.
Отвесьте на аналитических весах оксидный материал и сажу в соотношении примерно 7:1. Точно соблюдать это соотношение не обязательно, но точные навески нужно знать, чтобы потом правильно найти количество вещества в электроде. Тщательно разотрите вместе эти навески в ступке, прикапайте раствор связующего в таком количестве, чтобы масса сухого вещества в нём составляла 1-2 % готовой смеси, и продолжайте растирать до получения однородной вязкой пасты. Подготовьте коллектор тока в виде фольги или сетки из алюминия или никеля такого размера, чтобы входил в горлышко ячейки, взвесьте на аналитических весах, намажьте на него кисточкой приготовленную пасту, оставив свободный конец для крепления, высушите при 60-70°С (лучше всего - в вакууме), охладите и взвесьте опять. По разности определите массу электродной смеси и, зная её состав, массу активного вещества в ней. Далее следует рассчитать количество электричества, необходимое для извлечения всего содержащегося там лития, чтобы затем относить к нему реально пропущенное количество электричества и знать степень превращения. Укрепите электрод на контакте пробки, вставляемой в среднее колено трёхэлектродной ячейки. Эти процедуры можно делать на воздухе, но работу с металлическим литием и электролитом нужно вести в защитной атмосфере - в перчаточном боксе.
В качестве электролита используется раствор соли лития - гексафторфосфата или перхлората - в апротонном растворителе - смеси эфиров. Мешают кислород, азот и влага, которые взаимодействуют с литием. Кроме того, влага в электролите вызывает гидролиз LiPF6, а образующийся HF реагирует с оксидным материалом. Приготовление и осушка электролита сложны, лучше всего использовать готовый безводный электролит, который поставляется в герметичной упаковке и довольно дорог. Загрузите в бокс все необходимые материалы, посуду и инструменты, продуйте его сухим аргоном или углекислым газом для вытеснения воздуха, затем вскройте в боксе банку с осушителем - фосфорным ангидридом - пересыпьте его в широкую чашку и оставьте на сутки. Только после этого можно вскрывать упаковку лития и электролита, и то лишь на короткое время. Вырежьте два литиевых электрода, очистите их от вазелина и укрепите на пробках. Залейте в ячейку электролит, погрузите в него все три электрода, убедитесь, что оксидный электрод полностью покрыт электролитом, а литиевые погружены частично, и плотно закройте. Только после этого можно извлекать ячейку из бокса. Описанная процедура требует большого расхода времени, аргона и осушителя. Поэтому целесообразно накопить достаточно много материалов и заряжать все ячейки сразу.
Для испытания электрохимических характеристик электродного материала желательно использовать программируемый потенциостат-гальваностат, а при его отсутствии - источник регулируемого постоянного напряжения, миллиамперметр и самопишущий потенциометр. В крайнем случае можно обойтись вольтметром, но тогда показания придётся записывать вручную. Изучить все свойства материала на одном образце вряд ли удастся. Обсудите план работы с преподавателем. Возможна, например, такая схема эксперимента.
Проводим зарядку аккумулятора в гальваностатическом режиме (I=const), регистрируя напряжение относительно литиевого электрода сравнения и откладывая его в функции x - степени извлечения лития. Силу тока выбираем таким образом, чтобы зарядка на половину теоретической ёмкости проходила за разумное время - порядка часа. Если при этом возникает сильная поляризация, т.е. требуется слишком большое напряжение (больше 4,5 В), которое может вызвать разложение электролита, ток придётся уменьшить, а время эксперимента увеличить. Зарядка прекращается, если напряжение достигнет предельно допустимого, или по достижении заранее оговоренной величины x (например, 0,5). Далее проводим разряд, опять-таки в гальваностатическом режиме с регистрацией напряжения в функции x. При отсутствии потенциостата или стабилизатора тока придётся разряжать аккумулятор на переменное сопротивление, а постоянство силы тока поддерживать регулировкой вручную. Удаётся ли получить обратно при разряде то же количество электричества, которое было пропущено при заряде? Сильно ли отличаются зарядные и разрядные напряжения?
Если в первом цикле материал вёл себя удовлетворительно, далее следует повторить заряд-разряд несколько раз для проверки циклируемости: сохраняются ли параметры, наблюдавшиеся в первом цикле? Они могут и ухудшаться, и улучшаться!
Поляризация электрода может быть обусловлена малой скоростью диффузии лития в твёрдой фазе. Мы рассчитываем величину x, среднюю по объёму зерна, а реально она сильно изменяется на поверхности и мало изменяется в глубине зерна. Поэтому интересно также провести заряд и разряд с паузами, в которых ток отключается, и измеряется изменение напряжения разомкнутой цепи. По мере выравнивания состава по объёму зёрен это напряжение приближается к равновесному значению эдс. Но быстро ли? Если электрод плохо ведёт себя при большой силе тока, это может быть обусловлено не свойствами вещества как такового, а слишком крупным размером частиц или плохим контактом с сажей, или недостаточным её количеством.
Если материал хорошо циклируется в пределах заданных выше 50% теоретической ёмкости, интересно проверить максимально возможную глубину его заряда: заряжать небольшим током, пока напряжение не достигнет допустимого предела, а затем извлечь электрод, промыть его и исследовать рентгенографически.
Если необходимо рентгенографическое исследование на промежуточных стадиях
заряда-разряда, без извлечения электрода ("in situ"), то стеклянная трёхэлектродная ячейка не
годится. Предложена ячейка из никеля, титана или нержавеющей стали в виде
кюветы рентгеновского дифрактометра, герметически закрываемая
полуцилиндрической полиэтиленовой крышкой (рис. 6).
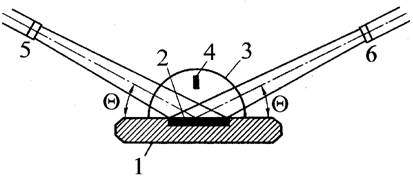
Рисунок 6 - Схема ячейки для рентгенофазового анализа электродного материала в процессе работы (in situ) [14]
- корпус ячейки, 2 - исследуемый электрод, 3 - крышка, 4 - литиевый
электрод, 5 - рентгеновская трубка, 6 - детектор дифрагированного излучения
При горизонтальном положении ячейки оба электрода омываются электролитом, и может идти электрохимический процесс. Когда её поворачивают вертикально, электролит стекает в имеющийся приёмник, и можно проводить РФА. Затем её поворачивают обратно и продолжают электрохимический процесс. При подготовке образца к такому комплексному исследованию рекомендуется для введения поправок в брегговские углы и для количественного РФА ввести в него 15-25 % инертного внутреннего эталона, например, BaF2.
Список рекомендуемой литературы
1. Иванов-Шиц, А.К. Ионика твёрдого тела [Текст]: монография / А.К. Иванов-Шиц, И.В. Мурин. - С.-Петербург: Изд-во С-Петербургского университета, 2010. - Т. 1. - 616 с.
. Вест, А. Химия твёрдого тела [Текст]: монография / А. Вест. - М.: Мир. - 1988. Ч. 2. - С. 5-58, 306-307.
. Чеботин, В.Н. Электрохимия твёрдых электролитов [Текст]: монография / В.Н. Чеботин, М.В. Перфильев. - М.: Химия, 1978. - 312 с.
. Укше, Е.А. Твёрдые электролиты [Текст]: монография / Е.А. Укше, Н.Г. Букун. - М.: Химия, 1977. - 176 с.
. Рао, Ч.Н.Р. Новые направления в химии твёрдого тела [Текст]: монография / Ч.Н.Р. Рао, Дж. Гопалакришнан. - Новосибирск: Наука. - 1990.
. Налбандян, В.Б. Задачник по химии твёрдого тела с примерами решений [Текст]: учеб. пособие / В.Б. Налбандян, Е.А. Кандюшева. - Ростов-на-Дону: УПЛ ЮФУ (готовится к печати).
. Беляев, И.Н. Солевые расплавы в химии и технологии сложных оксидов. 1. Обменные реакции солевых расплавов и сложных оксидов [Текст] / И.Н. Беляев, Т.Г. Лупейко, В.Б. Налбандян // Ионные расплавы и твёрдые электролиты. - Киев: Наукова думка, 1986. - Вып. 1. - С. 1-13.
. Справочник по плавкости систем из безводных неорганических солей. Т. 1. Двойные системы [Текст] / Н.К. Воскресенская [и др.]. - М.-Л.: Изд-во АН СССР. - 1961. - 846 с.
. Третьяков, Ю.Д. Твердофазные реакции [Текст]: монография / Ю.Д. Третьяков. - М.: Химия, 1978. - 360 с.
10. Paulsen, J.M. Layered T2-, O6-, O2-, and P2-type A2/3[M1/3'2+M2/34+]O2 bronzes, A = Li, Na; M' = Ni, Mg; M = Mn, Ti [Текст] / J.M. Paulsen, R.A. Donaberger, J.R. Dahn // Chem. Mater. - 2009. - V. 12. - № 8. - P. 2257-2267.
11. Налбандян, В.Б. Сравнение различных методик и источники ошибок определения удельного сопротивления керамических катионных проводников на примере силикатов натрия-РЗЭ [Текст] / В.Б. Налбандян, Л.И. Медведева, Н.Г. Судоргин, Б.С. Медведев // Электрохимия. - 1993. - Т. 29. - № 11. - С. 1380-1387.
. Шукаев, И.Л. Иммиттансная спектроскопия [Текст]: учеб. пособие / И.Л. Шукаев, А.А. Поспелов. - Ростов-на-Дону: УПЛ ЮФУ (готовится к печати).
. Налбандян, В.Б. Материалы литий-ионных аккумуляторов [Текст]: учеб. пособие / В.Б. Налбандян, В.Е. Гутерман, Б.С. Медведев. - Ростов-на-Дону: УПЛ ЮФУ (готовится к печати).
. Судоргин, Н.Г. Методика количественного рентгенографического контроля электродных процессов в герметичных ячейках. Восстановление b-молибдата циркония литием [Текст] / Н.Г. Судоргин, В.Б. Налбандян // Электрохимия. - 2012. - Т. 28. - № 1. - С.122-123.